-
电压门控钠离子通道2A(SCN2A)基因(染色体2q24.3),编码电压门控钠离子通道Ⅱ型(Nav1.2)的α2亚基,在中枢神经系统动作电位产生与传播中发挥关键作用[1-2]。SCN2A基因突变可导致癫痫、发育落后、孤独症谱系障碍、精神分裂症、智力低下等多种神经系统疾病[3]。既往研究[4]发现,SCN2A基因突变导致的癫痫表型谱较广泛,不仅可以表现为良性癫痫,还可能导致大田原综合征、West综合征、Dravet综合征以及其他癫痫性脑病。
大田原综合征是年龄依赖性癫痫性脑病的最早发病形式,多数有严重的先天性脑发育异常或围产期脑损伤,在新生儿出生后3个月内起病,表现为频繁的强直痉挛性癫痫发作,脑电图为特征性爆发抑制图形,同时伴有严重的精神运动发育落后,癫痫发作难以控制,预后极差,病死率高,存活者可演变为West综合征和Lennox-Gastaut综合征。约60%的病例由电压门控钠离子通道1A(SCN1A)、SCN2A或KCNQ2基因突变引起,SCN2A功能获得性突变可通过钠通道持续激活导致神经元超兴奋,此类患者对钠通道阻滞剂(如苯妥英钠)可能具有显著的治疗应答。
本文报道了1例SCN2A基因突变导致大田原综合征的患儿治疗经过。由于大田原综合征患者对多种抗癫痫药物有耐药性,临床药师参与了该患儿药学治疗全过程,借助治疗药物监测(therapeutic drug monitoring, TDM)优化患儿的治疗方案,以确保药物在安全有效的治疗范围内[5],为临床治疗SCN2A基因突变致大田原综合征提供依据。
-
患儿,男,年龄26日龄,系第一胎第一产(G1P1),胎龄36+4周,因孕母“胎心监护异常;高危妊娠监督(胎儿股骨长小6周)”剖宫产娩出,阿普加(Apgar)评分10/10分,出生体重2 550 g,出生后逐渐出现气促、口吐泡沫,入住新生儿科。患儿入院检查:体温36.5℃,脉搏149次/min,呼吸60次/min。患儿神智清楚,易激惹,反应一般,口唇紫绀,四肢末梢紫绀,口吐泡沫,呼吸急促,双肺呼吸音粗糙,可闻及湿性啰音,心率律齐,心前区I/6 收缩期杂音(systolic murmur,SM),腹平软,四肢肌张力降低。
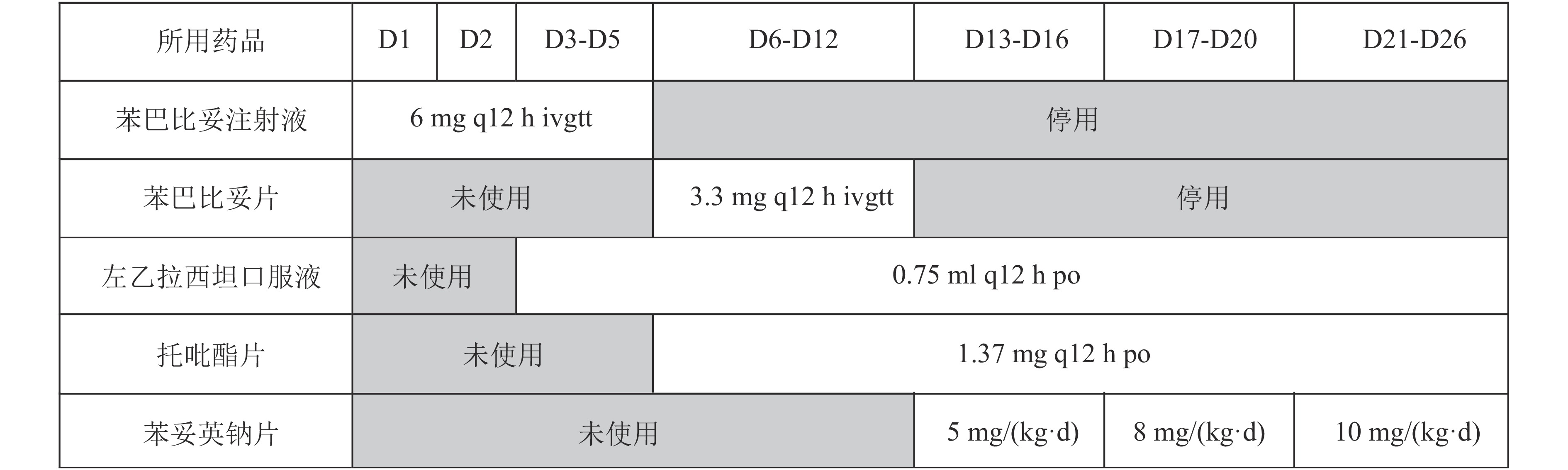
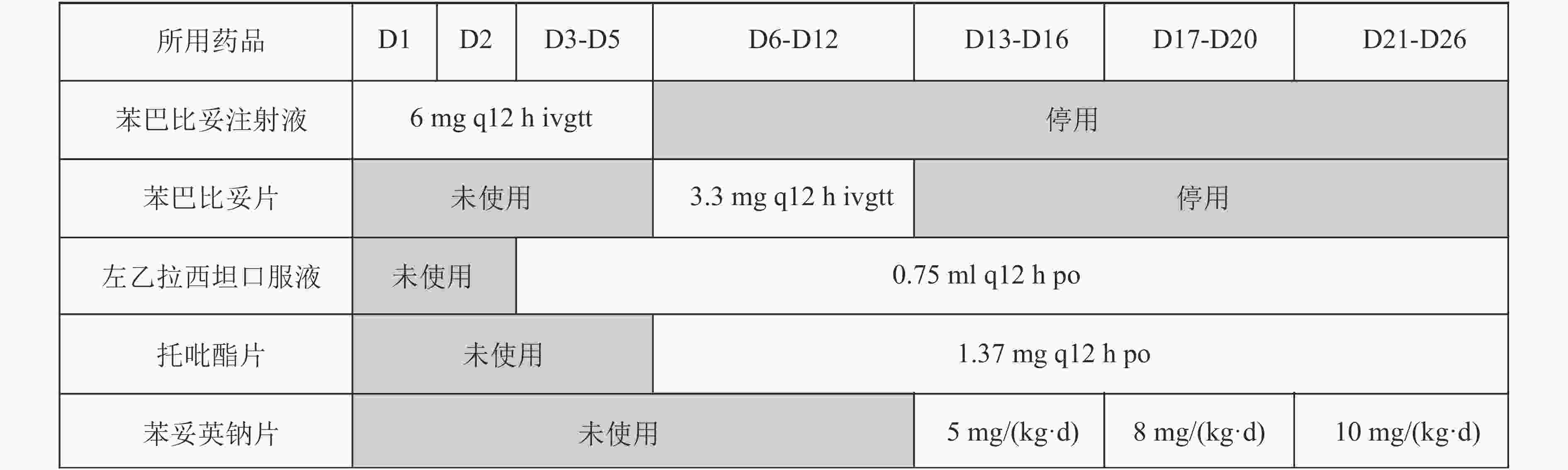
入院第1天,患儿出现癫痫发作,予以苯巴比妥注射液6 mg q12 h ivgtt治疗,3 d后仍有癫痫发作,加用左乙拉西坦0.75 ml q12 h po治疗,完善辅助检查显示:血氨43.7 μmol/L,胸片提示左肺透亮度减低,心脏彩超提示房间隔缺损(Ⅱ孔、多孔型),头颅MRI提示左侧侧脑室前角盘小出血灶,视频脑电图提示爆发抑制,诊断为大田原综合征。入院第6天,临床医生停用苯巴比妥注射液,针对大田原综合征,初始给药方案调整为口服左乙拉西坦口服液0.75 ml q12 h、托吡酯片1.37 mg q12 h及苯巴比妥片3.3 mg q12 h联合抗癫痫治疗。
联合抗癫痫治疗1周后,患儿癫痫仍无法控制,考虑治疗效果不佳。基因检测显示SCN2A基因突变(c.770T>C, p.Phe257Ser),根据该基因致病特点,临床医生拟加用奥卡西平口服液,家属因奥卡西平相关不良反应拒绝使用。针对SCN2A基因突变相关的癫痫性脑病,奥卡西平作为一种钠通道阻断剂,有研究显示对携带SCN2A基因变异的癫痫患者可能有效。也有研究指出,钠通道阻断剂可能在某些患者中加剧癫痫发作[4]。
考虑到患儿现用的抗癫痫药物方案疗效不佳,与家属沟通后逐渐减停苯巴比妥(图1),入院第13天,停用苯巴比妥片后加用苯妥英钠抗癫痫治疗,患儿26日龄,体重5.2 kg,初始给药剂量为5 mg/(kg·d),入院后第17天(给药后第3天),苯妥英钠血药浓度为4 μg/ml,期间患儿仍有频繁抽搐发作。苯妥英钠的有效治疗血药浓度通常在10~20 μg/ml[6]。患儿目前的血药浓度低于有效治疗浓度范围,这可能是导致患儿抽搐发作未得到控制的原因之一。因此,临床药师建议增加苯妥英钠的剂量,并考虑患儿体重增加情况,以达到有效的血药浓度。由于苯妥英钠的半衰期为7~42 h,需要一段时间才能达到稳态血药浓度。因此,临床药师建议苯妥英钠加量至8 mg/(kg·d)(患儿体重为5.25 kg),入院后第21天(调整剂量后3 d)。患儿血药浓度为7 μg/ml,患儿仍有抽搐发作,临床药师再次建议将苯妥英钠剂量增加至10 mg/(kg·d)(患儿体重为5.7 kg),调整剂量后3 d,血药浓度为10.2 μg/ml,在有效治疗浓度范围内,后续患儿未出现癫痫发作,维持原方案继续治疗。患儿在该方案治疗5 d后出院,患儿用药过程详见图1。
-
由SCN2A基因突变导致的癫痫往往与钠通道功能的改变有关,因此针对特定基因型的治疗可能更为有效。例如,SCN2A突变导致Nav1.2通道功能增强,表现为增益功能,可能对钠通道阻断剂有更好的反应。因此,对于此类患者,可以考虑使用钠通道阻断剂进行治疗。尽管奥卡西平/卡马西平被推荐为SCN2A基因突变治疗的一线药物,但本例患儿因家属担心药物不良反应未能使用。值得注意的是,苯妥英钠通过选择性结合失活态钠通道,显著降低通道再开放概率[6],其疗效可能与突变特异性通道动力学改变相关,提示同类突变患者可优先考虑苯妥英钠。
-
SCN2A基因突变导致的癫痫性脑病多呈难治性,同时SCN2A突变引起的大田原综合征表型多为功能增强型,钠离子通道阻滞剂如奥卡西平、卡马西平、苯妥英钠、拉莫三嗪等能使SCN2A基因突变导致的癫痫发作缓解或减少,但对部分患儿无效,可能与药物浓度未达标有关[1]。
苯妥英钠是一种钠离子阻滞剂,通过减少钠离子内流,降低神经元的兴奋性,从而控制癫痫发作。由于SCN2A基因突变导致的大田原综合征在临床表现和严重程度存在异质性,因此个体化给药尤为重要。苯妥英钠在新生儿中的应用存在双重挑战:① CYP2C9/CYP2C19代谢酶活性随日龄动态变化,导致剂量-浓度关系难以预测;②血脑屏障发育不成熟可能增加游离药物比例[7]。
本例中10 mg/(kg·d)剂量下,血药浓度10.2 μg/ml虽仅达常规治疗窗下限(10~20 μg/ml),但仍能实现无癫痫发作,其机制可能涉及以下两方面:①游离药物比例升高,新生儿期低白蛋白血症可降低苯妥英钠蛋白结合率(正常结合率90%),导致游离药物浓度显著增加(即使总浓度偏低),而本例未检测血清白蛋白水平及游离药物浓度。②突变特异性通道敏感性增强:SCN2A突变导致钠通道失活延迟(功能获得性),使神经元对钠通道阻滞剂的反应阈值降低。苯妥英钠通过优先结合失活态通道,可能在该突变背景下产生超常疗效。
本例患儿前期三联抗癫痫治疗效果不佳,可能是由于未联用钠离子通道阻滞剂,根据2015年国际抗癫痫联盟推荐指南,对于SCN2A基因突变相关的癫痫性脑病,应考虑使用钠离子通道阻滞剂作为治疗手段。不推荐苯妥英钠用于3月以下婴儿,因为苯妥英钠的药代动力学特征在婴儿体内可能与成人不同,且婴儿的代谢和排泄能力尚未完全发育,可能会导致药物在体内积累,增加毒副作用风险。此外,苯妥英钠的说明书中指出,其最大剂量为8 mg/(kg·d),而有效治疗血药浓度范围仅为10~20 μg/ml。这意味着在婴儿中使用苯妥英钠需要非常谨慎,以避免剂量过高导致的不良反应。因此,3个月以下婴儿在治疗时使用苯妥英钠需要密切监测血药浓度。
-
本例中,临床药师主导TDM流程(每3 ~5 d测定血药浓度),结合癫痫发作频率与脑电图演变,逐步调整剂量。初始剂量阶段5 mg/(kg·d):给药后第3天监测苯妥英钠血药浓度为4 μg/ml,低于治疗窗(10~20 μg/ml),患儿仍频繁抽搐(5~6次/d)。医疗团队决定维持当前剂量并密切观察72 h,排除其他诱因(如代谢紊乱或感染)。首次剂量调整为8 mg/(kg·d):增量后第3天血药浓度升至7 μg/ml,癫痫发作频率减少50%(2~3次/d)。经神经科评估,患儿未出现眼球震颤或共济失调等神经毒性体征,药师建议继续上调剂量。目标剂量10 mg/(kg·d);剂量调整后3 d,血药浓度达到10.2 μg/ml(治疗窗下限),患儿癫痫发作完全终止。同期脑电图显示背景节律连续性改善,爆发−抑制模式消失。临床药师与医疗团队确认疗效后维持该剂量,并制定出院随访计划。
同时监测到患儿使用苯妥英钠出现的不良反应呈剂量与时间依赖性:急性毒性(血药浓度>20 μg/ml)表现为眼球震颤、共济失调、意识障碍;慢性毒性(长期用药)表现为齿龈增生、骨代谢异常、巨幼红细胞贫血(叶酸拮抗效应)。
本例患儿治疗周期短(累计用药14 d),总浓度始终低于中毒阈值,且通过以下策略规避风险:①药学监护,每日监测生命体征、喂养耐受性及神经行为变化;②实验室筛查,基线及每周检测血红蛋白(维持120~130 g/L)、肝功能(ALT/AST无异常);③药物相互作用管理,停用苯巴比妥后,苯妥英钠代谢速率恢复正常,避免浓度波动。
-
本文首次证实苯妥英钠在SCN2A p.Phe257Ser突变新生儿中的剂量−效应关系,突破传统新生儿用药禁忌,为同类病例提供以下启示:SCN2A突变分型应作为抗癫痫药物选择的核心依据;新生儿苯妥英钠治疗需以TDM为基础,结合基因表型制定个体化目标浓度。
多学科协作模式可显著提升难治性癫痫救治的成功率,特别是临床药师利用TDM保障了患儿的用药安全。
本文报道了1例SCN2A基因突变致大田原综合征患儿,其癫痫发作频繁且使用3种抗癫痫药物治疗后仍难以控制癫痫发作,在此情况下,加用苯妥英钠抗癫痫治疗,同时指导患儿家属密切观察药物不良反应,交代用药和日常生活注意事项。经上述治疗后病情得到有效控制,遂予以出院,考虑患儿需长期口服抗癫痫药物,医嘱其定期到医院随访。本例SCN2A基因突变致大田原综合征患儿的药学监护实践表明,精准治疗与药学监护相结合,可以有效控制患儿病情,改善预后。
-
-
关键词:
- 电压门控钠离子通道2A /
- 基因突变 /
- 大田原综合征 /
- 药学监护
-
[1] 国志, 郑芳, 赵鹏军. 癫痫伴热性惊厥病儿SCN1A、SCN2A基因突变特点及表型分析[J]. 安徽医药, 2025, 29(2): 319-324. [2] 董晓立, 李花, 张佩琪, 等. SCN2A基因突变所致癫痫的遗传和表型特点[J]. 卒中与神经疾病, 2022, 29(3): 274-280. [3] 孙明霞, 华颖, 王艳萍, 等. 1例SCN2A基因突变早发癫痫性脑病的诊断及治疗[J]. 山东医药, 2022, 62(9): 66-68. [4] ZENG Q, YANG Y, DUAN J, et al. SCN2A-related epilepsy: the phenotypic spectrum, treatment and prognosis[J]. Front Mol Neurosci, 2022, 15: 809951. doi: 10.3389/fnmol.2022.809951 [5] PATEL N, MADI P, MONTEIRO I, et al. The anesthetic management of a child with ohtahara syndrome and severe stridor: a case report[J]. BMC Pediatrics, 2024, 24(1): 434. doi: 10.1186/s12887-024-04907-8 [6] MOON JU, CHO KO. Current pharmacologic strategies for treatment of intractable epilepsy in children[J]. Int Neurourol J, 2021, 25(Suppl 1): S8-18. [7] FALLAH MS, EUBANKS JH. Seizures in mouse models of rare neurodevelopmental disorders[J]. Neuroscience, 2020, 445: 50-68. doi: 10.1016/j.neuroscience.2020.01.041 -




 下载:
下载: