-
高尿酸血症(hyperuricemia,HUA)的发生是由于尿酸代谢异常,从而引起体内血清尿酸水平升高的疾病,已成为继高血压、糖尿病、高脂血症之后,威胁人类健康的又一重要代谢性疾病[1]。近年来,有较多研究发现尿酸过高会加重HUA患者的肾损伤,从而导致高尿酸肾病的发生,其损伤机制是通过尿酸盐晶体沉积、氧化应激反应诱导、炎症信号通路激活等多重病理机制,直接导致肾小管损伤、肾间质纤维化和肾小球硬化,进而加速肾功能恶化[2]。
目前HUA的主要治疗方案是抑制尿酸产生和促进尿酸排泄。肾为调节尿酸代谢的主要器官。常用的一线药物(如别嘌呤醇等)虽能有效降低尿酸,但治疗手段单一且易发生毒副作用,例如胃肠道反应及过敏反应等[3],影响安全用药。鉴于中医药在HUA治疗中具有多靶点、副作用小、安全性高等特点,其重要性日益显著。因此,全面归纳具有肾保护作用的降尿酸中药研究动态,不仅可以优化现有的治疗策略,也对推进HUA合并肾病患者的个体化治疗具有关键的临床意义。
-
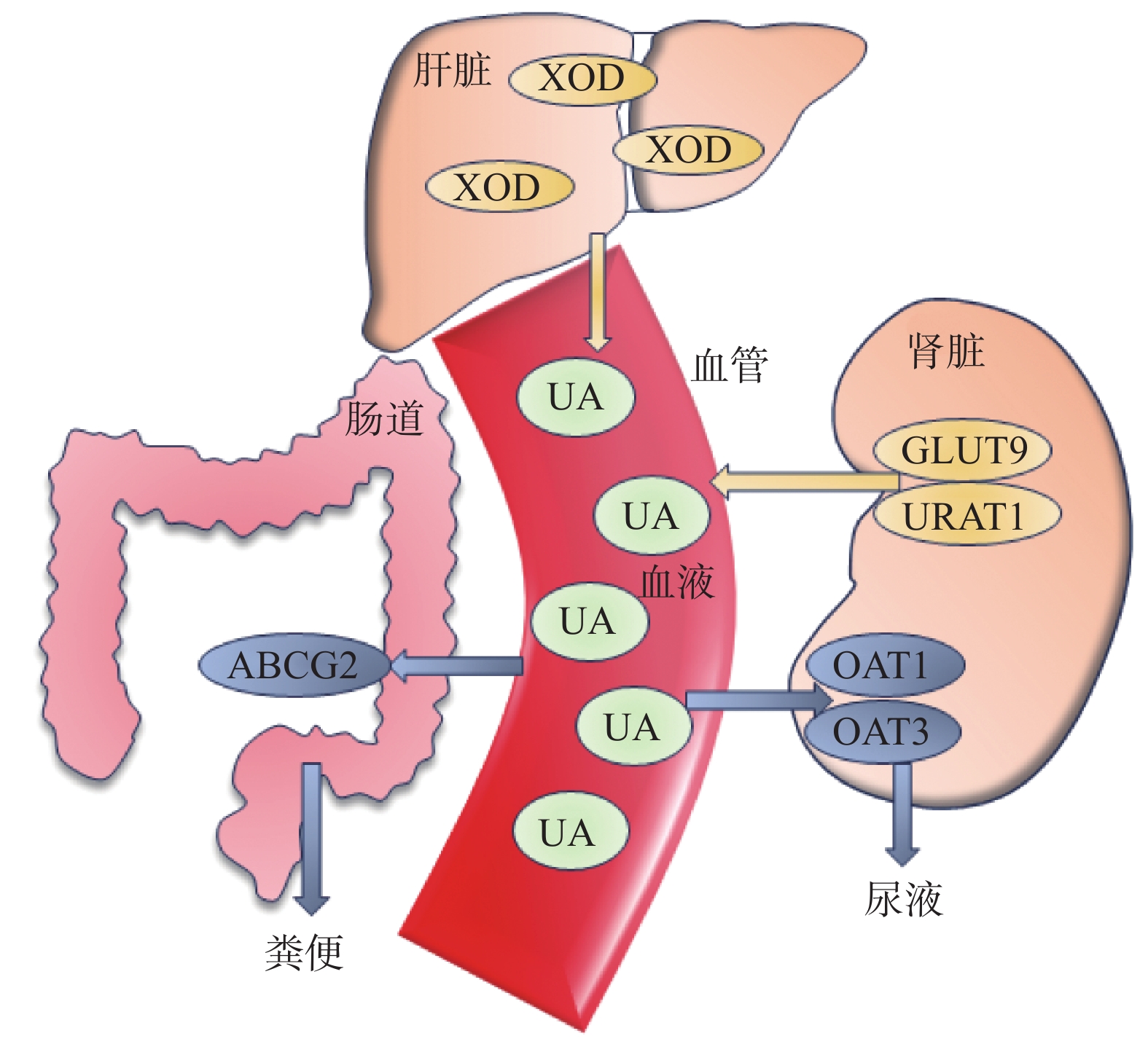
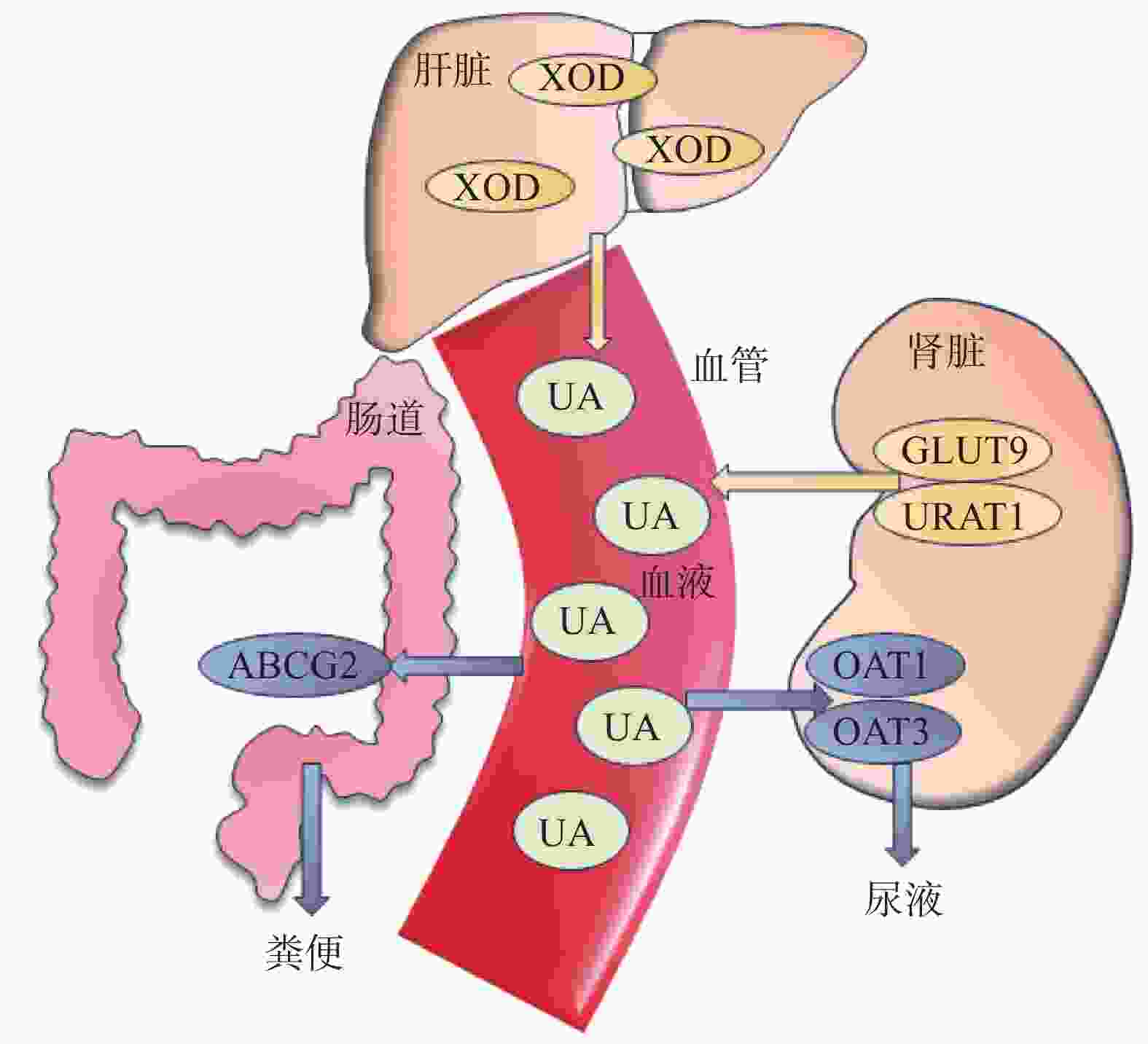
尿酸作为人体嘌呤代谢的最终产物,主要经由肾(约占70%)和肠(约占30%)排出体外,尿酸在经过肾小球过滤后,大部分会被肾小管重吸收。这一吸收与排泄过程主要通过近端肾小管上多种跨膜转运蛋白共同实现,包括尿酸转运体1(URAT1)、葡萄糖转运体9(GLUT9)[4]及有机阴离子转运体1(OAT1)和OAT3等[5]。尿酸的调控过程如图1所示。
当肾功能受到损害时,其尿酸排泄能力迅速下降,从而促进HUA,而HUA本身也通过多种机制反过来进一步损害肾功能[6],两者相互影响,形成恶性循环。
-
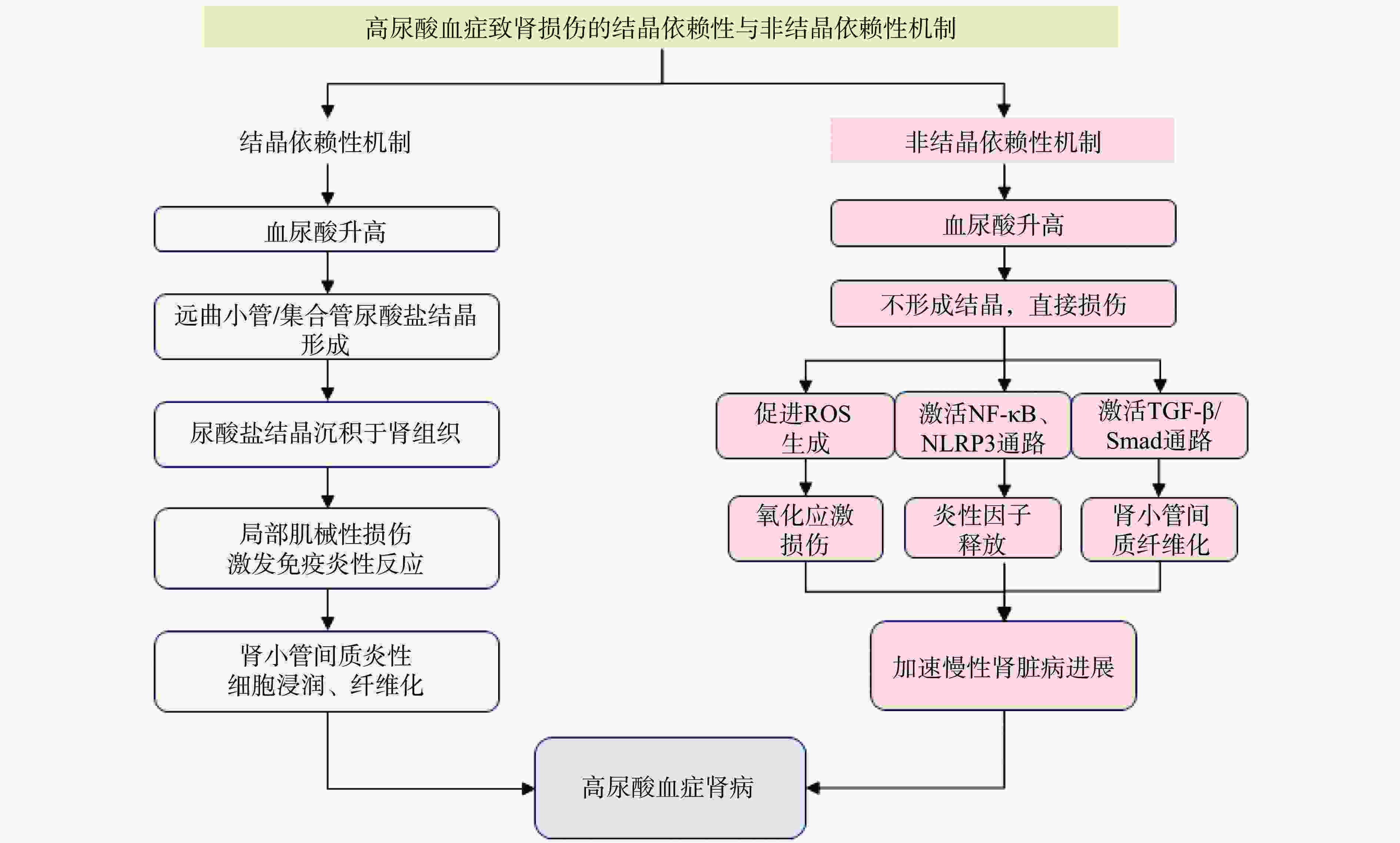
HUA引起肾损伤的机制主要包括结晶依赖性与非结晶依赖性两种途径(如图2)。在结晶依赖性机制中,过量的尿酸在远曲小管或集合管内形成尿酸盐结晶,并沉积于肾组织,造成局部机械性损伤,进而激发局部免疫炎症反应,导致肾小管间质的炎性细胞浸润及纤维化,典型的临床表现为高尿酸肾病[7]。在非结晶依赖性机制中,即使未形成尿酸盐结晶,过高水平的尿酸仍可通过多种途径产生肾损害,其作用途径包括促进活性氧(ROS)生成并诱导氧化应激损伤[8];激活NF-κB、核苷酸结合寡聚化结构域样受体蛋白3(NLRP3)等炎症信号通路[9],促进炎性因子释放[10];激活TGF-β/Smad通路,加速肾小管间质纤维化进程[11],上述多种机制加剧了高尿酸肾病的发生。
-
HUA引起的肾损伤一直是临床防治的难题。对于HUA的临床治疗,中医药相较于化学药物具有活性成分来源广、安全性高等优势,且可通过多靶点、多途径作用于多个环节发挥治疗作用。
-
中药方剂是中医特色的治疗方法,在祖国医学的发展中,诞生了如四妙散等用于肾病治疗的经典名方。现代研究发现,四妙散等复方通过抑制黄嘌呤氧化酶(XOD),同时作用于OAT3、URAT1、GLUT9等尿酸转运蛋白,降低血清尿酸水平(表2),并通过抗炎、抗氧化应激、改善肾纤维化等发挥肾保护作用。
表 2 中药复方降尿酸兼具肾保护的作用机制
中药复方名称 涉及通路 调节靶点 四妙散 激活PI3K/Akt通路;调控尿酸代谢通路 ABCG2↑,XOD↓ 痛风清利合剂 抑制JAK2/STAT3信号通路;调控尿酸代谢通路 OAT3↑,URAT1↓,TNF-α↓,IL-1β↓,IL-6↓ 健脾渗湿解毒汤 抑制JAK2/STAT3信号通路;调控尿酸代谢通路 OAT3↑,URAT1↓,TNF-α↓,IL-1β↓,IL-6↓ 痛风宁 调控尿酸代谢通路 XOD↓,ABCG2↑,GLUT9↓ 健脾化湿泄浊方 调控尿酸代谢通路 XOD↓,ABCG2↑, GLUT9↓,URAT1↓,OAT3↑ 石栀方 调控NLRP3/Caspase-1/GSDMD通路 XOD↓,IL-18↓,IL-1β↓,NLRP3↓,Caspase-1↓ 傣痛消 调控TLR4/MyD88/NF-κB通路 XOD↓,IL-18↓,IL-1β↓,TNF-α↓ 四妙散源自清代张秉成编写的《成方便读》,由苍术、牛膝、黄柏、薏苡仁组成,具有逐瘀通经、清热祛湿之效[20]。研究表明,四妙散可通过抑制XOD的活性、上调肠道ATP结合盒亚家族G成员2(ABCG2)表达促进肠道尿酸排泄,从而降低血清中尿酸、血肌酐、尿素氮的含量[21];通过激活PI3K/Akt通路,进而减轻肾损伤,达到肾保护的作用[22]。而在此基础上加减化裁而成的经验方痛风清利合剂[23]和健脾渗湿解毒汤[24],可上调尿酸分泌蛋白OAT3,抑制尿酸重吸收蛋白URAT1的表达以降低血清尿酸水平,通过抑制JAK2/STAT3信号通路、抑制肿瘤坏死因子-α(TNF-α)等炎症因子,达到肾脏保护作用。
痛风宁是基于临床实践基础上创立的经验方,由苍术、牛膝、薏苡仁、黄柏、土茯苓、牡丹皮、泽泻、茵陈蒿、猪苓、威灵仙组成,具有健脾胃、利湿浊的功效。痛风宁治疗HUA可能与降低肠道内腺苷脱氨酶及XOD表达、减少肠道尿酸生成;上调ABCG2及下调GLUT9表达,从而促进肠道尿酸排泄有关[25]。而健脾化湿泄浊方是基于痛风宁基础上把丹参、秦艽、肿节风、泽泻替换为石韦、薏苡仁、菊苣、葛根而成的经验方。研究表明,健脾化湿泄浊方通过抑制XOD活性,减少尿酸生成,上调大鼠模型肾小管上皮细胞OAT3蛋白的表达,下调URAT1蛋白的表达减少尿酸重吸收、促进尿酸排泄,从而降低HUA大鼠的血尿酸水平。二者均通过抑制JAK2/STAT3信号通路,抑制TNF-α、白介素-1β(IL-1β)、IL-6表达[26],从而发挥肾保护作用。
石栀方是临床治疗HUA的有效方,含有车前草、白芥子、王不留行等。临床研究表明石栀方可改善HUA患者的肾功能,减少蛋白尿的生成,同时基础研究也发现石栀方通过NLRP3/Caspase-1/GSDMD途径抑制HUA大鼠肾线粒体ROS触发的NLRP3炎性体激活,减轻肾小管损伤和炎症浸润,从而减轻HUA所致肾损伤[27]。
傣痛消是中国傣族广泛使用的治疗痛风的传统药物,配方由油麻和麦以3∶1的比例组成,已有
2500 多年的历史。当前也被用于缓解尿酸水平升高引起的肾脏疾病。研究显示药物通过抑制XOD活性来减少尿酸生成,下调TLR4/MyD88/ NF-κB通路蛋白抑制(IL-18、TNF-α等)减轻炎症损伤,进而增强肾的保护作用[28]。 -
目前研究较多的中药提取物主要包括生物碱类、黄酮类、多糖类等,肾保护作用主要集中在抗炎、抗氧化以及抑制细胞凋亡等途径。
-
黄柏是治疗痛风和HUA的常用药物,小檗碱是其降尿酸的主要有效成分之一。研究发现,小檗碱通过下调GLUT9和URAT1和上调OAT1、OAT3、ABCG2的表达来发挥治疗HUA作用,通过AMPK调节巨噬细胞极化抑制JAK2/STAT3信号通路来改善肾损伤[29]。
青风藤属于祛风湿药,具有祛风除湿、通络止痛、利水消肿之功效。研究发现,其主要活性成分青藤碱具有显著抗炎作用,可通过降低HUA大鼠的TNF-α、IL-18及环氧化酶-2(COX-2)的表达来减轻炎症反应及肾损伤[30]。
-
土茯苓为清热药之清热解毒药,具有解毒、除湿、通利关节的作用。其中土茯苓总黄酮为其改善HUA的主要活性成分,研究表明土茯苓不同部位醇提物均具有降低血清尿酸作用,其主要通过上调OAT1、OAT3、ABCG2的表达,来促进尿酸排泄,达到降尿酸目的,并通过抑制IL-1β、IL-6、TNF-α的表达,降低炎症反应,进而缓解肾损伤[31]。
槲皮素是具有多种生物活性的黄酮醇类化合物,广泛存在于多种中药中,具有抗氧化、抗炎等药理作用,可显著抑制HUA小鼠肝XOD活性和肠GLUT9的表达,并增加ABCG2蛋白的表达,从而改变HUA小鼠肠道菌群的多样性,不仅能降低血尿酸水平,还能降低HUA小鼠TNF-α、IL-1β、IL-6的水平,从而发挥肾保护作用[32]。
虎杖作为一种常用的利水渗湿药,具有止咳化痰、清热解毒、散瘀止痛、利胆退黄的功效。虎杖苷和大黄素是其主要活性成分,其主要通过抑制XOD活性的生成来降低HUA模型大鼠血清中尿酸的含量,通过下调NLRP3/Caspase-1/GSDMD通路蛋白表达及抑制肾小管上皮细胞凋亡发挥肾保护作用[33]。
异鼠李素是存在于多种天然植物中的一种黄酮类化合物,具有抗炎、抗氧化等广泛的药理活性,能够通过抑制XOD活性来减少尿酸的产生。降低GLUT9表达抑制尿酸重吸收,增强ABCG2、OAT1、OAT3表达促进尿酸排泄,降低肾脏炎症因子(TNF-α、IL-1β和IL-6)水平,最终改善小鼠HUA所致的肾炎症[34],从而减轻肾损伤。
另外,儿茶素、芒果苷在肾脏保护方面也可能具有潜在作用。前者是茶叶中重要的活性成分,因其具有抗炎、抗氧化及降血脂等良好的药理活性,现已成为研发抗HUA药物的先导化合物,其主要通过抑制XOD活性,来达到降尿酸目的[35]。芒果苷为知母的主要活性成分,主要作用机制是抑制XOD活性,调节ABCG2的表达,抑制尿酸生成和促进尿酸排泄[36]。
-
车前子为利水渗湿药之利尿通淋药,具有利尿、通淋、清热、明目的功效,研究表明,其有效成分车前子多糖具有降低尿酸水平和抗炎作用的双重作用,其主要通过调节XOD和腺苷脱氨酶(ADA),调控尿酸转运蛋白(GLUT9、URAT1、ABCG2和OAT1)的表达,显著降低血清尿酸水平。此外,车前子多糖抑制TNF-α和IL-1β的表达,从而减轻肾功能损伤[37]。
桑黄多糖是一种常见的药用真菌桑黄的主要活性成分之一,在中药中具有广泛应用。其可通过增强HUA小鼠肾肠道中转运体ABCG2的表达,减少肝脏中尿酸的产生和增加肾、肠道中尿酸的排泄,上调肾中NAD+/NADH比值、ATP水平、线粒体超氧化物歧化酶2(SOD2)活性和SOD2/PCG-1α/PPARγ表达,进而改善高尿酸诱导的肾损伤[38]。
-
丹参酮ⅡA是中药丹参中的主要活性成分,具有抗炎、抗氧化等多种药理作用。研究表明,丹参酮ⅡA通过调节XOD活性降低血清尿酸水平[39]。绿原酸是自然界中含量最丰富的酚酸之一,其可抑制XOD活性来降低血清尿酸水平,并显著降低血清脂多糖(LPS)水平和IL-1β、TNF-α、NLRP3和Caspase-1的表达,从而减轻HUA动物肾炎症反应,发挥肾保护作用[40]。
尿酸能够促进炎症反应及氧化应激而造成肾脏功能障碍,而上述中药的活性成分通过调节尿酸转运蛋白的表达以达降尿酸的目的,通过多种途径(抑制炎症因子活化、抗氧化应激等)实现多靶点缓解肾损伤,为治疗痛风性肾病的肾损伤拓宽了思路(表3)。
表 3 中药提取物降尿酸兼具肾保护的作用机制
有效成分 涉及通路 调节靶点 小檗碱 抑制JAK2/STAT3信号通路;尿酸代谢通路 TNF-α↓,IL-1β↓,IL-6↓,XOD↓,GLUT9↓,URAT1↓ABCG2↑,OAT1↑,OAT3↑ 青藤碱 激活AMPK/NF-κB信号通路 TNF-α↓,IL-1β↓,IL-6↓ 土茯苓总黄酮 调控NLRP3/ASC/Caspase-1通路;
调控尿酸代谢通路TNF-α↓,IL-1β↓,IL-6↓XOD↓,ABCG2↑,OAT1↑,OAT3↑,URAT1↓,GLUT9↓ 槲皮素 调控NLRP3/NF-κB信号通路;调控尿酸代谢通路 XOD↓,TNF-α↓,IL-1β↓,IL-6↓,ABCG2↑,GLUT9↓ 儿茶素 调控尿酸代谢通路 XOD↓ 虎杖苷 激活NLRP3炎症小体信号通路 NLRP3↓,Caspase-1↓,GSDMD↓,XOD↓ 芒果苷 调控尿酸代谢通路 ABCG2↑,XOD↓ 异鼠李素 调控PI3K/AKT/NF-κB信号通路;尿酸代谢通路 TNF-α↓,IL-1β↓,IL-6↓,XOD↓,GLUT9↓,ABCG2↑,OAT1↑,OAT3↑ 车前子多糖 调控PI3K/AKT/NF-κB信号通路;尿酸代谢通路 TNF-α↓,IL-1β↓,IL-6↓,XOD↓,GLUT9↓,ABCG2↑,OAT1↑,OAT3↑ 桑黄多糖 线粒体功能相关通路;尿酸代谢通路 SOD2↑、PGC-1α/PPARγ↑,XOD↓,ABCG2↑,OAT1↑,OAT3↑,URAT1↓,GLUT9↓ 丹参酮IIA 抑制尿酸生成 XOD↓ 绿原酸 调控TLR4/MyD88/NF-κB信号通路 TNF-α↓,IL-1β↓,IL-6↓ -
近年来,国内外研究者在HUA性肾损伤的病理机制及治疗方法上取得了显著进展。研究发现,治疗HUA的主流药物如别嘌呤醇、苯溴马隆、非布司他等均通过降尿酸来达到肾保护作用,作用机制较为单一,且具有一定程度的毒副作用[41],影响长期用药。而相关中医药的研究证实了单味中药或方剂(如青风藤、土茯苓、四妙散等)可通过多靶点抑制XOD、调控尿酸转运蛋白(OAT3、URAT1、GLUT9等)多种途径降低血清尿酸水平,同时通过抑制炎症反应、抗氧化应激、抗纤维化等作用,发挥肾保护作用。
未来可通过深度挖掘经典名方的相关经验方,加强相关中医药治疗HUA的多维度研究,扩大单味药的研究范围,应用网络药理学与临床治疗经验相结合的方法,明确相关中药及其有效组分等降尿酸及肾保护的作用机制。在此基础上,开展长期、大样本、前瞻性随机对照临床试验,加强基础机制研究与临床研究相结合,实现HUA的治疗从单纯“降尿酸”向综合“肾保护”的实质性临床治疗转变,为下一步的基础及临床研究提供方向。
Advances in reno-protective effects of traditional Chinese medicine in the treatment of hyperuricemia
-
摘要: 高尿酸血症(HUA)是一种常见的代谢紊乱性疾病,而血清尿酸持续升高则会造成尿酸相关性肾功能损伤。本文对具有降尿酸及肾保护作用的中药复方(如四妙散、痛风宁等)及中药单体组分(包括生物碱类、黄酮类、多糖类等)进行了归纳,并对其可能作用机制进行系统综述,包括调节尿酸转运蛋白(有机阴离子转运体3、尿酸转运体1、葡萄糖转运体9等)机制,抑制炎性反应作用(调控NF-κB等相关信号通路),抗氧化应激(调节线粒体功能相关通路,促进抗氧化酶的生成),减少肾纤维化(PI3K/AKT等相关通路)改善肾组织损伤等。目前相关研究存在作用机制尚未完全明确、临床方向研究不足等问题。因此,未来研究应深入挖掘中医药资源,着重探讨兼具降尿酸与肾保护的作用机制及应用潜力,为HUA肾保护的治疗提供新的思路和方法。Abstract: Hyperuricemia (HUA) is a common metabolic disorder characterized by persistently elevated serum uric acid levels, leading to uric acid-related renal injury through complex mechanisms involving inflammation, oxidative stress, and fibrosis. Key traditional Chinese medicine (TCM) formulas (e.g., Simiao Powder, Tongfengning) and individual herbal compounds (alkaloids, flavonoids, polysaccharides) with urate-lowering and renal protective properties were systematically summarized, including their mechanisms of regulating uric acid transporters (organic anion transporter 3, urate anion transporter 1, glucose transporter type 9), inhibiting inflammatory responses (via NF-κB signaling), reducing oxidative stress (via mitochondrial pathways and antioxidant enzyme enhancement), and attenuating renal fibrosis (via PI3K/AKT signaling). The challenges of current studies mainly focus on unclear mechanisms of action and insufficient clinical research. Future research may further explore TCM resources, clarify dual-action mechanisms of urate reduction and renal protection, and identify new therapeutic strategies for hyperuricemia-related renal injury.
-
Key words:
- hyperuricemia /
- renal injury /
- renoprotection /
- urate-lowering /
- uric acid transporters
-
表 1 治疗高尿酸血症药物的优劣对比
表 2 中药复方降尿酸兼具肾保护的作用机制
中药复方名称 涉及通路 调节靶点 四妙散 激活PI3K/Akt通路;调控尿酸代谢通路 ABCG2↑,XOD↓ 痛风清利合剂 抑制JAK2/STAT3信号通路;调控尿酸代谢通路 OAT3↑,URAT1↓,TNF-α↓,IL-1β↓,IL-6↓ 健脾渗湿解毒汤 抑制JAK2/STAT3信号通路;调控尿酸代谢通路 OAT3↑,URAT1↓,TNF-α↓,IL-1β↓,IL-6↓ 痛风宁 调控尿酸代谢通路 XOD↓,ABCG2↑,GLUT9↓ 健脾化湿泄浊方 调控尿酸代谢通路 XOD↓,ABCG2↑, GLUT9↓,URAT1↓,OAT3↑ 石栀方 调控NLRP3/Caspase-1/GSDMD通路 XOD↓,IL-18↓,IL-1β↓,NLRP3↓,Caspase-1↓ 傣痛消 调控TLR4/MyD88/NF-κB通路 XOD↓,IL-18↓,IL-1β↓,TNF-α↓ 表 3 中药提取物降尿酸兼具肾保护的作用机制
有效成分 涉及通路 调节靶点 小檗碱 抑制JAK2/STAT3信号通路;尿酸代谢通路 TNF-α↓,IL-1β↓,IL-6↓,XOD↓,GLUT9↓,URAT1↓ABCG2↑,OAT1↑,OAT3↑ 青藤碱 激活AMPK/NF-κB信号通路 TNF-α↓,IL-1β↓,IL-6↓ 土茯苓总黄酮 调控NLRP3/ASC/Caspase-1通路;
调控尿酸代谢通路TNF-α↓,IL-1β↓,IL-6↓XOD↓,ABCG2↑,OAT1↑,OAT3↑,URAT1↓,GLUT9↓ 槲皮素 调控NLRP3/NF-κB信号通路;调控尿酸代谢通路 XOD↓,TNF-α↓,IL-1β↓,IL-6↓,ABCG2↑,GLUT9↓ 儿茶素 调控尿酸代谢通路 XOD↓ 虎杖苷 激活NLRP3炎症小体信号通路 NLRP3↓,Caspase-1↓,GSDMD↓,XOD↓ 芒果苷 调控尿酸代谢通路 ABCG2↑,XOD↓ 异鼠李素 调控PI3K/AKT/NF-κB信号通路;尿酸代谢通路 TNF-α↓,IL-1β↓,IL-6↓,XOD↓,GLUT9↓,ABCG2↑,OAT1↑,OAT3↑ 车前子多糖 调控PI3K/AKT/NF-κB信号通路;尿酸代谢通路 TNF-α↓,IL-1β↓,IL-6↓,XOD↓,GLUT9↓,ABCG2↑,OAT1↑,OAT3↑ 桑黄多糖 线粒体功能相关通路;尿酸代谢通路 SOD2↑、PGC-1α/PPARγ↑,XOD↓,ABCG2↑,OAT1↑,OAT3↑,URAT1↓,GLUT9↓ 丹参酮IIA 抑制尿酸生成 XOD↓ 绿原酸 调控TLR4/MyD88/NF-κB信号通路 TNF-α↓,IL-1β↓,IL-6↓ -
[1] ZHANG M, ZHU X X, WU J, et al. Prevalence of hyperuricemia among Chinese adults: findings from two nationally representative cross-sectional surveys in 2015–16 and 2018–19[J]. Front Immunol, 2022, 12: 791983. doi: 10.3389/fimmu.2021.791983 [2] HASSAN W, SHRESTHA P, SUMIDA K, et al. Association of uric acid–lowering therapy with incident chronic kidney disease[J]. JAMA Netw Open, 2022, 5(6): e2215878. doi: 10.1001/jamanetworkopen.2022.15878 [3] GHANG B, PARK J, LEE J S, et al. Post-hoc analysis of the CARES trial suggests delayed progression of chronic kidney disease in patients with gout during urate-lowering therapy[J]. Kidney Int, 2025, 107(3): 521-529. doi: 10.1016/j.kint.2024.10.022 [4] AUBERSON M, STADELMANN S, STOUDMANN C, et al. SLC2A9 (GLUT9) mediates urate reabsorption in the mouse kidney[J]. Pflügers Arch Eur J Physiol, 2018, 470(12): 1739-1751. [5] LI L, ZHAO K L, LUO J, et al. Piperine improves hyperuricemic nephropathy by inhibiting URAT1/GLUT9 and the AKT-mTOR pathway[J]. J Agric Food Chem, 2024, 72(12): 6565-6574. doi: 10.1021/acs.jafc.3c07655 [6] SUIJK DLS, VAN BAAR MJB, VAN BOMMEL EJM, et al. SGLT2 inhibition and uric acid excretion in patients with type 2 diabetes and normal kidney function[J]. Clin J Am Soc Nephrol, 2022, 17(5): 663-671. doi: 10.2215/CJN.11480821 [7] GIBSON T. Hyperuricemia, gout and the kidney[J]. Curr Opin Rheumatol, 2012, 24(2): 127-131. doi: 10.1097/BOR.0b013e32834f049f [8] ZHOU J B, YANG F, ZHANG X M, et al. Jiangniaosuan formula inhibits hyperuricemia-induced apoptosis of renal tubular epithelial cells via ROS/HIF-1α/EZH2 pathway: a network pharmacology analysis and experimental validation[J]. Bioorg Chem, 2025, 159: 108363. doi: 10.1016/j.bioorg.2025.108363 [9] LI X Q, GU Y Q, LING Y Y, et al. Association between mitophagy and NLRP3 inflammasome in uric acid nephropathy[J]. Ren Fail, 2024, 46(2): 2438847. doi: 10.1080/0886022X.2024.2438847 [10] QIAN Y S, ZHANG Y, CHEN Y, et al. Linarin attenuates hyperuricemic nephropathy by modulating Nrf2/Keap1 and TLR4/NF-κB signaling pathways: Linarin attenuates hyperuricemic nephropathy[J]. Phytomedicine, 2025, 139: 156440. doi: 10.1016/j.phymed.2025.156440 [11] WU S H, YAN M X, LIU J Y, et al. Clerodendranthus spicatus inhibits epithelial-mesenchymal transition of renal tubular cells through the NF-κB/Snail signalling pathway in hyperuricaemia nephropathy[J]. Pharm Biol, 2023, 61(1): 1274-1285. doi: 10.1080/13880209.2023.2243086 [12] HELGET L N, DAVIS-KARIM A, O’DELL J R, et al. Efficacy and safety of allopurinol and febuxostat in patients with gout and CKD: subgroup analysis of the STOP gout trial[J]. Am J Kidney Dis, 2024, 84(5): 538-545. doi: 10.1053/j.ajkd.2024.04.017 [13] TERKELTAUB R. Emerging urate-lowering drugs and pharmacologic treatment strategies for gout: a narrative review[J]. Drugs, 2023, 83(16): 1501-1521. doi: 10.1007/s40265-023-01944-y [14] YAMADA T, SAKAI Y, KURIHARA O, et al. Effect of dotinurad on serum uric acid concentration in chronic kidney disease patients treated with febuxostat[J]. J Nippon Med Sch, 2024, 91(4): 352-356. doi: 10.1272/jnms.JNMS.2024_91-403 [15] MOHAMMED A, MARIE M A, ABDULAZIM D O, et al. Serum urate lowering therapy using allopurinol improves serum 25 hydroxy vitamin D in stage 3-5 CKD patients: a pilot study[J]. Nephron, 2021, 145(2): 133-136. doi: 10.1159/000512340 [16] YANG N, CAO B. Low-dose febuxostat exhibits a superior renal-protective effect and non-inferior safety profile compared to allopurinol in chronic kidney disease patients complicated with hyperuricemia: a double-centre, randomized, controlled study[J]. J Clin Pharm Ther, 2022, 47(12): 2214-2222. doi: 10.1111/jcpt.13794 [17] XUE X M, SUN M S, YAN F, et al. Superiority of low-dose benzbromarone add-on to low-dose febuxostat compared with febuxostat monotherapy in gout with combined-type hyperuricemia[J]. Arthritis Care Res, 2024, 76(5): 703-711. [18] 张恩红, 崔璨. 丙磺舒联合别嘌呤醇治疗痛风间歇期临床研究[J]. 中外医疗, 2016, 35(26): 115-117. doi: 10.16662/j.cnki.1674-0742.2016.26.115 [19] OKUI D, SASAKI T, FUSHIMI M, et al. The effect for hyperuricemia inpatient of uric acid overproduction type or in combination with topiroxostat on the pharmacokinetics, pharmacodynamics and safety of dotinurad, a selective urate reabsorption inhibitor[J]. Clin Exp Nephrol, 2020, 24(Suppl 1): 92-102. [20] ZHANG Y, WANG S, DAI X, et al. Simiao San alleviates hyperuricemia and kidney inflammation by inhibiting NLRP3 inflammasome and JAK2/STAT3 signaling in hyperuricemia mice[J]. J Ethnopharmacol, 2023, 312: 116530. doi: 10.1016/j.jep.2023.116530 [21] 张永琪, 陈杰伟, 叶博闻, 等. 四妙丸上调高尿酸血症大鼠小肠ABCG2表达促进肠道尿酸排泄的作用[J]. 中国实验方剂学杂志, 2022, 28(22): 33-39. [22] 王钐, 张悦怡, 刘田园, 等. 四妙散改善高尿酸血症和肾损伤以及调节肾脏线粒体相关蛋白的作用研究[J]. 中草药, 2023, 54(13): 4177-4185. doi: 10.7501/j.issn.0253-2670.2023.13.011 [23] 张婷婷, 党翔, 杨青, 等. 痛风清利合剂通过调节尿酸转运蛋白和JAK2/STAT3信号通路缓解大鼠高尿酸血症[J]. 中国病理生理杂志, 2025, 41(5): 984-994. doi: 10.3969/j.issn.1000-4718.2025.00.014 [24] 叶文静, 杨文奎, 符芸瑜, 等. 健脾渗湿解毒汤对高尿酸血症大鼠的作用及机制探讨[J]. 中国中医基础医学杂志, 2024, 30(1): 41-45. doi: 10.19945/j.cnki.issn.1006-3250.2024.01.006 [25] 张英杰, 毛骁, 肖艳, 等. 痛风宁对高尿酸血症脾虚湿盛证模型小鼠肠道菌群及肠道尿酸代谢的影响[J]. 中医杂志, 2023, 64(21): 2232-2240. doi: 10.13288/j.11-2166/r.2023.21.012 [26] 梁天文, 胡黎平, 黄锦桃, 等. 健脾化湿泄浊方对实验性高尿酸血症大鼠肾功能及XOD活性的影响[J]. 热带医学杂志, 2017, 17(1): 5-7,19,138. [27] ZHOU J B, WANG C X, ZHANG X M, et al. Shizhifang ameliorates pyroptosis of renal tubular epithelial cells in hyperuricemia through inhibiting NLRP3 inflammasome[J]. J Ethnopharmacol, 2023, 317: 116777. doi: 10.1016/j.jep.2023.116777 [28] LIU F F, BAI Y M, WAN Y, et al. DaiTongXiao improves gout nephropathy by inhibiting inflammatory response through the TLR4/MyD88/NF-κB pathway[J]. Front Pharmacol, 2024, 15: 1447241. doi: 10.3389/fphar.2024.1447241 [29] GONG S T, CHEN J Z, ZHENG X H, et al. Kidney targeting and modulating macrophage polarization through AMPK signaling: Therapeutic mechanism of berberine in uric acid nephropathy[J]. Int Immunopharmacol, 2024, 138: 112632. doi: 10.1016/j.intimp.2024.112632 [30] 尹智功, 肖敬, 蒋耀平, 等. 青藤碱对痛风性关节炎模型大鼠TNF-α, IL-1β及COX-2的影响[J]. 广西中医药, 2015, 38(4): 71-74. [31] 彭佳琦, 于志豪, 王浩臻, 等. 土茯苓通过槲皮素抑制黄嘌呤氧化酶降尿酸[J]. 智慧健康, 2023, 9(11): 125-131,136. doi: 10.19335/j.cnki.2096-1219.2023.11.030 [32] PENG B Z, DAI J J, JI S, et al. Quercetin ameliorates hyperuricemic nephropathy through improving gut dysfunctions and decreasing gut bacteria-derived uremic toxins[J]. Phytomedicine, 2025, 143: 156801. doi: 10.1016/j.phymed.2025.156801 [33] SHI X L, ZHUANG L L, ZHAI Z Q, et al. Polydatin protects against gouty nephropathy by inhibiting renal tubular cell pyroptosis[J]. Int J Rheum Dis, 2023, 26(1): 116-123. doi: 10.1111/1756-185X.14463 [34] KONG X R, ZHAO L, HUANG H, et al. Isorhamnetin ameliorates hyperuricemia by regulating uric acid metabolism and alleviates renal inflammation through the PI3K/AKT/NF-κB signaling pathway[J]. Food Funct, 2025, 16(7): 2840-2856. doi: 10.1039/D4FO04867A [35] XIE Q J, CAI X Q, DONG X, et al. Effects of epigallocatechin-3-gallate combined with ascorbic acid and glycerol on the stability and uric acid-lowering activity of epigallocatechin-3-gallate[J]. Pharm Biol, 2021, 59(1): 157-166. doi: 10.1080/13880209.2021.1878235 [36] LI X C, YAN Z X, CARLSTRÖM M, et al. Mangiferin ameliorates hyperuricemic nephropathy which is associated with downregulation of AQP2 and increased urinary uric acid excretion[J]. Front Pharmacol, 2020, 11: 49. doi: 10.3389/fphar.2020.00049 [37] ZHAO J, FU Y, QIU H B. Effect and mechanism of Plantaginis Semen polysaccharides on intestinal microecology in rats with hyperuricemia[J]. Front Microbiol, 2025, 16: 1555734. doi: 10.3389/fmicb.2025.1555734 [38] WANG L, TAO Y F, WANG X S, et al. Aqueous extract of Phellinus igniarius ameliorates hyperuricemia and renal injury in adenine/potassium oxonate-treated mice[J]. Biomed Pharmacother, 2024, 177: 116859. doi: 10.1016/j.biopha.2024.116859 [39] 靳宜静, 李堪董, 詹智晖, 等. 丹参酮ⅡA对小鼠高尿酸血症及并发心肌损伤的影响[J]. 中国组织化学与细胞化学杂志, 2024, 33(3): 232-238. doi: 10.16705/j.cnki.1004-1850.2024.03.004 [40] ZHOU X F, ZHANG B W, ZHAO X L, et al. Chlorogenic acid supplementation ameliorates hyperuricemia, relieves renal inflammation, and modulates intestinal homeostasis[J]. Food Funct, 2021, 12(12): 5637-5649. doi: 10.1039/D0FO03199B [41] LAI S W, LIAO K F, KUO Y H, et al. Comparison of benzbromarone and allopurinol on the risk of chronic kidney disease in people with asymptomatic hyperuricemia[J]. Eur J Intern Med, 2023, 113: 91-97. doi: 10.1016/j.ejim.2023.04.025 -




 下载:
下载: