-
钠-葡萄糖协同转运蛋白2(sodium-dependent glucose transporters 2,SGLT2)抑制剂是一类新型口服降糖药,其通过抑制近端小管对葡萄糖的重吸收,增加葡萄糖从尿液中排泄,从而降低血糖,是一种不依赖于胰岛素的降糖药[1]。目前,我国上市的SGLT2抑制剂有达格列净、恩格列净、卡格列净、艾格列净、恒格列净和贝沙格列净6种。SGLT2抑制剂因降糖疗效确切,兼具心、肾保护等优势[2],临床应用广泛,但也存在一些安全性问题。据国外研究,SGLT2抑制剂可使2型糖尿病(type 2 diabetes mellitus,T2DM)患者发生糖尿病酮症酸中毒(diabetic ketoacidosis,DKA)的风险增加至少7倍,其中71%为非高血糖性酮症酸中毒(euglycemic diabetic ketoacidosis,euDKA)[3]。DKA作为一种严重的糖尿病急性并发症,主要特点是起病急、进展快,患者表现为高血糖、酮症和代谢性酸中毒等,严重者可危及生命[4]。然而,与DKA不同的是,SGLT2抑制剂相关euDKA患者的血糖升高往往不显著,多饮、多尿等症状也不明显,易被临床忽视而延误治疗,造成严重后果[5]。因此,本研究探讨SGLT2抑制剂相关euDKA的影响因素并构建风险预测模型,以期为其预防和早期诊治提供参考。
-
回顾性分析2020年1月至2023年12月于厦门大学附属东南医院接受SGLT2抑制剂治疗的T2DM住院患者的临床资料。纳入标准:①T2DM患者,糖尿病诊断及分型符合《中国2型糖尿病防治指南(2020年版)》的标准[6];②患者接受SGLT2抑制剂治疗,包括达格列净、恩格列净、卡格列净等;③年龄≥18岁。排除标准:①1型糖尿病患者;②未使用SGLT2抑制剂的患者;③出现DKA的患者;④临床资料不完整或失随访的患者;⑤合并重要脏器功能明显异常的患者。本研究经厦门大学附属东南医院医学伦理委员会批准通过。
-
收集患者的临床资料,包括:①个人信息:年龄、性别、体质指数等;②既往史:吸烟史、酗酒史、DKA史、消化系统病史、用药期间手术史;③现病史:是否入院前3 d食欲或进食下降和糖尿病病程等;④实验室检验:糖化血红蛋白、入院血糖、白细胞计数、中性粒细胞计数、淋巴细胞计数、血小板总数、估算肾小球滤过率(estimated glomerular filtration rate,eGFR)、总胆红素、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、甘油三酯(triglyceride,TG)、胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)等、C-反应蛋白(c-reactive protein,CRP)、降钙素原(procalcitonin,PCT)等;⑤合并疾病:高血压、感染、动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)等;⑥治疗方案:SGLT2抑制剂种类、用法用量、用药疗程、是否院前调整降糖药以及联合其他降糖药情况等;⑦结局指标:是否出现euDKA:入院末梢或静脉血清葡萄糖<13.9 mmol/L、伴阴离子间隙升高的代谢性酸中毒(pH<7.3和血清碳酸氢盐<18 mEq/L)和酮症[7]。
-
运用SPSS 21.0软件进行统计学分析,对符合正态性检验的计量资料,用($ \overline{x} $±s)表示,两组比较采用独立样本t检验;对不符合正态性检验的计量资料,用中位数和四分位数间距表示,两组比较采用Man-Whitney U检验;计数资料用例数(百分比)表示,两组比较采用χ2检验。采用多因素Logistic回归分析SGLT2抑制剂相关euDKA的独立影响因素,并建立风险预测模型。根据受试者工作特征(receiver operating characteristic curve,ROC)曲线确定预测模型的曲线下面积(area under the curve,AUC)及临界值[8]。P<0.05表示差异有统计学意义。应用Python 3.8软件对模型样本进行十折交叉验证[9]。
-
119例患者中,男性68例(57.14%),女性51例(42.86%);平均年龄(57.31±12.28)岁;平均体质指数(24.39±2.95)kg/m2;达格列净11例(9.24%),恩格列净56例(47.06%),卡格列净52例(43.70%);所有患者均使用低剂量的SGLT2抑制剂(如达格列净5 mg/d、恩格列净10 mg/d、卡格列净100 mg/d)。
-
共纳入119例患者,其中21例(17.65%)发生euDKA。21例患者均表现为恶心、呕吐、腹泻等消化道症状,其中1例患者出现明显嗜睡。发生euDKA后,患者均立即停用口服降糖药,改用小剂量胰岛素降糖,并积极给予补液消酮、纠酸等对症措施。所有患者均好转后出院,出院后未再使用SGLT2抑制剂。
-
根据是否出现euDKA将119例患者分为非euDKA组98例和euDKA组21例。两组患者的年龄、吸烟史、DKA病史、用药期间手术史等23项临床资料比较,差异有统计学意义(P<0.05),见表1。
表 1 两组患者临床资料的单因素分析
项目 非euDKA组(n=98) euDKA组(n=21) u/χ2/t值 P值 年龄[岁,M(P25,P75)] 60.00(29.00,85.00) 50.00(24.00,75.00) −2.291 0.022 性别[男,n(%)] 52(53.06) 16(76.19) 3.778 0.052 体质指数(kg/m2,$ \overline{x} $±s) 24.62±2.87 23.30±3.12 1.873 0.064 吸烟史[n(%)] 21(21.43) 9(42.86) 4.212 0.040 酗酒史[n(%)] 7(7.14) 5(23.81) 3.619 0.057 DKA史[n(%)] 6(6.12) 5(23.81) 4.513 0.034 消化系统病史[n(%)] 42(42.86) 5(23.81) 2.626 0.105 用药期间手术史[n(%)] 52(53.06) 2(9.52) 13.225 <0.001 入院前3 d食欲或进食下降[n(%)] 4(4.08) 12(57.14) 37.405 <0.001 糖尿病病程 <1年[n(%)] 7(7.14) 1(4.76) <0.001 1.000 1~10年[n(%)] 39(39.80) 16(76.19) 9.216 0.002 >10年[n(%)] 52(53.06) 4(19.05) 8.031 0.005 糖化血红蛋白[%,M(P25,P75)] 7.95(5.40,13.40) 10.50(6.50,15.10) 3.319 0.001 入院血糖[mmol/L,M(P25,P75)] 8.22(3.01,29.20) 10.30(6.50,13.72) 2.523 0.012 白细胞计数[×109/L,M(P25,P75)] 6.68(2.78,14.46) 11.65(5.24,24.22) 4.186 <0.001 中性粒细胞计数[×109/L,M(P25,P75)] 3.55(1.79,12.89) 8.18(3.26,16.88) 5.507 <0.001 淋巴细胞计数(×109/L,$ \overline{x} $±s) 2.07±0.67 1.95±1.48 0.356 0.725 血小板总数[×109/L,M(P25,P75)] 231.50(101.00,358.00) 289.00(146.00,403.00) 2.558 0.011 eGFR[ml/(min·1.73m2),$ \overline{x} $±s] 95.41±32.31 106.68±35.47 −1.426 0.157 总胆红素(µmol/L,$ \overline{x} $±s) 11.51±5.50 13.41±11.70 −1.136 0.258 ALT(U/L,$ \overline{x} $±s) 29.59±40.99 23.93±19.51 0.617 0.539 AST(U/L,$ \overline{x} $±s) 22.01±17.87 21.09±9.87 0.230 0.818 TG(mmol/L,$ \overline{x} $±s) 3.61±14.42 3.10±3.32 0.161 0.872 TC(mmol/L,$ \overline{x} $±s) 4.39(2.33,8.94) 5.24(2.98,11.87) 3.004 0.003 HDL-C(mmol/L,$ \overline{x} $±s) 1.08±0.27 0.99±0.27 1.296 0.198 LDL-C(mmol/L,$ \overline{x} $±s) 2.46(0.85,5.66) 3.51(1.43,5.35) 3.067 0.002 CRP(mg/L,$ \overline{x} $±s) 2.31(0.07,341.00) 6.27(0.05,360.74) 2.938 0.003 PCT(ng/mL,$ \overline{x} $±s) 0.03(0.01,7.62) 0.06(0.01,12.15) 3.011 0.003 合并疾病 高血压[n(%)] 50(51.02) 3(14.29) 9.448 0.002 感染[n(%)] 17(17.35) 12(57.14) 14.860 <0.001 ASCVD[n(%)] 34(34.69) 7(33.33) 0.014 0.905 治疗方案 达格列净[n(%)] 6(6.12) 5(23.81) 4.513 0.034 恩格列净[n(%)] 46(46.94) 10(47.62) 0.003 0.955 卡格列净[n(%)] 46(46.94) 6(28.57) 2.371 0.124 用药疗程 <1月[n(%)] 16(16.33) 6(28.57) 1.004 0.316 1月~1年[n(%)] 54(55.10) 5(23.81) 6.774 0.009 >1年[n(%)] 28(28.57) 10(47.62) 2.887 0.089 院前调整降糖药 2(2.04) 7(33.33) 19.954 <0.001 联合其他降糖药情况 联合二甲双胍[n(%)] 64(65.31) 19(90.48) 5.193 0.023 联合磺脲类/非磺脲类 [n(%)] 38(38.78) 3(14.29) 4.593 0.032 联合α-糖苷酶抑制剂[n(%)] 44(44.90) 9(42.86) 0.029 0.864 联合噻唑烷二酮类[n(%)] 8(8.16) 4(19.05) 1.219 0.270 联合二肽基肽酶-4抑制剂[n(%)] 31(31.63) 5(23.81) 0.502 0.479 联合胰高血糖素样肽-1受体激动剂[n(%)] 7(7.14) 2(9.52) 0.140 0.708 联合胰岛素[n(%)] 34(34.69) 4(19.05) 1.948 0.163 注:DKA:糖尿病酮症酸中毒;eGFR:估算肾小球滤过率;ALT:丙氨酸氨基转移酶;AST:天门冬氨酸氨基转移酶;TG:甘油三酯;TC:胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;CRP:C-反应蛋白; PCT:降钙素原;ASCVD:动脉粥样硬化性心血管疾病。 -
以上述单因素分析中有统计学意义的变量作为自变量(二分类变量,否=0,是=1;糖尿病病程:<1年=0,1~10年=1,>10年=2;用药疗程:<1月=0,1月~1年=1,>1年=2;连续变量采用原数据),以患者是否出现euDKA为因变量(未出现=0,出现=1),进行多因素 Logistic回归分析。结果显示,DKA病史、入院前3 d食欲或进食下降、中性粒细胞计数升高、院前调整降糖药是增加SGLT2抑制剂相关euDKA风险的独立影响因素;而用药期间手术史是降低其风险的独立影响因素,见表2。
表 2 多因素logistic回归分析结果
项目 回归系数B 标准误S.E 卡方值Waldχ2 自由度df 比值比OR 95%CI置信区间 P值 DKA病史 4.738 2.017 5.515 1 114.153 2.189~5 952.744 0.019 用药期间手术史 −4.956 1.958 6.410 1 0.007 0.000~0.326 0.011 入院前3 d食欲或进食下降 3.081 1.262 5.957 1 21.774 1.834~258.463 0.015 中性粒细胞计数 0.721 0.202 12.678 1 2.056 1.383~3.058 <0.001 院前调整降糖药 3.823 1.483 6.649 1 45.745 2.502~836.278 0.010 常量 −6.575 1.564 17.666 1 0.001 / <0.001 -
以上述5个独立影响因素建立Logistic回归方程,Logit(P)= 4.738(DKA病史)−4.956(用药期间手术史)+3.081(入院前3 d食欲或进食下降)+0.721(中性粒细胞计数)+3.823(院前调整降糖药)−6.575,采用H-L法(Hosmerand Lemeshow test)对模型的拟合度进行检验,结果显示模型拟合良好(χ2值=3.557,P=0.895)。对上述回归方程转换后得出预测模型的计算公式=中性粒细胞计数+6.571(DKA病史)−6.874(用药期间手术史)+4.273(入院前3 d食欲或进食下降)+ 5.302(院前调整降糖药)。
-
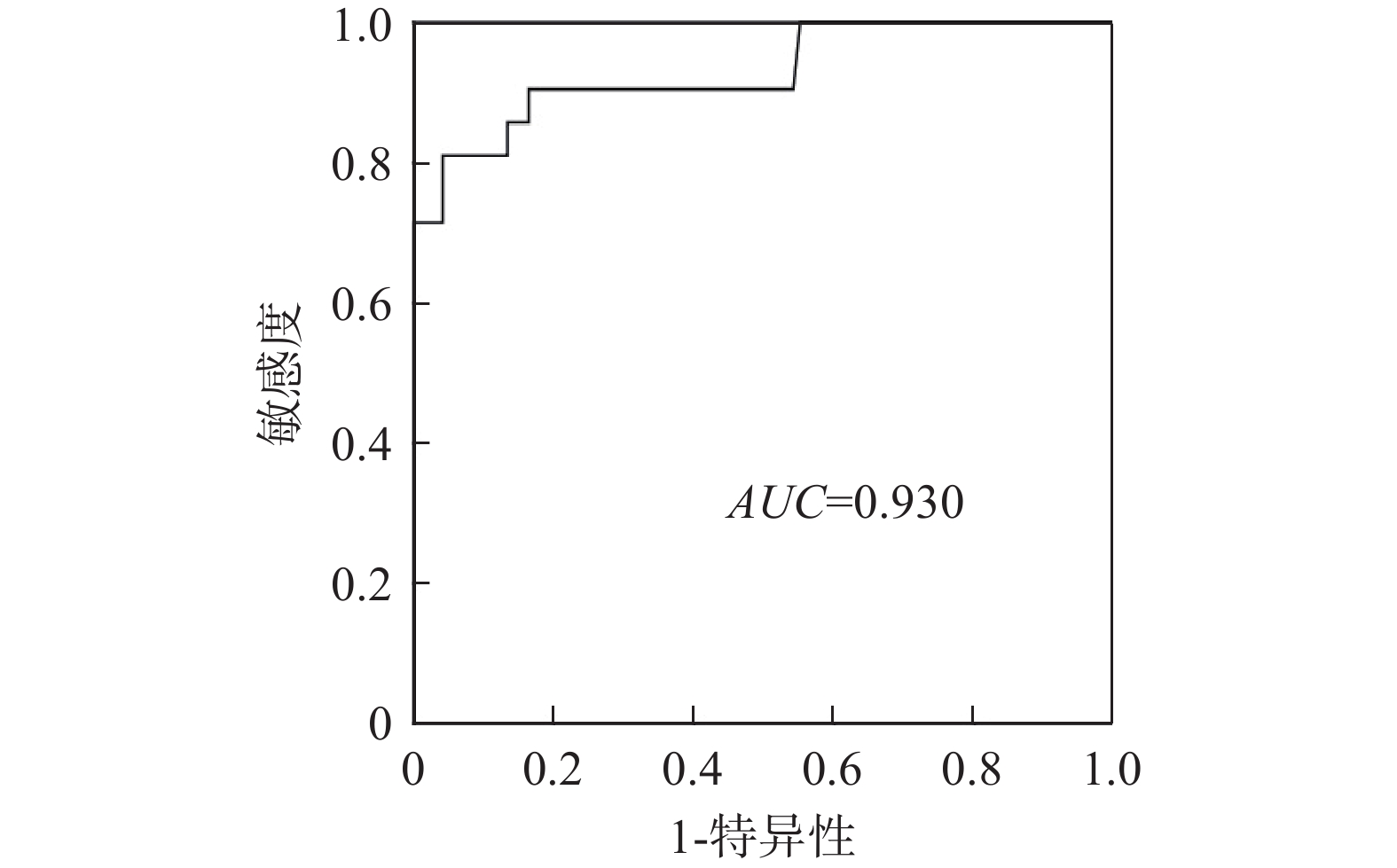
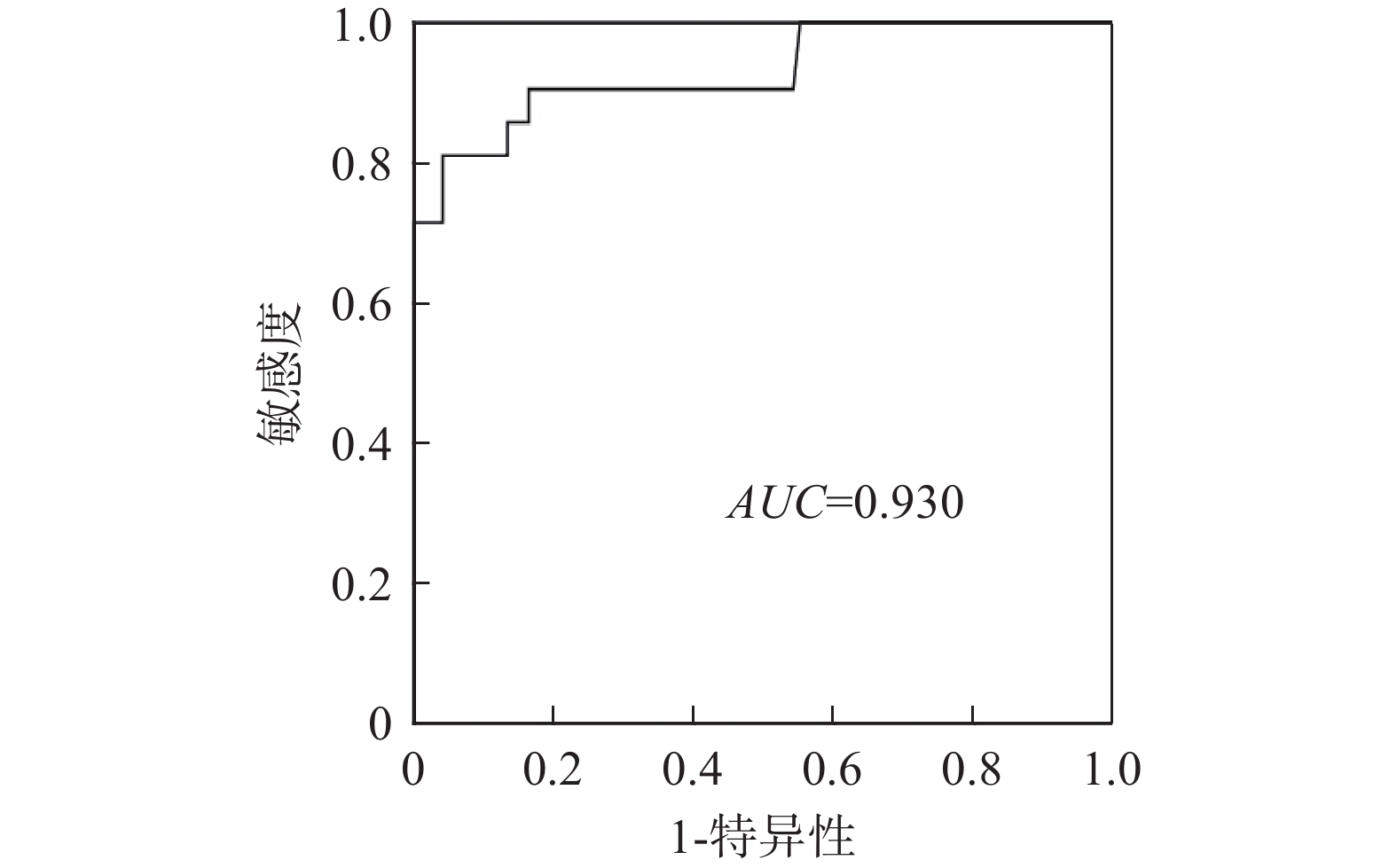
预测模型ROC曲线的AUC为0.982(P<0.001),准确率为94.96%,敏感度为0.905,特异性为0.959,临界值为7.405,见表3。模型十折交叉验证后预测模型ROC曲线的AUC为0.930,预测效果好,见图1。在预测模型外部验证的过程中,本研究选取2024年1月至12月期间符合纳排标准的34例住院患者作为验证集。将上述患者的中性粒细胞计数、DKA病史、用药期间手术史、入院前3 d食欲或进食下降、院前调整降糖药的数据代入计算公式中,得分高于7.405则表示存在euDKA高风险,并将预测结果与实际情况比较。结果显示,正确29例,假阴性3例,假阳性2例,模型预测的准确率为85.29%。
表 3 ROC曲线分析结果
项目 最佳临界值 敏感度 特异性 约登指数 AUC P 中性粒细胞计数 4.555 0.905 0.755 0.660 0.884(0.805~0.963) <0.001 DKA病史 0.500 0.238 0.939 0.177 0.588(0.443~0.734) 0.205 用药期间手术史 0.500 0.952 0.469 0.422 0.282(0.176~0.388) 0.002 入院前3 d食欲或进食下降 0.500 0.571 0.959 0.531 0.765(0.630~0.901) <0.001 院前调整降糖药 0.500 0.333 0.980 0.313 0.656(0.509~0.804) 0.025 预测模型 7.405 0.905 0.959 0.864 0.982(0.961~1.000) <0.001 -
euDKA是一种隐匿发病的糖尿病急症,特点是患者的血或尿酮体升高、碳酸氢盐降低伴阴离子间隙升高的代谢性酸中毒(pH<7.3),但血糖升高不明显,通常不超过13.9 mmol/L[10-11]。早在2015年,Hayami等[12]报道了全球首例由SGLT2抑制剂引起的euDKA。同年12月,美国FDA报告了73例患者服用SGLT2抑制剂后出现DKA,其中部分患者表现为euDKA[13]。由于euDKA易被漏诊,此前的研究中euDKA的比例较低,仅占所有DKA的2.6%~3.2%[14]。但随着SGLT2抑制剂临床应用增加,euDKA的发生率也有所增加。Goldenberg等[15]最新的研究发现,SGLT2抑制剂相关euDKA占所有DKA的比例高达70%,需格外重视。
SGLT2抑制剂诱发euDKA的可能机制主要包括:①促进尿糖排泄,降低血糖水平,一方面刺激胰高血糖素,增加糖异生,使代谢底物从碳水化合物转变为脂质[16];另一方面胰岛素分泌减少,对脂肪动员的抑制减弱,上述两方面均导致酮体生成增多[17];②抑制近端小管对钠和葡萄糖的重吸收,通过管球反馈降低肾脏对酮体的清除率[18];③利钠和渗透性利尿作用,造成血容量减少,激活下丘脑-垂体-肾上腺轴,分泌皮质醇和儿茶酚胺增多,加速脂肪动员,进一步增加酮体生成[19]。由此可见,SGLT2抑制剂可通过多种途径造成酮体在体内蓄积,引发酮症酸中毒。同时,SGLT2抑制剂促进尿糖排泄,导致机体出现血糖不高的酮症酸中毒状态,即euDKA。
有研究报道,SGLT2抑制剂相关euDKA的诱因包括合并急症(如感染、心肌梗死等)、手术、创伤、低血容量、饥饿或低碳水化合物饮食、胰岛素停用或减量以及饮酒等[20]。Bamgboye等[21]研究证实,感染如肺炎、胰腺炎、脓肿、败血症等均可引起euDKA。原因可能与感染导致碳水化合物的消耗减少,增加酮体生成有关[22]。中性粒细胞计数是临床上判断感染性疾病最常用的指标之一,其升高与炎性反应密切相关,细菌感染时更为明显[23]。本研究的结果同样得出,中性粒细胞计数升高的感染患者,SGLT2抑制剂相关euDKA的风险增加。
SGLT2抑制剂围术期用药的安全性,长期以来备受关注。Kameda等[24]研究发现,围术期患者使用SGLT2抑制剂易出现euDKA。Burke等[25]研究认为,约30%的患者术后服用SGLT2抑制剂可出现euDKA。患者术前常规禁食致血糖降低,胰岛素用量减少,术后应激又升高血糖,血糖调节失去平衡,促进脂肪氧化产生酮体,可能是围术期易出现SGLT2抑制剂相关euDKA的主要原因[26]。此前,美国内分泌协会曾建议择期手术患者术前1~3 d停用SGLT2抑制剂[27]。本研究结果显示,既往存在SGLT2抑制剂用药期间手术史的患者相比未行手术的患者出现euDKA的风险降低。因此,对于SGLT2抑制剂用药期间首次进行手术的患者,需特别警惕其euDKA的风险,应考虑术前1~3 d停止用药以降低该风险。
另外,与此前的报道相同的是,入院前3 d食欲或进食下降和院前调整降糖药也是SGLT2抑制剂相关euDKA的影响因素。减肥、限制饮食(尤其是生酮饮食)均会导致脂肪分解增加,酮体生成增多,出现euDKA的风险增高[11]。院前调整降糖药(尤其是胰岛素减量或停药)可能导致胰岛素相对缺乏,同样也会刺激脂肪组织动员,产生酮体[28]。除此之外,本研究还发现既往有DKA病史的患者出现SGLT2抑制剂相关euDKA的风险更高,可能与该类患者长期饮食不规律、用药依从性不高、不良生活习惯较多等有关。
综上所述,本研究结果显示DKA病史、入院前3 d食欲或进食下降、中性粒细胞计数升高和院前调整降糖药是增加SGLT2抑制剂相关euDKA风险的影响因素;用药期间手术史是降低该风险的影响因素。联合上述影响因素构建的预测模型对SGLT2抑制剂相关euDKA风险具有较好的预测价值,为早期预防和诊治提供了决策依据。
Risk factors analysis and prediction model construction of SGLT2 inhibitor-associated euglycemic diabetic ketoacidosis
-
摘要:
目的 探讨钠-葡萄糖协同转运蛋白2(sodium-dependent glucose transporters 2,SGLT2)抑制剂相关非高血糖性酮症酸中毒(euDKA)的影响因素,并建立风险预测模型。 方法 回顾性分析2020年1月至2023年12月厦门大学附属东南医院收治的接受SGLT2抑制剂治疗的2型糖尿病患者的临床资料,包括年龄、性别、糖尿病病程等,采用单因素分析和多因素Logistic回归分析SGLT2抑制剂相关euDKA的影响因素,并建立预测模型。根据受试者工作特征(ROC)曲线确定预测模型的曲线下面积(AUC)及最佳临界值。并对预测模型进行内外部验证。 结果 本研究共纳入119例接受SGLT2抑制剂治疗的2型糖尿病患者,其中未出现euDKA共98例(非euDKA组),出现euDKA共21例(euDKA组)。多因素Logistic回归分析显示,DKA病史、入院前3 d食欲或进食下降、中性粒细胞计数升高和院前调整降糖药是增加SGLT2抑制剂相关euDKA风险的独立影响因素(OR=114.153,21.774,2.056,45.745,P<0.05);用药期间手术史是降低该风险的独立影响因素(OR=0.007,P<0.05)。通过建立预测模型的计算公式=中性粒细胞计数+6.571(DKA病史)-6.874(用药期间手术史)+4.273(入院前3 d食欲或进食下降)+5.302(院前调整降糖药),绘制ROC曲线。预测模型的ROC曲线下面积(AUC)为0.982(95%CI:0.961~1.000,P<0.001),准确率为94.96%,敏感度为0.905,特异度为0.959,临界值为7.405。模型十折交叉验证后ROC曲线AUC为0.930。另外,预测模型外部验证的准确率为85.29%。 结论 DKA病史、入院前3 d食欲或进食下降、中性粒细胞计数升高和院前调整降糖药增加SGLT2抑制剂相关euDKA的风险,用药期间手术史降低该风险。据此建立的预测模型对SGLT2抑制剂相关euDKA的风险具有良好的预测价值。 -
关键词:
- 钠-葡萄糖协同转运蛋白2 /
- SGLT2抑制剂 /
- 非高血糖性酮症酸中毒 /
- 2型糖尿病 /
- 预测模型
Abstract:Objective To explore risk factors of sodium-dependent glucose transporters 2 (SGLT2) inhibitor-associated euglycemic diabetic ketoacidosis and to construct a risk prediction model. Methods A retrospective analysis was performed on the clinical data of type 2 diabetes patients treated with SGLT2 inhibitors in Dongnan Hospital of Xiamen University from January 2020 to December 2023, including age, gender and course of diabetes. The risk factors of SGLT2 inhibitor-associated euDKA were analyzed by univariate analysis and multivariate Logistic regression, and a prediction model was established. According to the receiver's operating characteristic (ROC) curve, the area under the curve (AUC) and the optimal critical value of the prediction model were determined. The prediction model was subjected to both internal and external validation. Results A total of 119 patients with type 2 diabetes treated with SGLT2 inhibitors were included in this study. Among them, there were 98 cases without euDKA (non-euDKA group)and 21 cases with euDKA (euDKA group). Multivariate Logistic regression analysis showed the DKA history, appetite or diet decreased three days before admission, elevated neutrophil count and pre-hospital adjustment of hypoglycemic agents were independent factors to increase risks of euDKA associated with SGLT2 inhibitors (OR=114.153, 21.774, 2.056, 45.745, P<0.05). Operation history during medication was an independent factor to reduce this risk (OR=0.007, P<0.05). By establishing the calculation formula of the prediction model = neutrophil count+6.571 (DKA history)−6.874 (operation history during medication)+4.273 (appetite or diet decreased three days before admission)+5.302 (pre-hospital adjustment of hypoglycemic drugs), the ROC curve was drawn. The area under the curve (AUC) of the ROC of the prediction model was 0.982 (95% CI: 0.961-1.000, P<0.001), with accuracy of 94.96%, sensitivity of 0.905, specificity of 0.959 and a critical value of 7.405. The AUC of ROC curve after the model’s ten-fold cross validation was 0.930. And the accuracy of the external validation of the prediction model was 85.29%. Conclusion The DKA history, appetite or diet decreased three days before admission, elevated neutrophil count and pre-hospital adjustment of hypoglycemic agents increased the risk of SGLT2 inhibitor-associated euDKA, while the operation history during medication reduced this risk. The risk prediction model constructed on this basis could better predict the risk of SGLT2 inhibitor-associated euDKA. -
表 1 两组患者临床资料的单因素分析
项目 非euDKA组(n=98) euDKA组(n=21) u/χ2/t值 P值 年龄[岁,M(P25,P75)] 60.00(29.00,85.00) 50.00(24.00,75.00) −2.291 0.022 性别[男,n(%)] 52(53.06) 16(76.19) 3.778 0.052 体质指数(kg/m2,$ \overline{x} $±s) 24.62±2.87 23.30±3.12 1.873 0.064 吸烟史[n(%)] 21(21.43) 9(42.86) 4.212 0.040 酗酒史[n(%)] 7(7.14) 5(23.81) 3.619 0.057 DKA史[n(%)] 6(6.12) 5(23.81) 4.513 0.034 消化系统病史[n(%)] 42(42.86) 5(23.81) 2.626 0.105 用药期间手术史[n(%)] 52(53.06) 2(9.52) 13.225 <0.001 入院前3 d食欲或进食下降[n(%)] 4(4.08) 12(57.14) 37.405 <0.001 糖尿病病程 <1年[n(%)] 7(7.14) 1(4.76) <0.001 1.000 1~10年[n(%)] 39(39.80) 16(76.19) 9.216 0.002 >10年[n(%)] 52(53.06) 4(19.05) 8.031 0.005 糖化血红蛋白[%,M(P25,P75)] 7.95(5.40,13.40) 10.50(6.50,15.10) 3.319 0.001 入院血糖[mmol/L,M(P25,P75)] 8.22(3.01,29.20) 10.30(6.50,13.72) 2.523 0.012 白细胞计数[×109/L,M(P25,P75)] 6.68(2.78,14.46) 11.65(5.24,24.22) 4.186 <0.001 中性粒细胞计数[×109/L,M(P25,P75)] 3.55(1.79,12.89) 8.18(3.26,16.88) 5.507 <0.001 淋巴细胞计数(×109/L,$ \overline{x} $±s) 2.07±0.67 1.95±1.48 0.356 0.725 血小板总数[×109/L,M(P25,P75)] 231.50(101.00,358.00) 289.00(146.00,403.00) 2.558 0.011 eGFR[ml/(min·1.73m2),$ \overline{x} $±s] 95.41±32.31 106.68±35.47 −1.426 0.157 总胆红素(µmol/L,$ \overline{x} $±s) 11.51±5.50 13.41±11.70 −1.136 0.258 ALT(U/L,$ \overline{x} $±s) 29.59±40.99 23.93±19.51 0.617 0.539 AST(U/L,$ \overline{x} $±s) 22.01±17.87 21.09±9.87 0.230 0.818 TG(mmol/L,$ \overline{x} $±s) 3.61±14.42 3.10±3.32 0.161 0.872 TC(mmol/L,$ \overline{x} $±s) 4.39(2.33,8.94) 5.24(2.98,11.87) 3.004 0.003 HDL-C(mmol/L,$ \overline{x} $±s) 1.08±0.27 0.99±0.27 1.296 0.198 LDL-C(mmol/L,$ \overline{x} $±s) 2.46(0.85,5.66) 3.51(1.43,5.35) 3.067 0.002 CRP(mg/L,$ \overline{x} $±s) 2.31(0.07,341.00) 6.27(0.05,360.74) 2.938 0.003 PCT(ng/mL,$ \overline{x} $±s) 0.03(0.01,7.62) 0.06(0.01,12.15) 3.011 0.003 合并疾病 高血压[n(%)] 50(51.02) 3(14.29) 9.448 0.002 感染[n(%)] 17(17.35) 12(57.14) 14.860 <0.001 ASCVD[n(%)] 34(34.69) 7(33.33) 0.014 0.905 治疗方案 达格列净[n(%)] 6(6.12) 5(23.81) 4.513 0.034 恩格列净[n(%)] 46(46.94) 10(47.62) 0.003 0.955 卡格列净[n(%)] 46(46.94) 6(28.57) 2.371 0.124 用药疗程 <1月[n(%)] 16(16.33) 6(28.57) 1.004 0.316 1月~1年[n(%)] 54(55.10) 5(23.81) 6.774 0.009 >1年[n(%)] 28(28.57) 10(47.62) 2.887 0.089 院前调整降糖药 2(2.04) 7(33.33) 19.954 <0.001 联合其他降糖药情况 联合二甲双胍[n(%)] 64(65.31) 19(90.48) 5.193 0.023 联合磺脲类/非磺脲类 [n(%)] 38(38.78) 3(14.29) 4.593 0.032 联合α-糖苷酶抑制剂[n(%)] 44(44.90) 9(42.86) 0.029 0.864 联合噻唑烷二酮类[n(%)] 8(8.16) 4(19.05) 1.219 0.270 联合二肽基肽酶-4抑制剂[n(%)] 31(31.63) 5(23.81) 0.502 0.479 联合胰高血糖素样肽-1受体激动剂[n(%)] 7(7.14) 2(9.52) 0.140 0.708 联合胰岛素[n(%)] 34(34.69) 4(19.05) 1.948 0.163 注:DKA:糖尿病酮症酸中毒;eGFR:估算肾小球滤过率;ALT:丙氨酸氨基转移酶;AST:天门冬氨酸氨基转移酶;TG:甘油三酯;TC:胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;CRP:C-反应蛋白; PCT:降钙素原;ASCVD:动脉粥样硬化性心血管疾病。 表 2 多因素logistic回归分析结果
项目 回归系数B 标准误S.E 卡方值Waldχ2 自由度df 比值比OR 95%CI置信区间 P值 DKA病史 4.738 2.017 5.515 1 114.153 2.189~5 952.744 0.019 用药期间手术史 −4.956 1.958 6.410 1 0.007 0.000~0.326 0.011 入院前3 d食欲或进食下降 3.081 1.262 5.957 1 21.774 1.834~258.463 0.015 中性粒细胞计数 0.721 0.202 12.678 1 2.056 1.383~3.058 <0.001 院前调整降糖药 3.823 1.483 6.649 1 45.745 2.502~836.278 0.010 常量 −6.575 1.564 17.666 1 0.001 / <0.001 表 3 ROC曲线分析结果
项目 最佳临界值 敏感度 特异性 约登指数 AUC P 中性粒细胞计数 4.555 0.905 0.755 0.660 0.884(0.805~0.963) <0.001 DKA病史 0.500 0.238 0.939 0.177 0.588(0.443~0.734) 0.205 用药期间手术史 0.500 0.952 0.469 0.422 0.282(0.176~0.388) 0.002 入院前3 d食欲或进食下降 0.500 0.571 0.959 0.531 0.765(0.630~0.901) <0.001 院前调整降糖药 0.500 0.333 0.980 0.313 0.656(0.509~0.804) 0.025 预测模型 7.405 0.905 0.959 0.864 0.982(0.961~1.000) <0.001 -
[1] MCGUIRE D K, SHIH W J, COSENTINO F, et al. Association of SGLT2 inhibitors with cardiovascular and kidney outcomes in patients with type 2 diabetes: a meta-analysis[J]. JAMA Cardiol, 2021, 6(2): 148-158. doi: 10.1001/jamacardio.2020.4511 [2] CAPARROTTA T M, GREENHALGH A M, OSINSKI K, et al. Sodium–glucose co-Transporter2 inhibitors(SGLT2i)exposure and outcomes in Type2 diabetes: a systematic review of population-based observational studies[J]. Diabetes Ther, 2021, 12(4): 991-1028. [3] BLAU J E, TELLA S H, TAYLOR S I, et al. Ketoacidosis associated with SGLT2 inhibitor treatment: analysis of FAERS data[J]. Diabetes Metab Res Rev, 2017, 33(8): e2924. [4] EVANS K. Diabetic ketoacidosis: update on management[J]. Clin Med, 2019, 19(5): 396-398. doi: 10.7861/clinmed.2019-0284 [5] 纪立伟. 关注钠-葡萄糖转运蛋白2抑制剂引起的非高血糖性酮症酸中毒[J]. 药物不良反应杂志, 2021, 23(6): 281-284. doi: 10.3760/cma.j.cn114015-20210515-00575 [6] 中华医学会糖尿病学分会, 朱大龙. 中国2型糖尿病防治指南(2020年版)[J]. 中华糖尿病杂志, 2021, 13(4): 315-409. [7] DANNE T, GARG S, PETERS A L, et al. International consensus on risk management of diabetic ketoacidosis in patients with type 1 diabetes treated with sodium-glucose cotransporter (SGLT) inhibitors[J]. Diabetes Care, 2019, 42(6): 1147-1154. doi: 10.2337/dc18-2316 [8] COLLINS G S, REITSMA J B, ALTMAN D G, et al. Transparent reporting of a multivariable prediction model for individual prognosis or diagnosis (TRIPOD): the TRIPOD statement[J]. BMJ, 2015, 350: g7594. doi: 10.7326/l15-0078-4 [9] 贺彩红, 刘金武, 朱照贺, 等. 联合预测因子对急性心肌梗死患者院内并发1型心肾综合征风险的预测价值[J]. 中华心血管病杂志, 2021, 49(8): 802-808. [10] MEYER E J, GABB G, JESUDASON D. SGLT2 inhibitor-associated euglycemic diabetic ketoacidosis: a south Australian clinical case series and Australian spontaneous adverse event notifications[J]. Diabetes Care, 2018, 41(4): e47-e49. doi: 10.2337/dc17-1721 [11] SAMPANI E, SARAFIDIS P, PAPAGIANNI A. Euglycaemic diabetic ketoacidosis as a complication of SGLT-2 inhibitors: epidemiology, pathophysiology, and treatment[J]. Expert Opin Drug Saf, 2020, 19(6): 673-682. doi: 10.1080/14740338.2020.1764532 [12] HAYAMI T, KATO Y, KAMIYA H, et al. Case of ketoacidosis by a sodium-glucose cotransporter 2 inhibitor in a diabetic patient with a low-carbohydrate diet[J]. J Diabetes Investig, 2015, 6(5): 587-590. [13] U. S. Food and Drug Administration. FDA revises labels of SGLT2 inhibitors for diabetes to include warnings about too much acid in the blood and serious urinary tract infections[EB/OL].(2015-04-12)[2024-03-20]. https://www.fda.gov/drugs/drug-safety-and-availability/fda-revises-labels-sglt2-inhibitors-diabetes-include-warnings-about-too-much-acid-blood-and-serious. [14] YU X F, ZHANG S F, ZHANG L. Newer perspectives of mechanisms for euglycemic diabetic ketoacidosis[J]. Int J Endocrinol, 2018, 2018: 7074868. doi: 10.1155/2018/7074868 [15] ATA F, YOUSAF Z, KHAN A A, et al. SGLT-2 inhibitors associated euglycemic and hyperglycemic DKA in a multicentric cohort[J]. Sci Rep, 2021, 11(1): 10293. doi: 10.1038/s41598-021-89752-w [16] VALLON V. The mechanisms and therapeutic potential of SGLT2 inhibitors in diabetes mellitus[J]. Annu Rev Med, 2015, 66: 255-270. doi: 10.1146/annurev-med-051013-110046 [17] FERRANNINI E, BALDI S, FRASCERRA S, et al. Shift to fatty substrate utilization in response to sodium-glucose cotransporter 2 inhibition in subjects without diabetes and patients with type 2 diabetes[J]. Diabetes, 2016, 65(5): 1190-1195. doi: 10.2337/db15-1356 [18] LI N, ZHOU G W, ZHENG Y W, et al. Effects of SGLT2 inhibitors on cardiovascular outcomes in patients with stage 3/4 CKD: a meta-analysis[J]. PLoS One, 2022, 17(1): e0261986. doi: 10.1371/journal.pone.0261986 [19] PERRY R J, RABIN-COURT A, SONG J D, et al. Dehydration and insulinopenia are necessary and sufficient for euglycemic ketoacidosis in SGLT2 inhibitor-treated rats[J]. Nat Commun, 2019, 10(1): 548. doi: 10.1038/s41467-019-08466-w [20] GOLDENBERG R M, BERARD L D, CHENG A Y Y, et al. SGLT2 inhibitor-associated diabetic ketoacidosis: clinical review and recommendations for prevention and diagnosis[J]. Clin Ther, 2016, 38(12): 2654-2664. e1. [21] BAMGBOYE A O, ONI I O, COLLIER A. Predisposing factors for the development of diabetic ketoacidosis with lower than anticipated glucose levels in type 2 diabetes patients on SGLT2-inhibitors: a review[J]. Eur J Clin Pharmacol, 2021, 77(5): 651-657. doi: 10.1007/s00228-020-03051-3 [22] QIU H Y, NOVIKOV A, VALLON V. Ketosis and diabetic ketoacidosis in response to SGLT2 inhibitors: Basic mechanisms and therapeutic perspectives[J]. Diabetes Metab Res Rev, 2017, 33(5). [23] 夏凌志, 李鹤. 血清降钙素原、C反应蛋白及中性粒细胞计数联合检测在儿童感染性肺炎中的应用评价[J]. 现代医药卫生, 2017, 33(22): 3460-3462. doi: 10.3969/j.issn.1009-5519.2017.22.033 [24] KAMEDA Y, KATO M, INOUE B, et al. Euglycemic diabetic ketoacidosis caused by a sodium-glucose co-transporter(SGLT)2 inhibitor after coronary artery bypass grafting[J]. Kyobu Geka, 2019, 72(5): 354-357. doi: 10.1016/s0735-1097(19)33029-3 [25] BURKE K R, SCHUMACHER C A, HARPE S E. SGLT2 inhibitors: a systematic review of diabetic ketoacidosis and related risk factors in the primary literature[J]. Pharmacotherapy, 2017, 37(2): 187-194. doi: 10.1002/phar.1881 [26] PACE D J, DUKLESKA K, PHILLIPS S, et al. Euglycemic diabetic ketoacidosis due to sodium-glucose cotransporter 2 inhibitor use in two patients undergoing pancreatectomy[J]. J Pancreat Cancer, 2018, 4(1): 95-99. doi: 10.1089/pancan.2018.0016 [27] HANDELSMAN Y, HENRY R R, BLOOMGARDEN Z T, et al. American association of clinical endocrinologists and American college of endocrinology position statement on the association of sglt-2 inhibitors and diabetic ketoacidosis[J]. Endocr Pract, 2016, 22(6): 753762. doi: 10.4158/ep161292.ps [28] LARROUMET A, CAMOIN M, FOUSSARD N, et al. Euglycemic ketoacidosis induced by therapeutic fasting in a non-diabetic patient[J]. Nutrition, 2020, 72: 110668. doi: 10.1016/j.nut.2019.110668 -




 下载:
下载: