-
真菌感染是威胁人类健康的重要公共卫生问题,全球每年感染真菌的患者超过10亿,导致死亡约250万[1]。危及生命的真菌感染一般是侵袭性真菌感染,常累及肺、肾和脑等,尤其在免疫功能低下者中更为常见,药物治疗仍然是当前临床抗真菌治疗的主要手段。
目前临床常见的抗真菌药物主要包括唑类、棘白菌素类、多烯类和核苷类等。唑类药物包括氟康唑(fluconazole)、伊曲康唑(itraconazole)和伏立康唑(voriconazole)等,随着以氟康唑为代表的唑类抗真菌药物在临床上的长期、广泛使用,真菌对该类药物的耐药性问题日益突出。棘白菌素类药物包括卡泊芬净(caspofungin)和米卡芬净(micafungin)等,对多数念珠菌属有杀菌作用,对曲霉菌属具有抑菌作用[2],具有良好的安全性,且与其他抗真菌药物之间无交叉耐药,但由于抗真菌谱较窄且价格昂贵,其临床应用受到了一定限制。多烯类药物以两性霉素B(amphotericin B)为代表,两性霉素B虽然疗效好并且具有广谱抗真菌活性,但是毒性问题限制了其临床应用[2]。核苷类的主要代表药物是5-氟胞嘧啶(5-fluorocytosine),其耐药问题普遍存在,所以5-氟胞嘧啶通常与其他抗真菌药物联合使用。
随着有限的抗真菌药物的广泛应用,真菌已快速进化出高适应性,通常表现为耐药性、耐受性和持留性。临床应用中最重要、最常用的抗真菌药物是唑类、棘白菌素类和多烯类。本文从耐药性、耐受性和持留性3方面重点综述病原真菌对这3类药物的高适应性机制,并探讨联合用药、新型抗真菌药物研发等应对策略。
-
耐药性是指真菌通过基因突变、表达调控改变等遗传机制,使药物对其最低抑菌浓度(minimum inhibitory concentration,MIC)升高至常规抑制浓度以上、导致抗真菌药物无法有效抑制其生长的现象。耐药性的产生与治疗持续时间无关。耐药基因可稳定遗传,并能用MIC量化评估耐药程度[3]。病原真菌耐药性问题,尤其是多药耐药(multiple drug resistance,MDR)现象的出现,增加了真菌感染疾病的治疗难度。
-
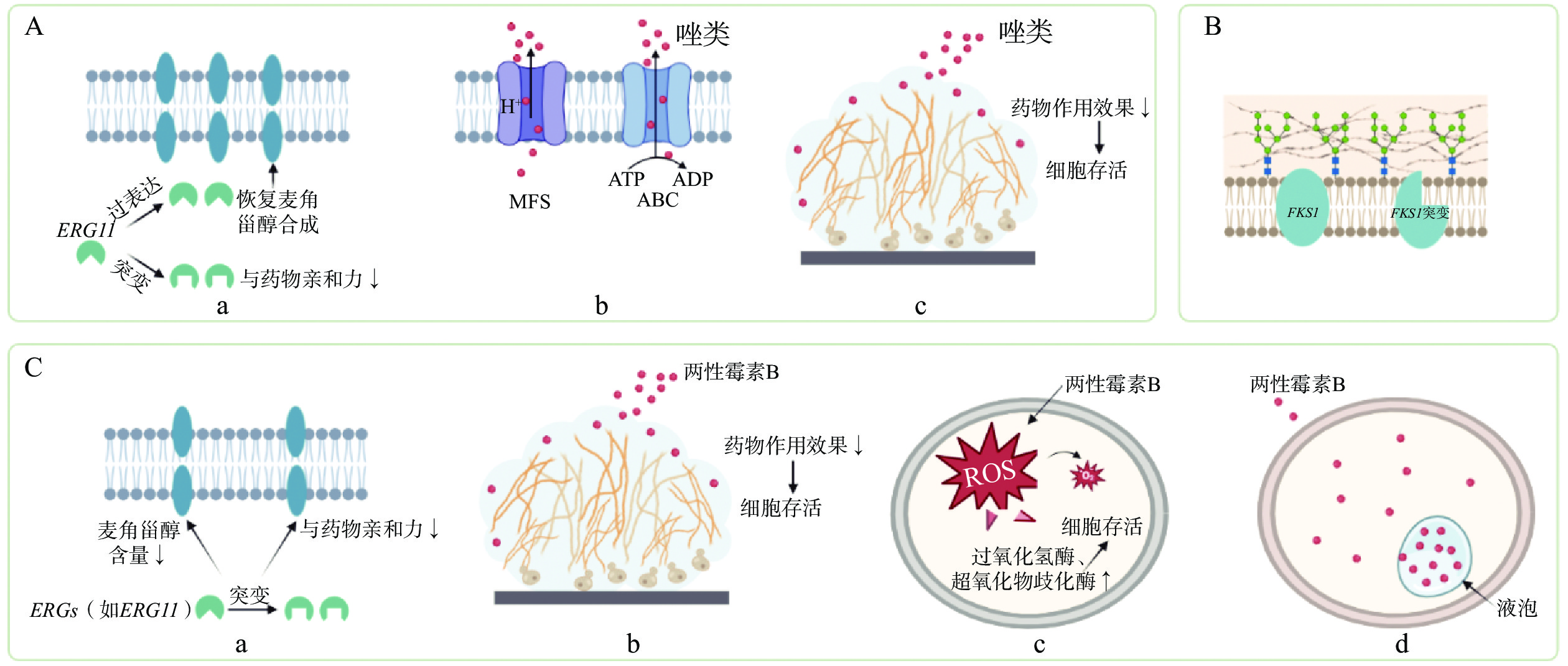
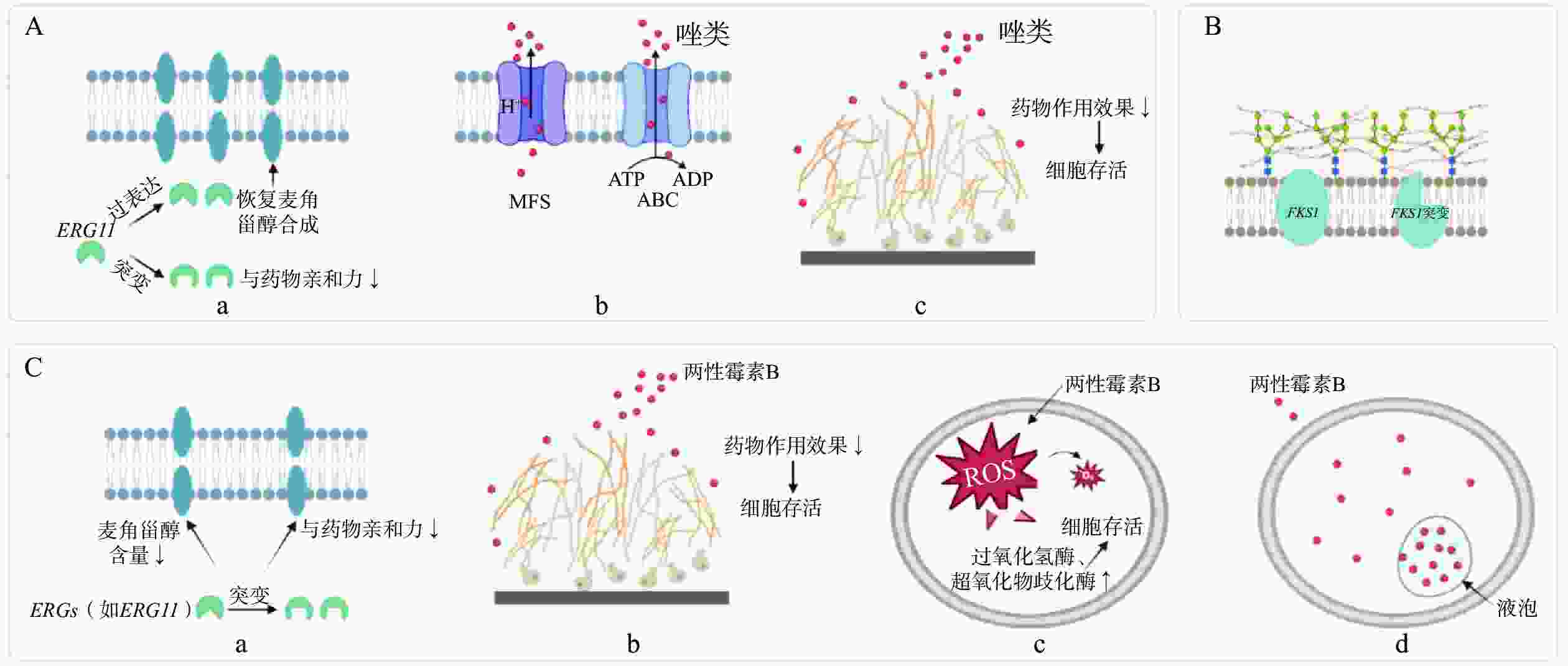
唑类抗真菌药物的主要作用靶点是ERG11基因编码的14α-去甲基化酶(CYP51),该酶是麦角甾醇生物合成途径中的关键酶。唑类药物通过抑制CYP51活性,阻断麦角甾醇合成,导致真菌细胞膜结构和功能受损,从而抑制真菌生长。真菌可以通过ERG11突变等方式改变药物靶点结构,从而降低药物与靶点的结合力,导致耐药性出现(见图1Aa)。
ERG11基因突变是多种念珠菌和隐球菌对唑类抗真菌药物耐药的主要机制之一。Y132F位点突变在白念珠菌、热带念珠菌和近平滑念珠菌中广泛发现,已证实其与唑类药物的耐药性密切相关。该突变通过改变ERG11蛋白空间构象,直接削弱唑类药物与靶酶的结合力,使真菌在药物存在下仍能合成细胞膜必需的麦角甾醇[4]。一项对近4 000个14α-去甲基化酶氨基酸变异的深度筛选研究发现,约33%的变异可导致耐药表型,其中高达88%表现为对多种唑类药物的交叉耐药[5]。此外,ERG11突变位点在耐药菌株中频繁出现,可以作为预测唑类耐药的标志,如Y132F突变可用于追踪耐药基因型[6]。需要注意的是,并非所有ERG11突变均具有功能性或足以引起显著的表型耐药[6],其耐药性可能依赖于其他机制(如药物外排泵)协同发挥作用。
-
除靶点自身发生结构或功能改变外,病原真菌还可通过上调靶点表达水平、扩增靶点编码基因等途径增加靶点的绝对数量,从而降低单位靶点所接触的药物浓度,进而削弱药物的抑制或杀伤效应。ERG11过表达导致唑类药物的靶酶显著增加,常规浓度的唑类药物无法完全抑制酶活性,从而导致耐药性的产生(见图1Aa)。研究表明,在白念珠菌中,ERG11基因过表达与唑类(尤其是氟康唑)耐药性直接相关;在氟康唑耐药株中,ERG11表达显著上调,其表达水平与耐药性呈正相关[7]。在白念珠菌中,ERG11的过表达通常与转录因子Upc2的功能获得性突变有关,这些突变会增强ERG11的表达,从而提高耐药性。在热带念珠菌中,ERG11过表达直接与氟康唑抗性相关。在一项研究中,所有8株氟康唑耐药菌株均表现为ERG11过表达,且多数同时伴随ERG3的过表达[8]。研究表明,CDR1和ERG11基因的过表达是氟康唑耐药光滑念珠菌的普遍特征,在所有受试分离株中均有发现[9]。
-
外排泵基因表达上调是念珠菌产生耐药的重要机制之一,它们通过主动将药物转运出细胞,降低胞内药物浓度,使唑类药物在细胞内难以达到抑菌浓度(见图1Ab)。目前已知白念珠菌中与耐药相关的外排泵主要分为ATP结合盒家族(ATP-binding cassette transporters superfamily,ABC)和主要易化超家族(major facilitator superfamily,MFS)两大类。在ABC家族中,CDR1/CDR2的表达受CDR基因转录激活因子1(transcription activator of CDR genes,Tac1p)调控,当Tac1p发生功能获得性突变时,CDR1和CDR2即可持续高表达,增强唑类药物外排,显著降低胞内氟康唑的累积。
在光滑念珠菌中,ABC转运蛋白中的药物外排泵蛋白1(Candida drug-resistance protein 1,Cdr1p)是介导唑类耐药的核心外排泵,其过表达可显著增强氟康唑等药物外排。Cdr1p的表达受转录因子Pdr1调控,Pdr1的功能获得性突变会过度激活外排泵基因的转录,从而导致耐药性增强[10]。Pdr1通过结合外排泵基因启动子区,并与Mediator复合物亚基Med15a的KIX结构域相互作用,激活外排泵基因的表达,是光滑念珠菌多药耐药通路的关键枢纽[11]。耳念珠菌耐药株中同时检测到CDR1、MDR1过表达及ERG11突变,多种耐药机制协同导致耳念珠菌对氟康唑的高度耐药性。此外,部分菌株还通过改变细胞膜脂质组成(如降低麦角甾醇含量)增强外排泵功能,从而减少药物累积[12]。
-
生物被膜亦是介导唑类药物耐药性的重要机制之一。生物被膜是由多层真菌细胞及其分泌的细胞外聚合物(如多糖、蛋白质等)构成的复合体结构,当其在医疗器械表面或宿主黏膜组织定植形成后,可使菌株对唑类药物产生显著耐药性。此类耐药性主要源于致密细胞外基质所形成的物理屏障,该屏障不仅能有效结合药物分子,还可阻碍药物的扩散渗透,从而大幅限制唑类药物抵达生物被膜深层发挥作用[13](见图1Ac)。最终,被包裹于被膜内部的真菌细胞因无法接触到有效抑菌浓度的药物而得以存活,其生存繁殖能力显著增强,进而直接导致临床抗真菌治疗失败。
-
棘白菌素类药物通过抑制β-1,3-葡聚糖合成破坏细胞壁的完整性而发挥抗真菌作用,是治疗念珠菌感染的一线药物。有研究发现,FKS1基因特定区域(如HS1和HS2)的点突变会导致β-1,3-葡聚糖合成酶构象改变,降低药物结合能力,从而产生耐药性(见图1B)。在光滑念珠菌中,FKS突变率高,易对棘白菌素和唑类产生交叉耐药,且常伴随MDR现象,FKS1和FKS2的任一热点突变都可能导致治疗失败[14]。同样,对棘白菌素固有耐药的近平滑念珠菌,其FKS1蛋白中丙氨酸替代脯氨酸的突变会进一步增加耐药性[15]。在耳念珠菌中,FKS1突变使2%~10%的菌株对棘白菌素产生耐药,这些菌株对唑类的耐药和对两性霉素B的耐药共存[16]。希木龙念珠菌耐药株Ch4’r在FKS1的HS2区域发生G4061A突变,也会引发对棘白菌素和其他抗真菌药物的交叉耐药[17]。
-
多烯类药物通过与真菌细胞膜中的麦角甾醇结合,形成跨膜孔隙,破坏膜完整性并导致细胞内容物泄漏,最终导致死亡。该类药物具有广谱抗真菌活性,虽耐药性相对少见,但耐药菌的报道正逐渐增多。在免疫功能缺陷人群中,耐药现象更常见,常伴随交叉耐药或MDR。其耐药机制主要包括以下几方面:①真菌可通过改变麦角甾醇的含量或分布来干扰孔隙形成,例如白念珠菌暴露于药物后即可出现此类变化,从而降低药物效力(见图1Ca);②生物被膜的形成可阻碍药物渗透,减少药物与作用靶点的接触机会,进而显著削弱多烯类抗真菌药物的治疗效果(见图1Cb);③氧化应激反应亦是介导多烯类药物耐药性产生的重要机制之一。以两性霉素B为例,该药物可通过破坏真菌细胞膜的完整性诱导活性氧(reactive oxygen species, ROS)大量累积,进而对真菌细胞造成氧化损伤;而耐药菌株则能通过激活过氧化氢酶、超氧化物歧化酶等抗氧化酶及下游相关信号通路,高效清除胞内ROS,从而维持自身存活并逃避药物杀伤[18](见图1Cc)。尤其值得关注的是,液泡隔离机制在多烯类药物耐药性的形成中扮演着关键角色。耐药菌株可通过这一途径将多烯类药物转运至液泡内,从而显著降低细胞质中药物的有效作用浓度(见图1Cd)。研究人员借助活细胞成像技术对多种高度耐药菌株展开观测。结果发现,3种具有不同结构的多烯类荧光探针均呈现出一致的特征:其在液泡腔内的累积水平显著升高。这一发现证实,液泡隔离是病原真菌应对多烯类药物的一种普遍且保守的耐药策略[19]。
-
耐受性是指整个真菌群体中的一部分亚群,在不改变MIC的情况下,通过多种可逆的生理适应机制,暂时存活于高浓度药物中,延缓被杀伤并维持缓慢生长的能力[20]。与耐药性不同,耐受性不涉及基因突变或药物靶点的永久性改变,而是真菌通过改变代谢途径或生化过程所产生的对药物的适应性改变[21]。在同一基因背景的菌群中,随机的基因表达波动、微环境差异等因素会导致表型异质性,导致不同细胞表现出差异化的药物耐受性,从而增强整个群体对环境压力的适应能力[22]。
研究表明,耐受性与细胞内药物浓度密切相关,高耐受性菌株通常表现出更低的药物蓄积。这一特性不仅与细胞膜屏障完整性相关,还涉及细胞壁功能相关的压力应答途径。其中,热休克蛋白90(heat shock protein 90,Hsp90)作为重要的分子伴侣蛋白,是维持耐受性的关键枢纽:①通过维持钙调磷酸酶的活性,促进其下游转录因子Crz1的激活,从而调控细胞壁稳态;②通过协同下游应激反应通路,帮助真菌在唑类药物压力下存活。因此,抑制Hsp90可显著削弱真菌对唑类药物的耐受性[23]。
细胞壁成分的动态调整是耐受性的另一核心策略。例如,在棘白菌素压力下,念珠菌会减少β-1,3-葡聚糖合成,同时上调几丁质和甘露聚糖含量,以此重塑细胞壁结构、维持细胞壁完整性,又降低药物靶向性[24]。维持细胞膜脂质稳态对耐受性也同样重要,其破坏会增加药物敏感性[25]。
非整倍体作为一种快速基因组适应机制,能使真菌亚群在更高药物浓度下生长,并在压力解除后恢复整倍体状态,表现出非剂量依赖性耐受[26]。例如,特定染色体的非整倍体化可导致对氟康唑的耐受性,而这种耐受性的获得和丧失与非整倍体的动态变化直接相关[27]。
此外,生物被膜通过物理屏障和代谢异质性赋予真菌固有的药物耐受性。①被膜细胞分泌的胞外基质形成物理屏障,限制抗真菌药物的渗透;②被膜内部的低营养、低氧微环境还能诱导真菌激活应激响应通路(如HOG-MAPK通路),从而进入高度耐受的生理状态[28]。值得注意的是,多菌种生物被膜(如真菌-细菌混合群落)还能通过跨界相互作用,进一步增强这种耐受性。
组学研究揭示,耐受性菌株会累积海藻糖等渗透压保护物质或特定代谢物(如抗氧化分子或能量储存物质),并重编程代谢通路(如上调白念珠菌的乙醛酸循环),以储存能量、抵抗氧化应激[29-30]。转录调控则驱动了这些适应性变化。例如,转录激活因子Rpn4对白念珠菌的药物耐受性至关重要,RPN4的缺失会消除其对氟康唑的耐受性[31]。而在新型隐球菌中,脑部葡萄糖微环境通过转录因子Mig1诱导代谢适应,从而产生对两性霉素B的耐受性,这限制了隐球菌性脑膜炎的治疗效果[32]。
-
持留性是指在同一菌群里,部分细胞亚群借助表型异质性在药物压力下存活的现象,这一细胞亚群称为持留菌[20]。持留性并非通过遗传变异获得,而是一种动态的、可逆的表型适应。其核心机制是当药物浓度高于MIC时进入休眠状态以逃避杀伤,待药物撤除后这些细胞可恢复生长[30]。休眠细胞在抗真菌药物撤除后能够重新增殖并占据感染部位,导致慢性感染,这一过程在免疫功能低下患者中尤为显著,是治疗失败和感染复发的重要因素[33]。
其机制主要包括以下几个方面:生长调控相关的TORC1信号通路被抑制会诱导真菌细胞退出增殖周期,进入G0期静止状态,并降低代谢活性,从而削弱细胞对依赖生长的抗真菌药物的敏感性,从而促使持留细胞亚群的形成[34]。此外,持留菌通过增强氧化应激反应能力,以清除抗真菌药物诱导的活性氧累积[35]。生物被膜通过提供物理庇护与低代谢微环境,为部分真菌细胞进入休眠并形成持留菌创造条件。这一机制在医疗器械相关感染中尤为突出,常导致顽固的慢性或复发性感染[36]。
群体遗传学研究表明,真菌群体内遗传多样性也会促进持留性形成。在囊性纤维化患者肺部的曲霉菌感染显示,遗传异质性群体通过维持不同表型细胞来增强整体适应性[37]。在小鼠肺部感染模型中,隐球菌可通过代谢重编程形成持留菌。铁限制和氧化应激等宿主微环境压力是关键的诱导因素,它们能迫使真菌进入低代谢状态,从而降低对药物的敏感性。这种代谢适应过程可能涉及线粒体功能与氧化应激响应通路的协同调控[38]。此外,真菌还进化出特殊结构应对环境压力。分生孢子通过细胞壁修饰和储能物质累积维持休眠状态,黑色素可抵御紫外线或宿主免疫攻击,这些结构特征显著延长真菌在药物胁迫环境中的持留时间[39]。
-
联合用药能降低真菌通过单一突变产生耐药性的风险,在提高抗真菌药物疗效的同时,降低药物用量和毒性。不同种类的抗真菌药物联合使用,能通过靶向不同机制发挥协同效应,适用于侵袭性真菌感染。唑类与棘白菌素类联合用药能有效减少耐药性的发生率,两性霉素B联合5-氟胞嘧啶是隐球菌脑膜炎的一线治疗方案,卡泊芬净与两性霉素B联用对曲霉菌属有极佳的治疗效果,伏立康唑和伊曲康唑合用对念珠菌也表现出协同作用[40]。此外,将抗真菌药物与其他具有抗真菌活性的化合物联用,也被证实能增强抗真菌活性或能解决生物被膜问题。比如,氟康唑联合铁螯合剂不仅能恢复部分真菌对氟康唑的敏感性,还能干扰生物被膜中铁离子代谢,有助于生物被膜的清除[41];Hinokitiol则通过铁剥夺机制抑制真菌生长,并协同增强唑类药物敏感性,其铁螯合能力充分揭示了铁代谢通路作为耐药逆转靶点的潜力[42]。肽类物质与卡泊芬净联用,通过影响细胞膜渗透性,对耳念珠菌表现出100%的协同抑菌作用[43]。
-
研发具有新结构或新作用机制的抗真菌药物,规避真菌的高适应性,是应对其耐药性问题的有效研究方向。研究人员通过结构修饰策略,增强化合物与靶点酶CYP51的亲和力,并改善其在真菌细胞内的累积,由此开发的新一代唑类化合物对白念珠菌、耳念珠菌等多种临床耐药念珠菌均表现出强效抑制作用[44]。1,2,3-三唑类化合物能高效结合真菌酶(如关键靶点酶),并通过对抗由酶突变引起的耐药性以降低耐药性风险,因此被视为极具潜力的新一代抗真菌药物结构[45]。植物内生真菌来源的次生代谢物6-氧甲基-2-羟基大黄素经化学修饰后,其抗真菌活性显著增强,这为开发新型抗耐药先导化合物开辟了新途径[46]。多肽聚合物是另一种新药物结构,其通过非传统作用机制(如穿透真菌膜和破坏细胞器)直接破坏真菌细胞的内部结构,因此不易引发耐药性[47]。研究发现,顺-6-十八碳烯酸是一种新型活性化合物,其作用靶标为Fba1,与当前临床抗真菌药物的靶点不同,因而可避免潜在的交叉耐药问题[48]。
基于新型通路或靶点进行药物开发,是规避真菌现有高适应性机制的有效策略。未折叠蛋白反应(unfolded protein response,UPR)在真菌应激适应、毒力调控和耐药性中起核心作用。一种可行的策略是筛选并开发靶向真菌UPR特有核心组件(如Hac1转录因子)的小分子抑制剂。该方法利用真菌与哺乳动物UPR通路的差异,旨在克服耐药性并避免对宿主同源通路的交叉影响[49]。研究表明,两性霉素B耐药菌株中,赖氨酸琥珀酰化水平的显著升高提示其是耐药的关键因素之一,因此开发靶向琥珀酰化酶的小分子抑制剂有望逆转此类耐药[50]。此外,干预真菌铁死亡相关蛋白(如谷胱甘肽代谢酶),或靶向组蛋白伴侣蛋白Rtt106或染色质重塑复合物SWI/SNF等表观遗传因子,也被证实可有效增强耐药菌株的药物敏感性[51-52]。双靶点策略是克服耐药性的另一有效途径。通过设计结构多样的杂环分子作为双靶点抑制剂,可同时作用于真菌的多个关键通路,从而显著降低耐药风险。此策略还有助于解决真菌与哺乳动物细胞的结构相似性难题,实现选择性抑制并减少宿主毒性。一个典型的例子是CYP51/组蛋白去乙酰化酶双重抑制剂,它能同时抑制真菌甾醇合成和组蛋白去乙酰化酶,不仅可显著干扰真菌的关键酶活性、增强对耐药念珠菌的杀伤作用,也能降低其耐药性演化的风险[53]。
-
病原真菌感染及其高度适应性已对全球公共卫生安全构成严峻挑战。为切实改善临床预后,亟需深入阐明真菌耐药、药物耐受及持留状态的核心分子机制,并在此基础上实施多维度协同防控:一方面积极优化与推广多药联合治疗策略,另一方面加快推进靶向全新作用位点的抗真菌新药研发。未来研究应进一步深化病原真菌-宿主互作的分子机制解析,同时依托人工智能等前沿技术,通过耐药组学大数据深度挖掘、虚拟药物筛选、耐药演化轨迹模拟及高通量表型分析等手段,系统破解病原真菌对抗真菌药物的适应性进化难题,推动个体化精准治疗方案的优化完善,最终为临床抗真菌治疗提供更为高效、安全的全新策略与理论支撑。
Research progress on high adaptability of pathogenic fungi to drugs
-
摘要: 真菌感染是威胁人类健康的重要公共卫生问题。现有抗真菌药物种类较少,且普遍存在抗菌谱窄、易产生耐药性等局限,严重影响临床疗效。病原真菌可通过多重机制形成对现有药物的高适应性,主要表现为耐药性、耐受性和持留性。本文系统综述病原真菌对现有药物形成耐药、耐受及持留的分子机制和调控通路,并探讨联合用药、新型抗真菌药物研发等应对策略,以期为真菌感染的精准治疗提供理论依据和临床参考。Abstract: Fungal infections have emerged as a critical public health issue endangering human health. However, the existing arsenal of antifungal agents is limited in diversity and is commonly plagued by drawbacks including narrow antimicrobial spectrums and the frequent emergence of drug resistance, which severely compromises the efficacy of clinical treatments. Pathogenic fungi can develop extensive adaptability to currently available drugs through multiple mechanisms, which are mainly manifested in three aspects: drug resistance, tolerance and persistence. The molecular mechanisms and regulatory pathways underlying drug resistance, tolerance and persistence in pathogenic fungi were systematically summarized in this review, and the counteractive strategies such as combination therapy and the development of novel antifungal agents were further discussed, which aimed to provide theoretical basis and practical reference for the precision treatment of fungal infections.
-
Key words:
- pathogenic fungi /
- adaptability /
- resistance /
- tolerance /
- persistence
-
[1] AKINOSOGLOU K, PAPAGEORGIOU D, GOGOS C, et al. An update on newer antifungals[J]. Expert Rev Anti Infect Ther, 2025, 23(2-4): 149-158. doi: 10.1080/14787210.2025.2461566 [2] SZYMAŃSKI M, CHMIELEWSKA S, CZYŻEWSKA U, et al. Echinocandins–structure, mechanism of action and use in antifungal therapy[J]. J Enzyme Inhib Med Chem, 2022, 37(1): 876-894. doi: 10.1080/14756366.2022.2050224 [3] BERMAN J, KRYSAN D J. Drug resistance and tolerance in fungi[J]. Nat Rev Microbiol, 2020, 18(6): 319-331. doi: 10.1038/s41579-019-0322-2 [4] NOURRISSON C, MONIOT M, LAVERGNE R A, et al. Acquired fluconazole resistance and genetic clustering in Diutina (Candida) catenulata from clinical samples[J]. Clin Microbiol Infect, 2023, 29(2): 257. e7-257. e11. [5] BÉDARD C, GAGNON-ARSENAULT I, BOISVERT J, et al. Most azole resistance mutations in the Candida albicans drug target confer cross-resistance without intrinsic fitness cost[J]. Nat Microbiol, 2024, 9(11): 3025-3040. doi: 10.1038/s41564-024-01819-2 [6] FANDILOLU P, KUMAR C, PALIA D, et al. Investigating role of positively selected genes and mutation sites of ERG11 in drug resistance of Candida albicans[J]. Arch Microbiol, 2024, 206(11): 437. doi: 10.1007/s00203-024-04159-1 [7] ZARE-BIDAKI M, MALEKI A, GHANBARZADEH N, et al. Expression pattern of drug-resistance genes ERG11 and TAC1 in Candida albicans Clinical isolates[J]. Mol Biol Rep, 2022, 49(12): 11625-11633. doi: 10.1007/s11033-022-07878-0 [8] ROJAS A E, CÁRDENAS L Y, GARCÍA M C, et al. Expression of ERG11 ERG3 MDR1 and CDR1 genes in Candida tropicalis[J]. Biomedica, 2023, 43(Sp.1): 144-155. doi: 10.7705/biomedica.6852 [9] YENIŞEHIRLI G, ALıCı A, YENIŞEHIRLI A. Antifungal drug susceptibility profiles and molecular mechanisms of azole resistance in Candida blood stream isolates[J]. Indian J Med Microbiol, 2023, 45: 100389. doi: 10.1016/j.ijmmb.2023.100389 [10] VU B G, SIMONICOVA L, MOYE-ROWLEY W S. Calcineurin is required for Candida glabrata Pdr1 transcriptional activation[J]. mBio, 2023, 14(6): e02416-e02423. doi: 10.1101/2023.07.10.548434 [11] WASEEM M, DAS S, MONDAL D, et al. Identification of novel inhibitors against Med15a KIX domain of Candida glabrata[J]. Int J Biol Macromol, 2023, 253(Pt 2): 126720. [12] SUCHODOLSKI J, MURASZKO J, KORBA A, et al. Lipid composition and cell surface hydrophobicity of Candida albicans influence the efficacy of fluconazole-gentamicin treatment[J]. Yeast, 2020, 37(1): 117-129. doi: 10.1002/yea.3455 [13] MASSEY J, ZARNOWSKI R, ANDES D. Role of the extracellular matrix in Candida biofilm antifungal resistance[J]. FEMS Microbiol Rev, 2023, 47(6): fuad059. doi: 10.1093/femsre/fuad059 [14] ARASTEHFAR A, DANESHNIA F, HOVHANNISYAN H, et al. A multidimensional assessment of in-host fitness costs of drug resistance in the opportunistic fungal pathogen Candida glabrata[J]. FEMS Yeast Res, 2024, 24: foae035. doi: 10.1093/femsyr/foae035 [15] GÓMEZ-GAVIRIA M, GARCÍA-CARNERO L C, BARUCH-MARTÍNEZ D A, et al. The emerging pathogen Candida metapsilosis: biological aspects, virulence factors, diagnosis, and treatment[J]. Infect Drug Resist, 2024, 17: 171-185. doi: 10.2147/IDR.S448213 [16] BOUTIN C A, LUONG M L. Update on therapeutic approaches for invasive fungal infections in adults[J]. Ther Adv Infect Dis, 2024, 11: 20499361231224980. [17] RAMOS L S, BARBOSA P F, LORENTINO C M A, et al. The multidrug-resistant Candida auris, Candida haemulonii complex and phylogenetic related species: Insights into antifungal resistance mechanisms[J]. Curr Res Microb Sci, 2025, 8: 100354. [18] CAROLUS H, PIERSON S, LAGROU K, et al. Amphotericin B and other polyenes: discovery, clinical use, mode of action and drug resistance[J]. J Fungi, 2020, 6(4): E321. doi: 10.3390/jof6040321 [19] SHBETA M, KOPP T, VORONOV I, et al. Fluorescent probes derived from the polyene class of antifungal drugs reveal distinct localization patterns and resistance-associated vacuolar sequestration in Candida Species[J]. Angew Chem Int Ed, 2026, 65(2): e21135. doi: 10.1002/anie.202521135 [20] KE W X, XIE Y Y, CHEN Y Y, et al. Fungicide-tolerant persister formation during cryptococcal pulmonary infection[J]. Cell Host Microbe, 2024, 32(2): 276-289. e7. [21] BRAUNER A, FRIDMAN O, GEFEN O, et al. Distinguishing between resistance, tolerance and persistence to antibiotic treatment[J]. Nat Rev Microbiol, 2016, 14(5): 320-330. doi: 10.1038/nrmicro.2016.34 [22] DUMEAUX V, MASSAHI S, BETTAUER V, et al. Candida albicans exhibits heterogeneous and adaptive cytoprotective responses to antifungal compounds[J]. eLife, 2023, 12: e81406. doi: 10.7554/eLife.81406 [23] ZHENG L J, XU Y, WANG C, et al. Ketoconazole induces reversible antifungal drug tolerance mediated by trisomy of chromosome R in Candida albicans[J]. Front Microbiol, 2024, 15: 1450557. doi: 10.3389/fmicb.2024.1450557 [24] SAH S K, YADAV A, STAHL T, et al. Echinocandin adaptation in Candida albicans is accompanied by altered chromatin accessibility at gene promoters and by cell wall remodeling[J]. J Fungi, 2025, 11(2): 110. doi: 10.3390/jof11020110 [25] FENG Y R, LU H, WHITEWAY M, et al. Understanding fluconazole tolerance in Candida albicans: implications for effective treatment of candidiasis and combating invasive fungal infections[J]. J Glob Antimicrob Resist, 2023, 35: 314-321. doi: 10.1016/j.jgar.2023.10.019 [26] SUN L L, LI H, YAN T H, et al. Aneuploidy mediates rapid adaptation to a subinhibitory amount of fluconazole in Candida albicans[J]. Microbiol Spectr, 2023, 11(2): e03016-e03022. doi: 10.1128/spectrum.03016-22 [27] YANG F, SCOPEL E F C, LI H, et al. Antifungal tolerance and resistance emerge at distinct drug concentrations and rely upon different aneuploid chromosomes[J]. mBio, 2023, 14(2): e00227-e00223. doi: 10.1101/2022.11.30.518455 [28] ZARNOWSKI R, HORTON M V, JOHNSON C J, et al. Dual function of Candida auris mannosyltransferase, MNT5, in biofilm community protection from antifungal therapy and the host[J]. mBio, 2025, 16(4): e00346-e00325. doi: 10.1128/mbio.00346-25 [29] ADEJOR J, TUMUKUNDE E, LI G Q, et al. Stepping out of the dark: how metabolomics shed light on fungal biology[J]. FEMS Microbiol Rev, 2025, 49: fuaf028. doi: 10.1093/femsre/fuaf028 [30] EL MEOUCHE I, JAIN P, JOLLY M K, et al. Drug tolerance and persistence in bacteria, fungi and cancer cells: Role of non-genetic heterogeneity[J]. Transl Oncol, 2024, 49: 102069. doi: 10.1016/j.tranon.2024.102069 [31] YAU K P S, WEERASINGHE H, OLIVIER F A B, et al. The proteasome regulator Rpn4 controls antifungal drug tolerance by coupling protein homeostasis with metabolic responses to drug stress[J]. PLoS Pathog, 2023, 19(4): e1011338. doi: 10.1371/journal.ppat.1011338 [32] CHEN L, TIAN X Y, ZHANG L Y, et al. Brain glucose induces tolerance of Cryptococcus neoformans to amphotericin B during meningitis[J]. Nat Microbiol, 2024, 9(2): 346-358. doi: 10.1038/s41564-023-01561-1 [33] SU Y Y, LI Y, YI Q L, et al. Insight into the mechanisms and clinical relevance of antifungal heteroresistance[J]. J Fungi, 2025, 11(2): 143. doi: 10.3390/jof11020143 [34] BOJSEN R, REGENBERG B, FOLKESSON A. Persistence and drug tolerance in pathogenic yeast[J]. Curr Genet, 2017, 63(1): 19-22. doi: 10.1007/s00294-016-0613-3 [35] WUYTS J, VAN DIJCK P, HOLTAPPELS M. Fungal persister cells: The basis for recalcitrant infections?[J]. PLoS Pathog, 2018, 14(10): e1007301. doi: 10.1371/journal.ppat.1007301 [36] BICER M. Exploring therapeutic avenues: mesenchymal stem/stromal cells and exosomes in confronting enigmatic biofilm-producing fungi[J]. Arch Microbiol, 2023, 206(1): 11. doi: 10.1007/s00203-023-03744-0 [37] MURANTE D, HOGAN D A. Drivers of diversification in fungal pathogen populations[J]. PLoS Pathog, 2024, 20(9): e1012430. doi: 10.1371/journal.ppat.1012430 [38] AMICH J, BROMLEY M, GOLDMAN G H, et al. Toward the consensus of definitions for the phenomena of antifungal tolerance and persistence in filamentous fungi[J]. mBio, 2025, 16(4): e03475-e03424. doi: 10.1128/mbio.03475-24 [39] CORONA RAMIREZ A, BREGNARD D, JUNIER T, et al. Assessment of fungal spores and spore-like diversity in environmental samples by targeted lysis[J]. BMC Microbiol, 2023, 23(1): 1-19. doi: 10.1186/s12866-023-02809-w [40] MOGHADAM S, ZARRINFAR H, NASERI A, et al. Investigating the susceptibility profiles and in vitro combinations of caspofungin, itraconazole, fluconazole, voriconazole, clotrimazole, and amphotericin B against clinical isolates causing fungal keratitis[J]. Diagn Microbiol Infect Dis, 2025, 112(3): 116806. doi: 10.1016/j.diagmicrobio.2025.116806 [41] AN L L, TAN J W, WANG Y Y, et al. Synergistic effect of the combination of deferoxamine and fluconazole in vitro and in vivo against fluconazole-resistant Candida Spp[J]. Antimicrob Agents Chemother, 2022, 66(11): e00725-e00722. [42] JIN X Y, ZHANG M, LU J H, et al. Hinokitiol chelates intracellular iron to retard fungal growth by disturbing mitochondrial respiration[J]. J Adv Res, 2021, 34: 65-77. doi: 10.1016/j.jare.2021.06.016 [43] SHABAN S, PATEL M, AHMAD A. Fungicidal activity of human antimicrobial peptides and their synergistic interaction with common antifungals against multidrug-resistant Candida auris[J]. Int Microbiol, 2023, 26(2): 165-177. doi: 10.21203/rs.3.rs-1938651/v1 [44] CHEN Y Y, LI Y X, NAHAR K S, et al. New generation modified azole antifungals against multidrug-resistant Candida auris[J]. J Med Chem, 2025, 68(13): 14054-14071. doi: 10.1021/acs.jmedchem.5c01253 [45] LAL K, GROVER A, RAGSHANIYA A, et al. Current advancements and future perspectives of 1, 2, 3-triazoles to target lanosterol 14α-demethylase(CYP51), a cytochrome P450 enzyme: a computational approach[J]. Int J Biol Macromol, 2025, 315(Pt 1): 144240. [46] PRAJAPATI C, RAI S N, SINGH A K, et al. An update of fungal endophyte diversity and strategies for augmenting therapeutic potential of their potent metabolites: recent advancement[J]. Appl Biochem Biotechnol, 2025, 197(5): 2799-2866. doi: 10.1007/s12010-024-05098-9 [47] WU Y M, JIANG W N, CONG Z H, et al. An effective strategy to develop potent and selective antifungal agents from cell penetrating peptides in tackling drug-resistant invasive fungal infections[J]. J Med Chem, 2022, 65(10): 7296-7311. doi: 10.1021/acs.jmedchem.2c00274 [48] WANG X R, ZHONG H, MA S S, et al. Discovery of petroselinic acid with in vitro and in vivo antifungal activity by targeting fructose-1, 6-bisphosphate aldolase[J]. Phytomedicine, 2024, 133: 155948. doi: 10.1016/j.phymed.2024.155948 [49] ZHOU H, ZHANG J P, WANG R, et al. The unfolded protein response is a potential therapeutic target in pathogenic fungi[J]. FEBS J, 2025, 292(19): 5008-5025. doi: 10.1111/febs.70100 [50] ZHANG L, XIAO J Z, DU M W, et al. Post-translational modifications confer amphotericin B resistance in Candida krusei isolated from a neutropenic patient[J]. Front Immunol, 2023, 14: 1148681. doi: 10.3389/fimmu.2023.1148681 [51] NIKOLOV V N, MALAVIA D, KUBOTA T. SWI/SNF and the histone chaperone Rtt106 drive expression of the Pleiotropic Drug Resistance network genes[J]. Nat Commun, 2022, 13(1): 1968. doi: 10.1038/s41467-022-29591-z [52] SHANG X X, ZHANG Q, YANG Q L, et al. Do fungi also undergo “ferroptosis”? A microscopic exploration of cellular death[J]. Apoptosis, 2025, 30(11-12): 2495-2510. doi: 10.1007/s10495-025-02164-3 [53] ZHU T B, CHEN X, LI C L, et al. Lanosterol 14α-demethylase (CYP51)/histone deacetylase (HDAC) dual inhibitors for treatment of Candida tropicalis and Cryptococcus neoformans infections[J]. Eur J Med Chem, 2021, 221: 113524. doi: 10.1016/j.ejmech.2021.113524 -




 下载:
下载: