-
随着抗菌药物的广泛使用,细菌耐药问题已经成为全球面临的严重公共卫生挑战。近年来,在院内分离菌株中,革兰阴性菌(G−菌)占比远超革兰阳性菌(G+菌),其中耐药株日益增多[1],特别是耐碳青霉烯类肠杆菌属(CRE)、多重耐药(MDR)和泛耐药(XDR),甚至全耐药(PDR)菌株的出现(具体定义参考国际专家建议的暂行标准[2-3]),给临床抗感染治疗带来更多困难。并且不同地区抗菌药物应用和耐药菌流行分布有所不同,在2020年全国耐药监测报告中发现,各种耐药菌检出率排名前3位的地区中,北京市、上海市和河南省出现次数较多,如上海市、河南省及北京市是全国耐碳青霉烯肺炎克雷伯菌(CR-KPN)检出率最高的3个地区[4]。作为上海市北部的区属某二级综合医院(以下简称本院),周边社区老年患者多,2022年起又承担着大量新冠患者救治任务,因此本院抗菌药物的使用量一直居高不下。
本研究收集本院2018年7月至2023年3月细菌的分离检出数据,分析近年来院内耐药菌变化趋势,有助于临床合理选择和使用抗菌药物,也为制定抗菌药物管理策略提供了数据基础。
-
收集2018年7月1日至2023年3月31日本院临床分离的菌株,本次入院时间段内同一患者同一标本取第一次送检结果,并剔除重复菌株。采用法国梅里埃公司的vitek2_compact细菌鉴定仪进行菌株鉴定。
-
本院主要采用MIC法,K-B法辅助进行药物敏感性试验,检验结果参考美国临床实验室标准协会(CLSI)指南。质控菌株有大肠埃希菌ATCC25922、铜绿假单胞菌ATCC27853、粪肠球菌ATCC29212和金黄色葡萄球菌ATCC25923等。
-
使用院内检验系统、Excel软件等对每个季度分离菌株的类型和细菌耐药情况等进行统计分析和数据整理。
-
菌株标本主要来源于粪便、血液、尿液、分泌物、脓液和呼吸道标本等。其中血液标本阳性率7.97%,呼吸道标本(咽拭子+痰液)阳性率33.04%,粪便标本阳性率4.59%,中段尿标本阳性率30.26%。
-
2018年7月1日至2023年3月31日本院共分离检出细菌病原菌14 844株,其中G+菌4 757株(32.05%)、G−菌10 087株(67.95%),G−菌检出的菌株数是G+菌的2倍多。本院G−菌和G+菌各季度检出率较平稳,分别为68.22%和31.78%。可以看出本院致病病原细菌以G−菌为主,也是需要关注的焦点。
-
G−菌中最为常见的是大肠埃希菌(G−菌中占比30.25%)、肺炎克雷伯菌(G−菌中占比29.04%)、铜绿假单胞菌(G−菌中占比22.59%)和鲍曼不动杆菌(G−菌中占比15.70%),如表1所示。
表 1 临床分离检出G−菌菌株的分布情况
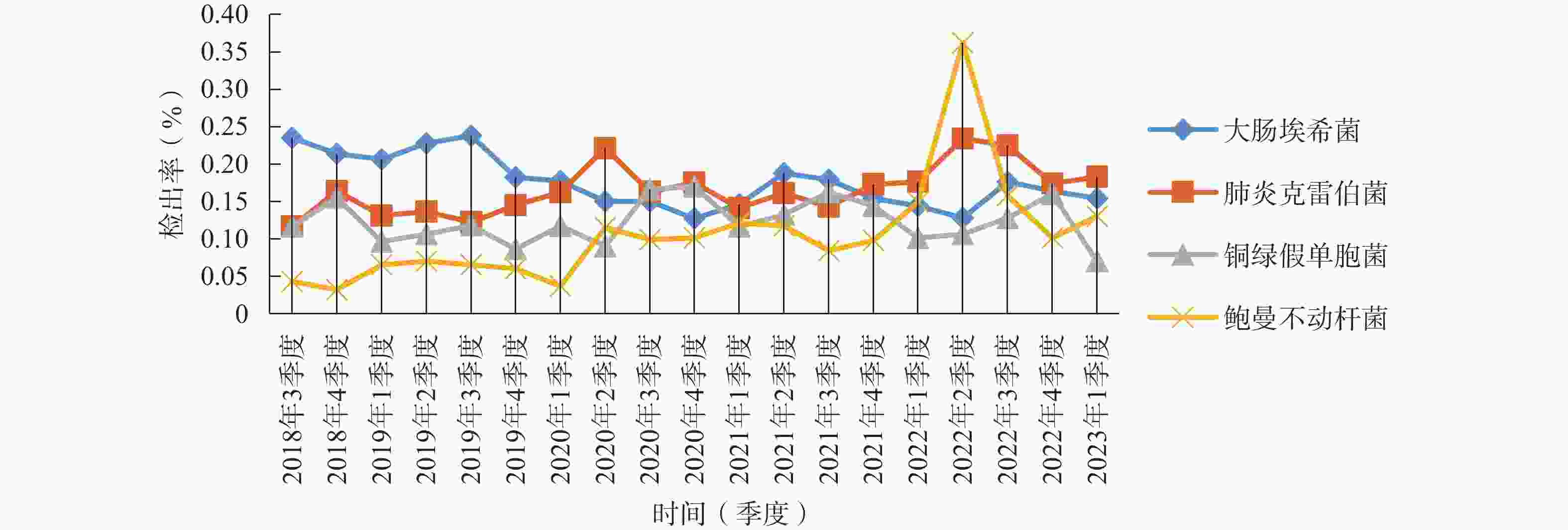
菌株 菌株数 构成比(%) 大肠埃希菌 3 051 30.25 肺炎克雷伯菌 2 929 29.04 铜绿假单胞菌 2 279 22.59 鲍曼不动杆菌 1 584 15.70 如图1所示,2018年7月至2023年3月各季度检出G−菌病原菌构成比和具体检出数值基本较为稳定(2022年第2季度本院成为疫情定点医院,标本数量较少,存在一定偶然性)。大肠埃希菌占总检出菌株数的20%左右,呈下降趋势,肺炎克雷伯菌和铜绿假单胞菌在15%左右,其中肺炎克雷伯菌检出率呈上升趋势,于2020年第2季度起总体上超过大肠埃希菌检出率位居第一,铜绿假单胞菌检出率略低于肺炎克雷伯菌,近5年来鲍曼不动杆菌检出率上升较为明显,由2018年第3季度的4.96%上升至2023年第1季度的18.75%。
-
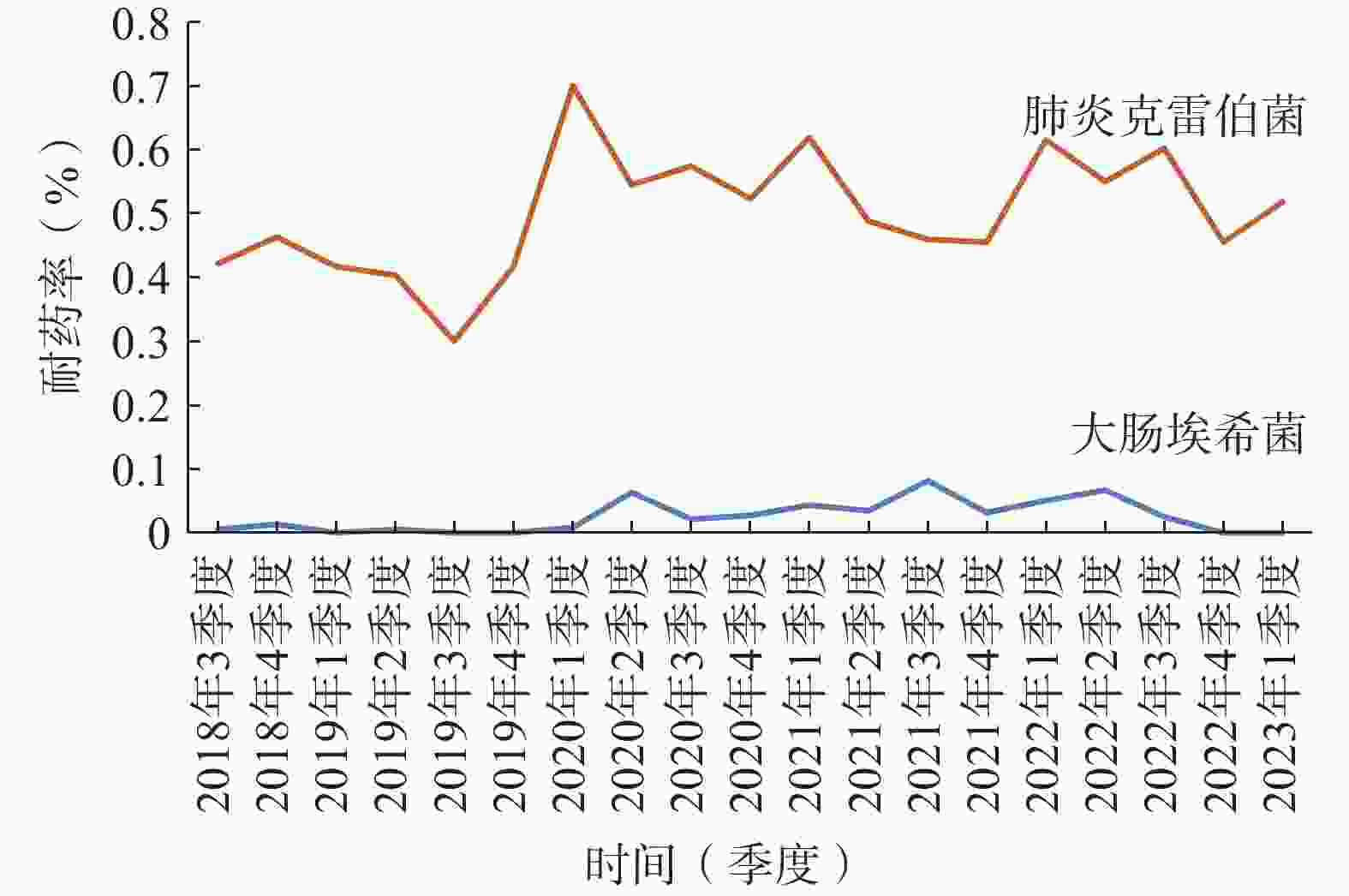
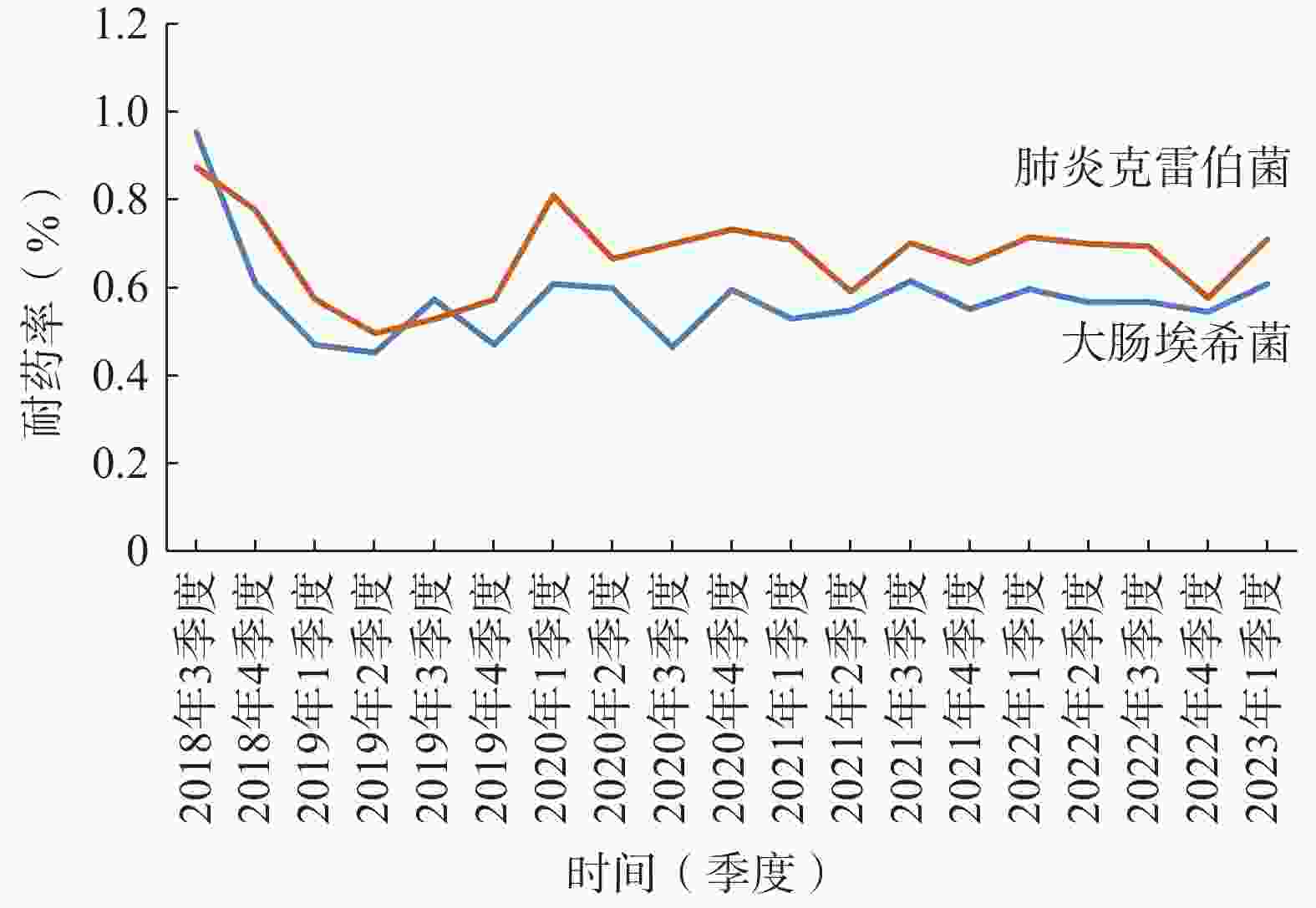
本院对检出的肠杆菌科细菌均进行了产超广谱β-内酰胺酶(ESBLs)监测。2022年大肠杆菌和肺炎克雷伯菌ESBLs的检出率为43.23%和19.50%;对碳青霉烯耐药的大肠杆菌(CR-EC)和肺炎克雷伯菌检出率分别为2.92%和58.07%,对亚胺培南的耐药率逐渐趋于平稳(图2);喹诺酮类耐药大肠杆菌(QNR-EC)检出率为58.91%,头孢曲松耐药肺炎克雷伯菌(CRO-R KP)检出率为62.41%。但头孢唑林对上述两种肠杆菌的耐药率有下降趋势 (图3)。总体上看肺炎克雷伯菌的耐药形势较大肠杆菌更为严峻,对头孢菌素类、喹诺酮类、β-内酰胺酶抑制剂(除阿维巴坦)和呋喃妥因的耐药率均>50%,对氨基糖苷类和复方新诺明耐药率>30%,仅对替加环素和头孢他啶/阿维巴坦较为敏感,具体数据详见表2。
表 2 2022年大肠埃希菌和肺炎克雷伯菌的耐药率(%)
检测项目 大肠埃希菌
(n=393)肺炎克雷伯菌
(n=331)ESBL检测 43.23 19.50 氨苄西林 78.64 100.00 氨苄西林/舒巴坦 35.56 66.42 哌拉西林/他唑巴坦 3.21 57.08 头孢唑林 56.95 66.22 头孢呋辛 64.52 55.57 头孢曲松 53.41 62.41 头孢他啶 26.48 60.59 头孢吡肟 16.25 57.85 头孢替坦 4.44 53.33 头孢哌酮/舒巴坦 5.34 56.82 头孢他啶/阿维巴坦 1.32 1.89 氨曲南 32.87 60.00 亚胺培南 2.51 55.76 美罗培南 2.52 55.46 厄他培南 2.92 58.07 庆大霉素 29.43 50.70 妥布霉素 10.06 47.54 阿米卡星 2.17 32.99 替加环素 0.31 4.62 环丙沙星 58.91 60.83 左氧氟沙星 58.88 60.57 复方新诺明 41.07 39.58 呋喃妥因 1.45 50.31 -
2022年碳青霉烯耐药铜绿假单胞菌(CR-PA)和鲍曼不动杆菌(CR-AB)的检出率为22.02%和74.34%,2020年耐药率上升,现趋于稳定(CR-PA检出率约25%,CR-AB检出率约80%);多重耐药铜绿假单胞菌(MDR-PA)检出率26.41%,多重耐药鲍曼不动杆菌(MDR-AB)的检出率为74.34%;铜绿假单胞菌对氨基糖苷类、头孢他啶和头孢吡肟敏感性较好,耐药率均<20%,对氟喹诺酮类的耐药率<30%。鲍曼不动杆菌耐药性高,对头孢菌素类、碳青霉烯类和喹诺酮类的耐药率均>70%,对氨基糖苷类的耐药率>60%,仅对替加环素敏感率高,具体数据详见表3。
表 3 2022年铜绿假单胞菌和鲍曼不动杆菌的耐药率(%)
检测项目 铜绿假单胞菌
(n=269)鲍曼不动杆菌
(n=289)氨苄西林 100.00 100.00 氨苄西林/舒巴坦 98.83 62.17 哌拉西林/他唑巴坦 5.10 70.88 头孢唑林 100.00 100.00 头孢呋辛 − − 头孢曲松 98.83 71.93 头孢他啶 6.44 72.10 头孢吡肟 5.73 72.71 头孢替坦 100.00 100.00 头孢哌酮/舒巴坦 6.49 49.85 头孢他啶/阿维巴坦 4.03 − 氨曲南 19.69 100.00 亚胺培南 22.02 72.10 美罗培南 17.48 74.34 厄他培南 − − 庆大霉素 17.28 67.03 妥布霉素 18.68 66.36 阿米卡星 0 60.83 替加环素 − 3.37 环丙沙星 26.41 73.61 左氧氟沙星 24.13 72.05 复方新诺明 98.83 23.79 呋喃妥因 100.00 100.00 注:“−”表示不适用。 -
近5年本院检出数居于前列的是大肠埃希菌、肺炎克雷伯菌、铜绿假单胞菌、金黄色葡萄球菌、粪肠球菌、鲍曼不动杆菌、屎肠球菌和表皮葡萄球菌,2022年病原菌的流行分布情况与Chinet报道[5]基本一致。本院各季度细菌分离检出构成比基本稳定,反映出本院收治的患者及病种较为稳定,未出现院内感控问题。但细菌耐药仍较严重,特别是G− 菌CRE(对碳青霉烯类抗生素耐药菌)、MDR和XDR问题。肺炎克雷伯菌耐药形势严峻,总体耐药率要高于Chinet报道[5]。大肠杆菌的耐药率与Chinet报道[5]大体一致。碳青霉烯类一直被称为治疗肠杆菌科多重耐药菌(尤其是ESBLs菌)的“最后一道防线”,但随着抗菌药物的滥用,对其的耐药菌株的检出率呈上升趋势[6]。2022年本院肺炎克雷伯菌对亚胺培南和美罗培南的耐药率远高于2022年Chinet报告中的22.60%和24.20%,在2021年第2季度也开始出现对厄他培南耐药菌株,2023年第1季度对亚胺培南耐药率高达54.82%。
目前提出4种CRE耐药机制:①产碳青霉烯酶(产KPC为主的A类碳青霉烯酶、以锌离子为活性中心的B类金属β-内酰胺酶和D类的OXA-48);②产AmpC酶或ESBLs合并外膜蛋白的丢失或改变;③结合位点的缺失、数量下降或亲和性降低/药物作用靶点的改变;④外排泵的高表达/细菌外排泵系统的改变。碳青霉烯酶又分为A类、B类和D类[7]。经研究表明,CRE耐药机制主要是产碳青霉烯酶,其中CR-KP最常见,其耐药机制与总体CRE一致并有相关研究[8-11]佐证。另外有研究表明,CR-KP重要的是有AcrAB-TolC外排泵,该泵是由外膜通道TolC、位于内膜的继发性主动转运体AcrB和周质蛋白AcrA三者构成的完整膜蛋白,该主动转运系统可有方向性的运输不同的化合物,使得肺炎克雷伯菌对多种抗菌药物产生耐药[12]。CRE对目前临床上常应用的绝大多数抗菌药物都耐药,给临床治疗带来巨大困难。在应对泛耐药Kpn,有研究[13]提出增加药物敏感试验(CLSI未推荐)的种类,为临床治疗感染提供有效选择。
本院非发酵菌(特别是鲍曼不动杆菌)分离检出率有逐渐上升趋势,临床上分布广泛,耐药形势极为严峻。CR-AB检出率要高于2022年Chinet监测[5]。鲍曼不动杆菌已成为我国医院感染最主要病原菌,在院内广泛存在,且其抵抗力强、定植和污染多,可通过医务工作者的手和污染的医疗器械以及空气等引起院内感染,病死率高[14]。本院鲍曼不动杆菌检出率增长过快,且对大多数抗菌药物的耐药率高于75%。肺炎克雷伯菌、鲍曼不动杆菌等细菌耐药未能有效改善,以及近年来出现CRE、MDR和XDR问题等,这些情况都需要引起临床警惕。在2020年第1季度本院细菌耐药有小幅度上升情况,可能与疫情爆发,大量使用抗菌药物进行经验治疗有一定相关性。
前7批国家组织药品集中带量采购,已有42种抗菌药物(不包括局部用药)被纳入其中,美罗培南、法罗培南、厄他培南已被纳入第7批集中大量采购中。有专家对于碳青霉烯类纳入集采表示担忧,为此,中华医学会临床药学分会与中华医学会细菌感染与耐药防治分会针对医疗机构在抗菌药物集采执行过程中面临的问题,组织药学、感染、医保、政策及方法学专家共同撰写专家共识[15]。抗菌药物目录管理在药品集采常态化背景下,医疗机构应主动及时开展抗菌药物供应目录遴选和评估工作,确保本医疗机构抗菌药物目录科学合理前提下,开展病原菌耐药情况的分析和研究,有助于提高临床抗感染治疗的针对性和有效性,更能及时发现问题和遏制细菌耐药。
Retrospective analysis of the epidemic characteristics of Gram-negative bacteria in a second-class hospital in Shanghai
-
摘要:
目的 回顾性分析医院内分离病原细菌(特别是革兰阴性菌,G−菌)的分布情况和耐药特征,以促进医院合理使用抗菌药。 方法 收集2018年7月至2023年3月每季度全院分离检出的病原菌以及药物敏感试验结果,并进行回顾性分析。 结果 共分离检出病原细菌14 844株,其中,革兰阳性菌(G+菌)4 757株(32.05%),G−菌10 087株(67.95%)。产超广谱β-内酰胺酶大肠埃希菌检出率为43.23%,对碳青霉烯类和加酶抑制剂保持着较高的敏感性,敏感率约99.00%。肺炎克雷伯菌的耐药情况较为严重,出现耐碳青霉烯、多重耐药和泛耐药菌。2022年,碳青霉烯类耐药肺炎克雷伯菌检出率为54.82%;非发酵菌中碳青霉烯类耐药铜绿假单胞菌和碳青霉烯类耐药鲍曼不动杆菌的检出率为22.02%和74.34%,多重耐药的鲍曼不动杆菌的检出率>70%。 结论 G−菌耐药问题仍较为严重,特别是肺炎克雷伯和鲍曼不动杆菌。细菌耐药问题给临床治疗带来极大的挑战,有必要进行定期监测以促进合理用药。 Abstract:Objective To retrospectively analyze the distribution and drug resistant characteristics of isolated pathogens (especially Gram-negative bacteria) in hospital and promote the rational use of antibacterial drugs. Methods The pathogens and drug sensitivity test results were collected from the whole hospital every quarter from July 2018 to March 2023, and were conducted retrospective analysis. Results A total of 14 844 pathogens were isolated and detected, including 4 757 Gram-positive bacteria (32.05%) and 10 087 Gram-negative bacteria (67.95%). The detection rate of extended spectrum beta-lactamases Escherichia coli was 43.23%, and it maintained high sensitivity to carbapenems and enzyme inhibitors, and the sensitivity rate was about 99.00%. The drug resistance of Klebsiella pneumoniae was more serious, and carbapenem-resistant, multi-drug resistance and extensively-drug resistance appeared. In 2022, the detection rate of carbapenem-resistant Klebsiella pneumoniae was 54.82%; the detection rates of carbapenem-resistant Pseudomonas Aeruginosa and carbapenem-resistant Acinetobacter baumannii in non-fermentative bacteria were 22.02% and 74.34%, the detection rate of multi-drug resistant Acinetobacter baumannii was >70%. Conclusion The problem of drug resistance of Gram-negative bacteria was still serious, especially in Klebsiella pneumoniae and Acinetobacter baumannii. The problem of bacterial resistance poses great challenges to clinical treatment, and it is necessary to conduct regular monitoring and promote rational drug use. -
Key words:
- bacterial resistance /
- antibiotics /
- Gram-negative bacteria
-
表 1 临床分离检出G−菌菌株的分布情况
菌株 菌株数 构成比(%) 大肠埃希菌 3 051 30.25 肺炎克雷伯菌 2 929 29.04 铜绿假单胞菌 2 279 22.59 鲍曼不动杆菌 1 584 15.70 表 2 2022年大肠埃希菌和肺炎克雷伯菌的耐药率(%)
检测项目 大肠埃希菌
(n=393)肺炎克雷伯菌
(n=331)ESBL检测 43.23 19.50 氨苄西林 78.64 100.00 氨苄西林/舒巴坦 35.56 66.42 哌拉西林/他唑巴坦 3.21 57.08 头孢唑林 56.95 66.22 头孢呋辛 64.52 55.57 头孢曲松 53.41 62.41 头孢他啶 26.48 60.59 头孢吡肟 16.25 57.85 头孢替坦 4.44 53.33 头孢哌酮/舒巴坦 5.34 56.82 头孢他啶/阿维巴坦 1.32 1.89 氨曲南 32.87 60.00 亚胺培南 2.51 55.76 美罗培南 2.52 55.46 厄他培南 2.92 58.07 庆大霉素 29.43 50.70 妥布霉素 10.06 47.54 阿米卡星 2.17 32.99 替加环素 0.31 4.62 环丙沙星 58.91 60.83 左氧氟沙星 58.88 60.57 复方新诺明 41.07 39.58 呋喃妥因 1.45 50.31 表 3 2022年铜绿假单胞菌和鲍曼不动杆菌的耐药率(%)
检测项目 铜绿假单胞菌
(n=269)鲍曼不动杆菌
(n=289)氨苄西林 100.00 100.00 氨苄西林/舒巴坦 98.83 62.17 哌拉西林/他唑巴坦 5.10 70.88 头孢唑林 100.00 100.00 头孢呋辛 − − 头孢曲松 98.83 71.93 头孢他啶 6.44 72.10 头孢吡肟 5.73 72.71 头孢替坦 100.00 100.00 头孢哌酮/舒巴坦 6.49 49.85 头孢他啶/阿维巴坦 4.03 − 氨曲南 19.69 100.00 亚胺培南 22.02 72.10 美罗培南 17.48 74.34 厄他培南 − − 庆大霉素 17.28 67.03 妥布霉素 18.68 66.36 阿米卡星 0 60.83 替加环素 − 3.37 环丙沙星 26.41 73.61 左氧氟沙星 24.13 72.05 复方新诺明 98.83 23.79 呋喃妥因 100.00 100.00 注:“−”表示不适用。 -
[1] 李继霞, 公衍文. 多重耐药菌医院感染状况分析[J]. 检验医学, 2013, 28(9):784-788. [2] Centers for Disease Control and Prevention. Antibiotic resis-tance threats in the United States 2019[EB/OL]. [2020-10-08]. https://www.cdc.gov/drugresistance/pdf/threats-report/2019-arthreats-report-508.Pdf. [3] 国家卫生计生委办公厅. 国家卫生计生委办公厅关于印发麻醉等6个专业质控指标(2015年版)的通知国卫办医函〔2015〕252号[EB/OL].(2015 -04 -10)[2020 -10 -08]. http://www.nhc.gov.cn/yzygj/s3585/201504/5fa7461c3d044cb6a93eb6cc6eece087.shtml. [4] 全国细菌耐药监测网. 2020年全国细菌耐药监测报告[J]. 中华检验医学杂志, 2022, 45(2):122-136. doi: 10.3760/cma.j.cn114452-20211118-00721 [5] HU F P, GUO Y, YANG Y, et al. Resistance reported from China antimicrobial surveillance network (CHINET) in 2022[J]. Eur J Clin Microbiol Infect Dis, 2023, 38:1-7. [6] HU F P, CHEN S D, XU X G, et al. Emergence of carbapenem-resistant clinical Enterobacteriaceae isolates from a teaching hospital in Shanghai, China[J]. J Med Microbiol, 2012, 61(1):132-136. doi: 10.1099/jmm.0.036483-0 [7] 李翠翠, 胡同平. 碳青霉烯类耐药肠杆菌科细菌的耐药机制研究进展[J]. 检验医学与临床, 2019, 16(11):1600-1604. doi: 10.3969/j.issn.1672-9455.2019.11.040 [8] VEERARAGHAVAN B, SHANKAR C, KARUNASREE S, et al. Carbapenem resistant Klebsiella pneumoniae isolated from bloodstream infection: Indian experience[J]. Pathog Glob Health, 2017, 111(5):240-246. doi: 10.1080/20477724.2017.1340128 [9] 杨雪, 刘琳, 张湘燕. 耐碳青霉烯类肺炎克雷伯杆菌的耐药机制及治疗策略研究进展[J]. 医学研究生学报, 2018, 31(4):430-434. [10] TIAN D X, PAN F, WANG C, et al. Resistance phenotype and clinical molecular epidemiology of carbapenem-resistant Klebsiella pneumoniae among pediatric patients in Shanghai[J]. Infect Drug Resist, 2018, 11:1935-1943. doi: 10.2147/IDR.S175584 [11] LIN D, CHEN J, YANG Y, et al. Epidemiological study of carbapenem-resistant Klebsiella pneumoniae[J]. Open Med, 2018, 13:460-466. doi: 10.1515/med-2018-0070 [12] 乔晓彧, 芦起. 肺炎克雷伯菌耐碳青霉烯类药物的机制[J]. 临床儿科杂志, 2015, 33(10):907-911. doi: 10.3969/j.issn.1000-3606.2015.10.017 [13] 王艳艳, 刘红, 杜昕, 等. 泛耐药肺炎克雷伯菌株的医院内流行特性的研究[J]. 中华微生物学和免疫学杂志, 2011, 31(3):208-212. doi: 10.3760/cma.j.issn.0254-5101.2011.03.004 [14] 孙淑娟, 张才擎. 感染性疾病[M]. 北京: 人民卫生出版社, 2014: 633-638. [15] 中华医学会临床药学分会, 中华医学会细菌感染与耐药防治分会《医疗机构抗菌药物集中带量采购管理专家共识》编写组. 医疗机构抗菌药物集中带量采购管理专家共识[J]. 医药导报,2023,42(1): 1-5. -




 下载:
下载: