-
2023年10月以来,全国多地儿童医院内科门诊接诊肺炎支原体感染的患儿增多,肺炎支原体感染发病率有所上升。部分地区患儿呈现低龄化,即1至3岁肺炎支原体肺炎(mycoplasma pneumoniae pneumonia,MPP)患儿数量有所增加。MPP是中国5岁及以上儿童最主要的社区获得性肺炎[1],可以累及支气管、细支气管、肺泡和肺间质[2]。
对轻症患者,抗肺炎支原体治疗首选敏感抗生素,包括大环内酯类、新型四环素类和喹诺酮类抗菌药物[3]。由于新型四环素类抗菌药物8岁以下儿童禁用,喹诺酮类抗菌药物18 岁以下儿童禁用,两者都会影响儿童生长发育,故大环内酯类抗菌药物则成为治疗儿童MPP感染的首选药物[1,4]。
大环内酯类抗生素主要有阿奇霉素、克拉霉素、红霉素等,均可对MPP发挥一定效果[3]。由于抗菌药物滥用屡见不鲜,不良事件(adverse event,AE)发生率普遍较高,探索儿童使用大环内酯类抗生素的安全性,在治疗儿童MPP选用药物时意义重大。
本研究通过对美国食品药品监督管理局(FDA)不良事件报告系统(FAERS)数据库中大环内酯类抗生素(主要包括阿奇霉素、克拉霉素和红霉素)的AE报告信号进行检测,挖掘潜在的安全风险,为儿童MPP临床安全用药提供基于真实世界的循证依据。
-
FAERS是FDA重要的公开数据库,用于收集已批准药物的AE和药物错误相关报告[5-6]。本研究提取2004年第1季度至2023年第2季度FAERS数据库中阿奇霉素、克拉霉素、红霉素的12岁以下儿童AE报告数据,检索对象为首要怀疑药品。
排除无关、信息不确定及重复报告后,按《监管活动医学词典》(MedDRA)(26.0版)“首选术语(preferred term,PT)”进行编码和系统器官分类(system organ class,SOC),最终得到总的AE报告数[7]。收集纳入报告中患者年龄、性别、报告地区、AE结局、报告年份等信息。
-
采用描述性分析来呈现与阿奇霉素、克拉霉素、红霉素儿童相关的所有AE报告的特征。常见的数据挖掘方法通过使用不相称性分析方法,包括报告比值比法(reporting odds ratio,ROR)、比例报告比值比法(proportional reporting ratio,PRR)、贝叶斯置信区间递进神经网络法(Bayesian confidence propagation neural network,BCPNN)和多项伽玛泊松分布缩减法(multi-item Gamma Poisson shrinker,MGPS)等[8-11]。本研究采用ROR法联合BCPNN法进行AE信号挖掘,当2种算法均呈阳性时,即目标AE的报告数量不少于3例,ROR 95%置信区间(CI)的下限超过1且BCPNN 95% 置信区间下限(IC-2SD)超过0,判断为潜在风险信号。其中,0<IC-2SD<1.5 为弱信号,1.5≤IC-2SD<3.0 为中强信号,IC-2SD≥3.0为强信号[12]。
-
使用阿奇霉素、克拉霉素、红霉素的儿童人口学特征见表1。2004年第1季度至2023年第2季度,从FAERS数据库中,共检索到阿奇霉素AE报告数1 024份,克拉霉素AE报告数460份,红霉素AE报告131份。
表 1 使用阿奇霉素、克拉霉素、红霉素的儿童人口学特征及AE结局[n(%)]
阿奇霉素 克拉霉素 红霉素 性别 男 530(51.8) 204(44.3) 69(52.7) 女 436(42.6) 241(52.4) 49(37.4) 未填写 58(5.6) 15(3.3) 13(9.9) 年龄 平均年龄(标准差) 4.7(3.5) 4.8(3.4) 3.4(3.8) 中位数 4 4 2 给药途径 口服 493(48.1) 247(53.7) 35(26.7) 注射 165(16.1) 5(1.1) 6(4.6) 胎盘/母乳 12(1.2) 6(1.3) 3(2.3) 未知 354(34.6) 202(43.9) 87(66.4) AE结局 死亡 55(5.1) 12(2.3) 14(8.8) 危及生命 69(6.4) 23(4.4) 11(6.9) 残疾 19(1.8) 22(4.2) 5(3.1) 出生缺陷 4(0.4) 3(0.6) 2(1.3) 住院 303(28.2) 179(34.5) 62(38.8) 需要干预防止永久损伤 3(0.3) 1(0.2) 4(2.5) 其他严重AE 620(57.8) 279(53.8) 62(38.8) 3种药品AE报告中男女报告数比例不同,阿奇霉素、红霉素的男生报告数多于女生,克拉霉素的女生报告数多于男生。在已知给药途径中,三者均是口服给药报告数最多。在报告的AE结局中,阿奇霉素和克拉霉素以其他严重AE为主,红霉素则是以住院和其他严重AE为主见表1。阿奇霉素、克拉霉素和红霉素AE报告数及占比见表2。
表 2 阿奇霉素、克拉霉素、红霉素AE报告数前5的国家例数与占比[n(%)]
阿奇霉素 克拉霉素 红霉素 美国 312(30.5) 英国 133(28.9) 英国 46(35.1) 中国 286(27.9) 意大利 52(11.3) 美国 39(29.8) 意大利 45(4.4) 美国 51(11.1) 日本 8(6.1) 日本 39(3.8) 法国 27(5.9) 中国 4(3.0) 西班牙 25(2.4) 日本 20(4.3) 比利时 4(3.0) -
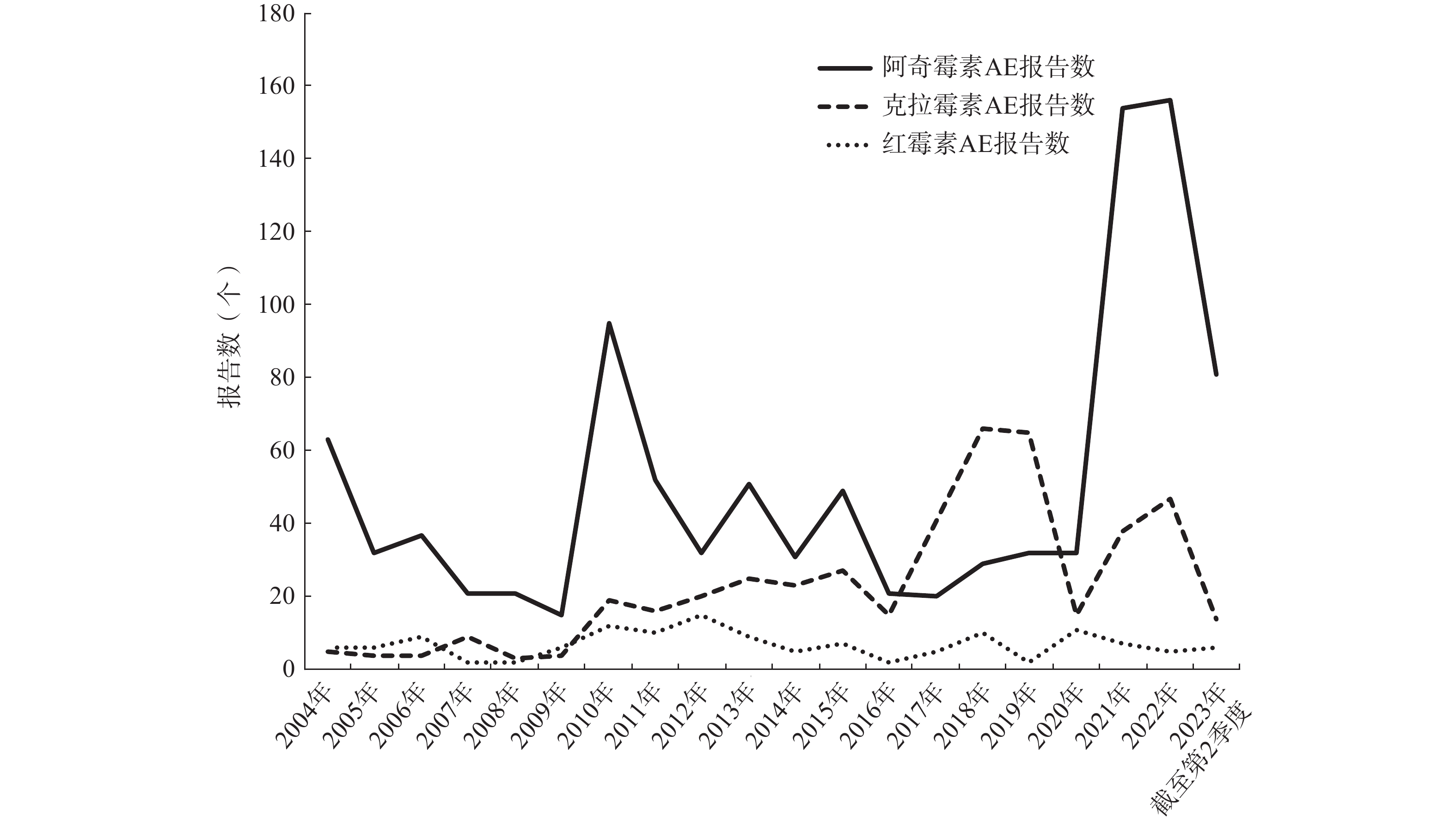
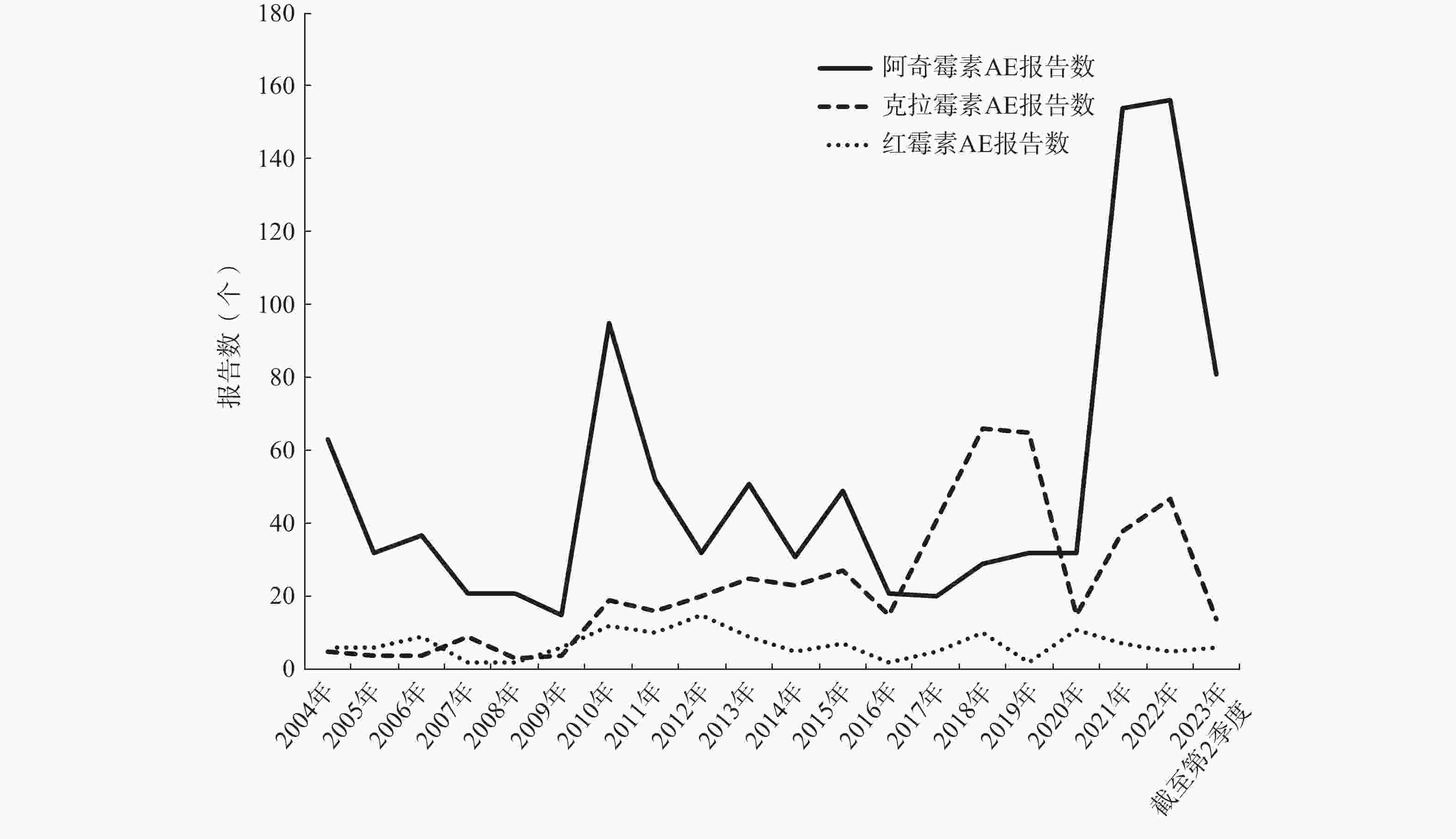
儿童使用阿奇霉素、克拉霉素、红霉素AE报告数随时间的变化趋势如图1所示。在2004−2023年期间,从2004年开始,阿奇霉素AE报告数上下波动,2020年、2021年报告数激增,超过150例。克拉霉素AE报告数呈现缓慢上升趋势,2018年、2019年报告数激增,超过60例。红霉素AE报告数普遍较少,年报告数不超过15例。
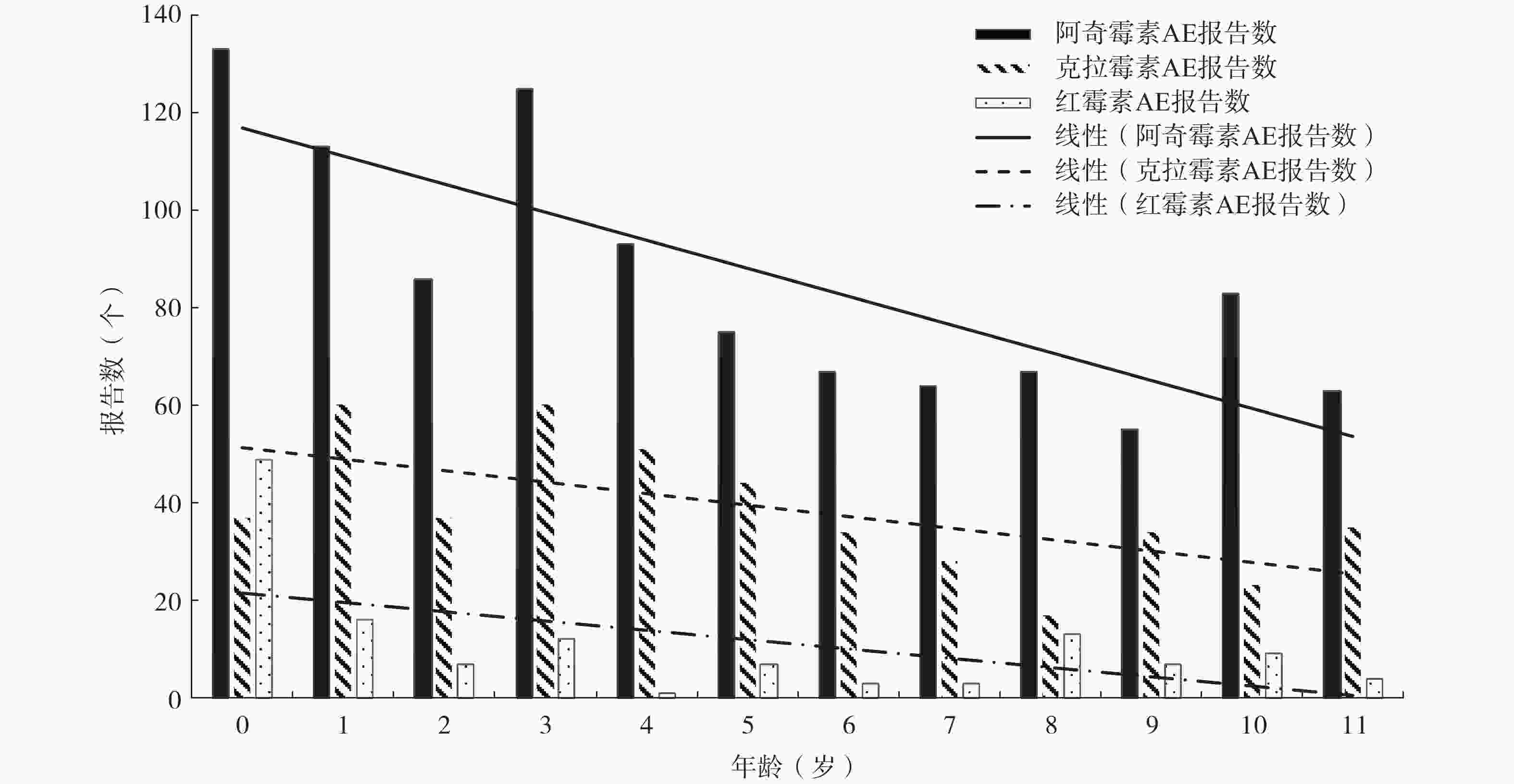
阿奇霉素、克拉霉素、红霉素儿童不同年龄的AE报告数如图2所示。三者AE报告数随年龄增长呈下降趋势,0~3岁报告数较多。
-
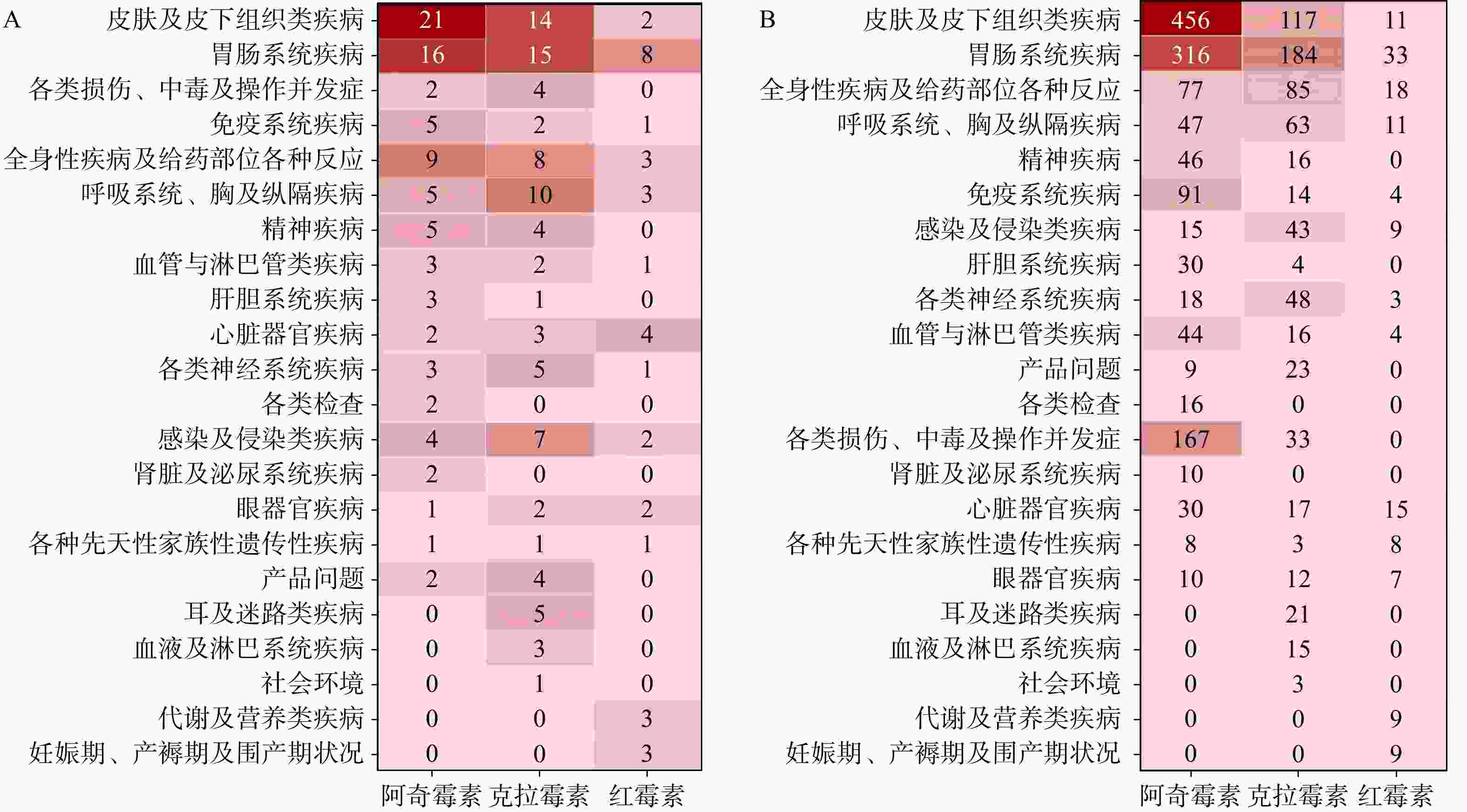
采用ROR法和BCPNN法检测SOC和PT级的AE信号,儿童使用阿奇霉素、克拉霉素、红霉素相关的SOC如图3所示。
克拉霉素信号数(n=91)高于阿奇霉素(n=86)、红霉素(n=34)。在SOC水平中,阿奇霉素AE信号涉及17个SOC,主要集中在皮肤及皮下组织类疾病(n=21)、胃肠系统疾病(n=16)、全身性疾病及给药部位各种反应(n=9)。克拉霉素AE信号涉及18个SOC,主要集中在胃肠系统疾病(n=15)、皮肤及皮下组织类疾病(n=14)、呼吸系统、胸及纵隔疾病(n=10)。红霉素AE信号涉及13个SOC,主要集中在胃肠系统疾病(n=8)、心脏器官疾病(n=4)。在肾脏及泌尿系统疾病SOC中,只有阿奇霉素检出信号;在耳及迷路类疾病、血液及淋巴系统疾病中,只有克拉霉素检出信号;在代谢及营养类疾病和妊娠期、产褥期及围产期状况中SOC,只有红霉素检出信号。
阿奇霉素AE报告1 390份,主要报告为皮肤及皮下组织类疾病(n=456)。克拉霉素AE报告717份,主要报告为胃肠系统疾病(n=184)。红霉素AE报告141份,主要报告为胃肠系统疾病(n=33)。
在PT水平上检测出的强及中强AE信号如表3所示。
表 3 阿奇霉素、克拉霉素、红霉素检测出的强及中强AE信号
排序 PT SOC 频数 ROR IC-2SD 说明书是否收录 阿奇霉素 1 红斑性发疹 皮肤及皮下组织类疾病 45 14.2 2.9 是 2 转变障碍 精神病类 17 35.7 2.7 否 3 史蒂文斯-约翰逊综合征 皮肤及皮下组织类疾病 34 8.8 2.3 是 4 瘙痒 皮肤及皮下组织类疾病 70 7.1 2.2 是 5 药物诱导的肝损伤 肝胆系统疾病 17 13.1 2.2 是 6 药物性超敏反应 免疫系统疾病 38 7.2 2.1 是 7 药疹 皮肤及皮下组织类疾病 13 13.0 1.9 是 8 荨麻疹 皮肤及皮下组织类疾病 66 5.4 1.9 是 9 皮疹 皮肤及皮下组织类疾病 96 5.0 1.8 是 10 粪便变色 胃肠系统疾病 11 11.7 1.7 否 11 幼儿呕吐 胃肠系统疾病 8 26.6 1.6 是 12 幽门狭窄 各种先天性家族性遗传性疾病 8 18.0 1.5 是 13 斑丘疹 皮肤及皮下组织类疾病 17 6.2 1.5 否 克拉霉素 1 产品味道异常 产品问题 14 23.0 2.4 否 2 口腔不适 胃肠系统疾病 11 53.1 2.3 否 3 唇部肿胀 胃肠系统疾病 15 14.8 2.2 否 4 平衡疾病 各类神经系统疾病 12 15.1 2.0 否 5 中毒性表皮坏死松解症 皮肤及皮下组织类疾病 13 10.0 1.8 是 6 发声困难 呼吸系统、胸及纵隔疾病 9 18.7 1.8 否 7 头晕 各类神经系统疾病 19 6.4 1.6 是 8 味觉倒错 各类神经系统疾病 9 13.7 1.6 是 9 咽喉刺激 呼吸系统、胸及纵隔疾病 8 14.5 1.5 否 红霉素 1 急性全身发疹性脓包性皮病 皮肤及皮下组织类疾病 8 101.4 1.9 是 2 幽门狭窄 各种先天性家族性遗传性疾病 8 149.7 1.9 是 超说明书使用(n=151)、呕吐(n=59)、药物相互作用(n=9)分别在阿奇霉素、克拉霉素、红霉素中报告最多。红斑性发疹(IC-2SD=2.88)、转变障碍(IC-2SD=2.66)、史蒂文斯-约翰逊综合征(IC-2SD=2.25)在阿奇霉素AE中信号较强。产品味道异常(IC-2SD=2.36)、口腔不适(IC-2SD=2.28)、唇部肿胀(IC-2SD=2.17)在克拉霉素AE中信号较强。急性全身发疹性脓包性皮病(IC-2SD=1.92)、幽门狭窄(IC-2SD=1.91)在红霉素AE中信号较强。
在儿童中,有2个中强信号未在阿奇霉素说明书中明确收录,包括转变障碍、斑丘疹等。有6个中强信号未在克拉霉素说明书中明确收录,包括产品味道异常、口腔不适、唇部肿胀、平衡疾病、发生困难、咽喉刺激等。
-
本研究采用ROR法和BCPNN法进行阿奇霉素、克拉霉素、红霉素AE信号挖掘,进而评估对比其在儿童中的用药安全性。
-
报告性别方面,阿奇霉素和红霉素男性儿童比女性儿童AE报告数多,克拉霉素女性儿童比男性儿童AE报告数多。目前,大环内酯类抗菌药物在儿童中发生不良反应是否有性别特异性还未见相关研究,本文样本量较小,与大环内酯类抗菌药物AE的影响因素的结论仍需要通过更大规模的研究或临床试验进一步验证。
报告年龄方面,3种药品AE报告平均年龄都小于5岁,红霉素AE平均报告年龄小于阿奇霉素、克拉霉素,红霉素可能在低龄儿童中风险性更高。0~3岁年龄段AE报告数较多,这可能是因低龄儿童身体正处于发育阶段,易受多种因素的影响使得不良反应发生率较高[13]。各地区肺炎支原体诊疗指南中建议:在怀疑非典型肺炎的情况下,对5岁以上儿童使用大环内酯类药物[1,14-15]。应严格控制≤3岁儿童大环内酯类抗生素的使用频率,减少红霉素在低龄儿童中的使用,必须警惕并监控AE。
从AE报告数分布来看,阿奇霉素更多,且AE累及系统更集中,克拉霉素相对于阿奇霉素的AE报告数较少, 但其所累及系统最多,AE信号最多,红霉素累及系统最少,AE信号数也最少。这可能与临床中使用频率不同有关,临床中优先选择阿奇霉素,其次是红霉素或克拉霉素。也有研究表明阿奇霉素不良反应所涉及的系统更加集中,其不良反应多于克拉霉素,克拉霉素相对于阿奇霉素的临床症状较少,但其所涉及的系统较广泛,这与既往研究结果一致[16-17]。有研究表明,阿奇霉素和克拉霉素比红霉素更稳定,耐受性更好[18]。
-
在皮肤及皮下组织类疾病SOC中,阿奇霉素信号比克拉霉素、红霉素多且强,显现出阿奇霉素更容易发生皮肤类AE,明显多于克拉霉素、红霉素,症状主要为各类皮疹,AE较为集中,研究结果与说明书基本一致[19]。Shaeer等人的研究曾报道阿奇霉素会引起各种反应,包括超敏反应、斑丘疹和严重的皮肤反应[20]。皮肤反应与超敏反应密切相关,其中皮疹是最常见的超敏反应,还包括荨麻疹、血管性水肿、斑丘疹或不明皮疹[21-23]。Barni等人回顾性分析发现,在儿童中,阿奇霉素比克拉霉素更易致敏,阿奇霉素可能引起更多的超敏反应[24]。
此外,在肝胆系统疾病SOC中,阿奇霉素的信号多于克拉霉素。在阿奇霉素中检测出一个有关肝损伤的中强信号(药物诱导的肝损伤)。肝脏是清除阿奇霉素的主要途径,患儿长时间使用阿奇霉素会增加肝脏负担,对于肝病显著的患者,阿奇霉素应慎重使用[25]。
胃肠系统疾病的强弱信号分布不同,阿奇霉素中强以上信号主要为粪便变色与幼儿呕吐,主要与胃肠疾病有关(腹泻、腹痛、腹部不适等);克拉霉素中强以上信号主要为口腔不适与唇部肿胀,主要与口腔部位相关(口腔不适、肿舌、口腔疼痛等);红霉素无中强以上信号,其信号主要与胃肠疾病有关。呕吐(n=59)在克拉霉素中报告最多,研究结果与说明书中的AE基本一致[26]。产品味道异常在克拉霉素AE中信号强度最强。克拉霉素具有强烈的苦味,其产品味道会影响患者的依从性[27]。
在各类神经系统疾病和呼吸系统、胸及纵隔疾病SOC中,克拉霉素的信号多于阿奇霉素。克拉霉素信号以平衡疾病、头晕、味觉倒错为主。克拉霉素的罕见神经精神后遗症已有报道,研究发现服用克拉霉素可能出现神经系统副作用,且药物相互作用是神经毒性的重要潜在原因[28-34]。此外,发声困难也是克拉霉素的中强信号,且未在说明书中收录,在临床实践中应加强对此类事件的监测。
建议临床治疗儿童MPP应考虑药物在不同系统的风险性,个体化给药。对药品说明书上未标明的药物AE,要持续监测AE。
本研究基于FAERS数据库仍存在一些局限:①FAERS数据库存在漏报、错报、误报且信息不完整、数据不规范等固有问题[35],影响分析结果。②数据主要来源是欧美地区,我国患儿相关数据相对不足,且研究中红霉素数据量少,用于指导我国儿童临床用药的适用性存在局限。③信号检测结果仅代表AE与药品存在统计学联系,可为后续研究提供方向,判断必然的因果关系仍需进一步研究证实。
-
阿奇霉素有关皮肤及皮下组织类疾病、免疫系统疾病、肝胆系统疾病和精神病类等相关AE的风险性高于克拉霉素与红霉素。克拉霉素有关胃肠系统、各类神经系统和呼吸系统等相关AE的风险性高于阿奇霉素。红霉素有关心脏器官疾病方面等相关AE的风险性高于阿奇霉素和克拉霉素。临床治疗时应考虑药物在不同系统的风险性,个体化给药。
Signal mining of adverse reactions associated with macrolide antibiotics in pediatric patients based on the FAERS database
-
摘要:
目的 挖掘儿童使用大环内酯类药物(阿奇霉素、克拉霉素与红霉素)的不良事件(adverse event,AE)信号,为临床安全用药提供参考。 方法 从美国FDA不良事件报告系统(FAERS)数据库中提取2004年第1季度至2023年第2季度12岁以下儿童数据,采用报告比值比法(reporting odds ratio,ROR)和贝叶斯置信区间递进神经网络法(Bayesian confidence propagation neural network,BCPNN)对3种大环内酯类药物进行AE信号挖掘,重点分析对比3种药物的AE差异。 结果 FAERS数据库共检索到12岁以下儿童的报告1 615份,其中,阿奇霉素1 024份、克拉霉素460份、红霉素131份。阿奇霉素、红霉素中男生报告数多于女生,克拉霉素女生报告数多于男生。在已知给药途径中,三者均是口服给药报告数最多。在报告的AE结局中,阿奇霉素和克拉霉素以其他严重AE为主,红霉素则是以住院和其他严重AE为主。三者AE报告数随年龄增长呈下降趋势,0~3岁报告数较多。经ROR法和BCPNN法信号检测,阿奇霉素风险信号86个,克拉霉素风险信号91个,红霉素风险信号34个。信号累及22个系统器官分类(system organ class,SOC);阿奇霉素主要集中在皮肤及皮下组织类疾病(n=21);克拉霉素主要集中在胃肠系统疾病(n=15);红霉素主要集中在胃肠系统疾病(n=8)。检测到中强及以上风险信号24个,阿奇霉素13个、克拉霉素9个、红霉素2个。 结论 3种药物所致AE不同,不同系统风险性不同。临床治疗儿童肺炎支原体肺炎等应考虑药物在不同系统的风险性,进行个体化给药。 Abstract:Objective To explore the adverse event signals of children using macrolide drugs (azithromycin, clarithromycin, and erythromycin), and provide reference for rational medicine use in clinical practice. Methods Data from children under 12 years old were extracted from the US FAERS database spanning from the first quarter of 2004 to the second quarter of 2023. The adverse drug reaction (ADR) signal mining for three macrolide antibiotics was conducted using the Reporting Odds Ratio (ROR) and Bayesian Confidence Propagation Neural Network (BCPNN) methods. Special emphasis was placed on analyzing and contrasting the differences in adverse events among the three drugs. Results A total of 1 615 reports for children under 12 years old were retrieved from the FAERS database, including 1 024 reports of azithromycin, 460 reports of clarithromycin, and 131 reports of erythromycin. Among azithromycin and erythromycin, there were more reports from boys than girls, while for clarithromycin, there were more reports from girls than boys. Oral administration was the most common route of administration for all three drugs. Regarding the outcome of adverse events reported, azithromycin and clarithromycin were primarily associated with other serious adverse events, whereas erythromycin was mainly associated with hospitalization and other serious adverse events. The number of adverse events reported decreased with increasing age, with a higher number of reports in the 0-3 age group. Using the ROR and BCPNN methods for signal detection, 86 signals were identified for azithromycin, 91 for clarithromycin, and 34 for erythromycin. These signals involved 22 System Organ Classes (SOCs), with azithromycin mainly concentrated in skin and subcutaneous tissue disorders (n=21), clarithromycin in gastrointestinal disorders (n=15), and erythromycin in gastrointestinal disorders (n=8). Twenty-four signals of moderate to high risk were detected, with 13 for azithromycin, 9 for clarithromycin, and 2 for erythromycin. Conclusion The adverse events induced by the three drugs with different risks in different systems. When clinically treating Mycoplasma pneumoniae pneumonia in children, the risk profiles of drugs in different systems should be considered, and personalized dosing should be implemented. -
Key words:
- azithromycin /
- clarithromycin /
- erythromycin /
- FAERS /
- adverse events /
- data mining
-
表 1 使用阿奇霉素、克拉霉素、红霉素的儿童人口学特征及AE结局[n(%)]
阿奇霉素 克拉霉素 红霉素 性别 男 530(51.8) 204(44.3) 69(52.7) 女 436(42.6) 241(52.4) 49(37.4) 未填写 58(5.6) 15(3.3) 13(9.9) 年龄 平均年龄(标准差) 4.7(3.5) 4.8(3.4) 3.4(3.8) 中位数 4 4 2 给药途径 口服 493(48.1) 247(53.7) 35(26.7) 注射 165(16.1) 5(1.1) 6(4.6) 胎盘/母乳 12(1.2) 6(1.3) 3(2.3) 未知 354(34.6) 202(43.9) 87(66.4) AE结局 死亡 55(5.1) 12(2.3) 14(8.8) 危及生命 69(6.4) 23(4.4) 11(6.9) 残疾 19(1.8) 22(4.2) 5(3.1) 出生缺陷 4(0.4) 3(0.6) 2(1.3) 住院 303(28.2) 179(34.5) 62(38.8) 需要干预防止永久损伤 3(0.3) 1(0.2) 4(2.5) 其他严重AE 620(57.8) 279(53.8) 62(38.8) 表 2 阿奇霉素、克拉霉素、红霉素AE报告数前5的国家例数与占比[n(%)]
阿奇霉素 克拉霉素 红霉素 美国 312(30.5) 英国 133(28.9) 英国 46(35.1) 中国 286(27.9) 意大利 52(11.3) 美国 39(29.8) 意大利 45(4.4) 美国 51(11.1) 日本 8(6.1) 日本 39(3.8) 法国 27(5.9) 中国 4(3.0) 西班牙 25(2.4) 日本 20(4.3) 比利时 4(3.0) 表 3 阿奇霉素、克拉霉素、红霉素检测出的强及中强AE信号
排序 PT SOC 频数 ROR IC-2SD 说明书是否收录 阿奇霉素 1 红斑性发疹 皮肤及皮下组织类疾病 45 14.2 2.9 是 2 转变障碍 精神病类 17 35.7 2.7 否 3 史蒂文斯-约翰逊综合征 皮肤及皮下组织类疾病 34 8.8 2.3 是 4 瘙痒 皮肤及皮下组织类疾病 70 7.1 2.2 是 5 药物诱导的肝损伤 肝胆系统疾病 17 13.1 2.2 是 6 药物性超敏反应 免疫系统疾病 38 7.2 2.1 是 7 药疹 皮肤及皮下组织类疾病 13 13.0 1.9 是 8 荨麻疹 皮肤及皮下组织类疾病 66 5.4 1.9 是 9 皮疹 皮肤及皮下组织类疾病 96 5.0 1.8 是 10 粪便变色 胃肠系统疾病 11 11.7 1.7 否 11 幼儿呕吐 胃肠系统疾病 8 26.6 1.6 是 12 幽门狭窄 各种先天性家族性遗传性疾病 8 18.0 1.5 是 13 斑丘疹 皮肤及皮下组织类疾病 17 6.2 1.5 否 克拉霉素 1 产品味道异常 产品问题 14 23.0 2.4 否 2 口腔不适 胃肠系统疾病 11 53.1 2.3 否 3 唇部肿胀 胃肠系统疾病 15 14.8 2.2 否 4 平衡疾病 各类神经系统疾病 12 15.1 2.0 否 5 中毒性表皮坏死松解症 皮肤及皮下组织类疾病 13 10.0 1.8 是 6 发声困难 呼吸系统、胸及纵隔疾病 9 18.7 1.8 否 7 头晕 各类神经系统疾病 19 6.4 1.6 是 8 味觉倒错 各类神经系统疾病 9 13.7 1.6 是 9 咽喉刺激 呼吸系统、胸及纵隔疾病 8 14.5 1.5 否 红霉素 1 急性全身发疹性脓包性皮病 皮肤及皮下组织类疾病 8 101.4 1.9 是 2 幽门狭窄 各种先天性家族性遗传性疾病 8 149.7 1.9 是 -
[1] 国家卫生健康委员会. 儿童肺炎支原体肺炎诊疗指南(2023年版)[J]. 传染病信息, 2023, 36(4): 291-297. doi: 10.3969/j.issn.1007-8134.2023.04.002 [2] 范志诚, 戴红臣. 阿奇霉素和红霉素用于肺炎支原体感染患儿的临床分析[J/OL]. 中华肺部疾病杂志(电子版), 2023, 16(3): 385-387. [3] 林莉, 狄天伟, 杨爱娟, 等. 儿童肺炎支原体感染流行病学特征分析[J]. 中国病原生物学杂志, 2023, 18(11): 1333-1336. [4] 刘雪. 大环内酯类药物治疗小儿支原体感染的药学分析[J]. 名医, 2023(10): 156-158. doi: 10.3969/j.issn.1674-9561.mingy202310054 [5] EDWARDS B J, BUNTA A D, LANE J, et al. Bisphosphonates and nonhealing femoral fractures: analysis of the FDA adverse event reporting system(FAERS)and international safety efforts: a systematic review from the research on adverse drug events and reports(RADAR)project[J]. J Bone Joint Surg Am, 2013, 95(4): 297-307. doi: 10.2106/JBJS.K.01181 [6] ALATAWI Y M, HANSEN R A. Empirical estimation of under-reporting in the U. S. food and drug administration adverse event reporting system (FAERS)[J]. Expert Opin Drug Saf, 2017, 16(7): 761-767. doi: 10.1080/14740338.2017.1323867 [7] BROWN E G. Using MedDRA: implications for risk management[J]. Drug Saf, 2004, 27(8): 591-602. doi: 10.2165/00002018-200427080-00010 [8] ROTHMAN K J, LANES S, SACKS S T. The reporting odds ratio and its advantages over the proportional reporting ratio[J]. Pharmacoepidemiol Drug Saf, 2004, 13(8): 519-523. doi: 10.1002/pds.1001 [9] EVANS S J, WALLER P C, DAVIS S. Use of proportional reporting ratios(PRRs)for signal generation from spontaneous adverse drug reaction reports[J]. Pharmacoepidemiol Drug Saf, 2001, 10(6): 483-486. doi: 10.1002/pds.677 [10] BATE A, LINDQUIST M, EDWARDS I R, et al. A Bayesian neural network method for adverse drug reaction signal generation[J]. Eur J Clin Pharmacol, 1998, 54(4): 315-321. doi: 10.1007/s002280050466 [11] DUMOUCHEL W. Bayesian data mining in large frequency tables, with an application to the FDA spontaneous reporting system[J]. Am Stat, 1999, 53(3): 177-190. doi: 10.1080/00031305.1999.10474456 [12] 马攀, 龚莉, 张妮, 等. 基于FDA不良事件数据库对洛匹那韦/利托那韦安全信号的检测与分析[J]. 中国现代应用药学, 2020, 37(4): 406-413. [13] 鲁晴, 王伟明. 抗Hp感染中克拉霉素致药物性口炎1例[J]. 中国民族民间医药, 2016, 25(5): 40. doi: 10.3969/j.issn.1007-8517.2016.5.zgmzmjyyzz201605019 [14] WAITES K B, TALKINGTON D F. Mycoplasma pneumoniae and its role as a human pathogen[J]. Clin Microbiol Rev, 2004, 17(4): 697-728. [15] USONIS V, IVASKEVICIUS R, DIEZ-DOMINGO J, et al. Comparison between diagnosis and treatment of community-acquired pneumonia in children in various medical centres across Europe with the United States, United Kingdom and the World Health Organization guidelines[J]. Pneumonia (Nathan), 2016, 8: 5. doi: 10.1186/s41479-016-0005-y [16] 王家满, 韩琼. 克拉霉素、阿奇霉素药物不良反应的分析[J]. 中国现代药物应用, 2015, 9(1): 92-93. [17] 黄开华. 万载县株潭中心卫生院门诊患者阿奇霉素与克拉霉素临床用药情况分析[J]. 临床合理用药杂志, 2019, 12(12): 122-123. [18] ALVAREZ-ELCORO S, ENZLER M J. The macrolides: erythromycin, clarithromycin, and azithromycin[J]. Mayo Clin Proc, 1999, 74(6): 613-634. doi: 10.4065/74.6.613 [19] 辉瑞制药科技有限公司. 阿奇霉素片说明书[EB/OL].(2022-05-31) [2024-02-22]. https://labeling.pfizer.com/ShowLabeling.aspx?id=14475. [20] SHAEER K M, CHAHINE E B, VARGHESE GUPTA S, et al. Macrolide allergic reactions[J]. Pharmacy, 2019, 7(3): 135. [21] BENAHMED S, SCARAMUZZA C, MESSAAD D, et al. The accuracy of the diagnosis of suspected macrolide antibiotic hypersensitivity: results of a single-blinded trial[J]. Allergy, 2004, 59(10): 1130-1133. doi: 10.1111/j.1398-9995.2004.00638.x [22] MORI F, PECORARI L, PANTANO S, et al. Azithromycin anaphylaxis in children[J]. Int J Immunopathol Pharmacol, 2014, 27(1): 121-126. doi: 10.1177/039463201402700116 [23] ARAÚJO L, DEMOLY P. Macrolides allergy[J]. Curr Pharm Des, 2008, 14(27): 2840-2862. doi: 10.2174/138161208786369812 [24] BARNI S, BUTTI D, MORI F, et al. Azithromycin is more allergenic than clarithromycin in children with suspected hypersensitivity reaction to macrolides[J]. J Investig Allergol Clin Immunol, 2015, 25(2): 128-132. [25] 陈煜. 阿奇霉素和克拉霉素治疗患者药物不良反应的临床分析[J]. 北方药学, 2020, 17(7): 186-187. doi: 10.3969/j.issn.1672-8351.2020.07.138 [26] 上海雅培制药有限公司. 克拉霉素片说明书[EB/OL]. (2017-10-19) [2024-02-22]. https://labeling.pfizer.com/ShowLabeling.aspxid=14475. [27] NTEMI P V, WALKER R B, KHAMANGA S M. Design, evaluation and optimization of taste masked clarithromycin powder[J]. Pharmazie, 2019, 74(12): 721-727. [28] YOUNG M J, CAPLAN R A, CONNOLLY I, et al. Closed-eye visual hallucinations associated with clarithromycin[J]. J Neuropsychiatry Clin Neurosci, 2021, 33(3): 230-232. doi: 10.1176/appi.neuropsych.20100253 [29] BANDETTINI DI POGGIO M, ANFOSSO S, AUDENINO D, et al. Clarithromycin-induced neurotoxicity in adults[J]. J Clin Neurosci, 2011, 18(3): 313-318. doi: 10.1016/j.jocn.2010.08.014 [30] YASUI N, OTANI K, KANEKO S, et al. Carbamazepine toxicity induced by clarithromycin coadministration in psychiatric patients[J]. Int Clin Psychopharmacol, 1997, 12(4): 225-229. doi: 10.1097/00004850-199707000-00007 [31] GÉLISSE P, HILLAIRE-BUYS D, HALAILI E, et al. Carbamazepine and clarithromycin: a clinically relevant drug interaction[J]. Rev Neurol, 2007, 163(11): 1096-1099. doi: 10.1016/S0035-3787(07)74183-8 [32] POLLAK P T, SKETRIS I S, MACKENZIE S L, et al. Delirium probably induced by clarithromycin in a patient receiving fluoxetine[J]. Ann Pharmacother, 1995, 29(5): 486-488. doi: 10.1177/106002809502900506 [33] JABER B L, LOBON L F, MADIAS N E. The serotonin syndrome complicating co-prescription of paroxetine and clarithromycin[J]. Am J Med, 2006, 119(4): e3. doi: 10.1016/j.amjmed.2005.05.022 [34] PRIME K, FRENCH P. Neuropsychiatric reaction induced by clarithromycin in a patient on highly active antiretroviral therapy(HAART)[J]. Sex Transm Infect, 2001, 77(4): 297-298. doi: 10.1136/sti.77.4.297 [35] SAKAEDA T, TAMON A, KADOYAMA K, et al. Data mining of the public version of the FDA adverse event reporting system[J]. Int J Med Sci, 2013, 10(7): 796-803. doi: 10.7150/ijms.6048 -




 下载:
下载: