-
硝苯地平常用于高血压患者,也因其显著的疗效被广泛应用于高血压孕妇[1-2]。现有的研究多是评价硝苯地平的临床疗效,对其安全性评估较少[3]。尽管一些研究表明硝苯地平在高血压孕妇中具有一定的安全性[4-5],但也有研究表明硝苯地平会引起头痛和外周性水肿等不良事件[6],因此,系统评价硝苯地平在高血压孕妇中的安全性具有十分重要的临床价值。
本研究基于真实世界数据,系统评价了硝苯地平在高血压孕妇中的药物毒性,并挖掘了相关不良事件信号,旨在为临床安全用药提供参考。
-
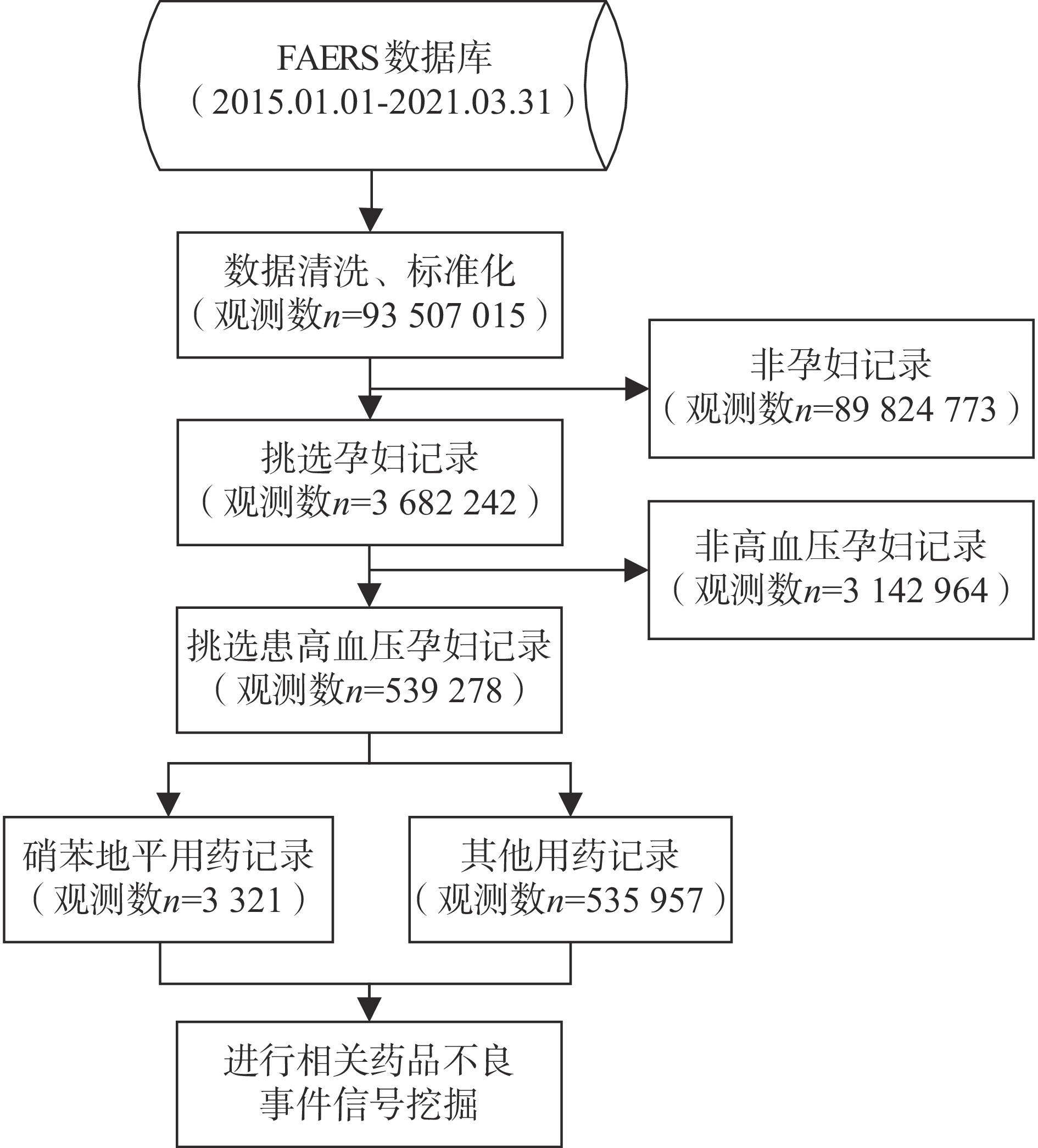
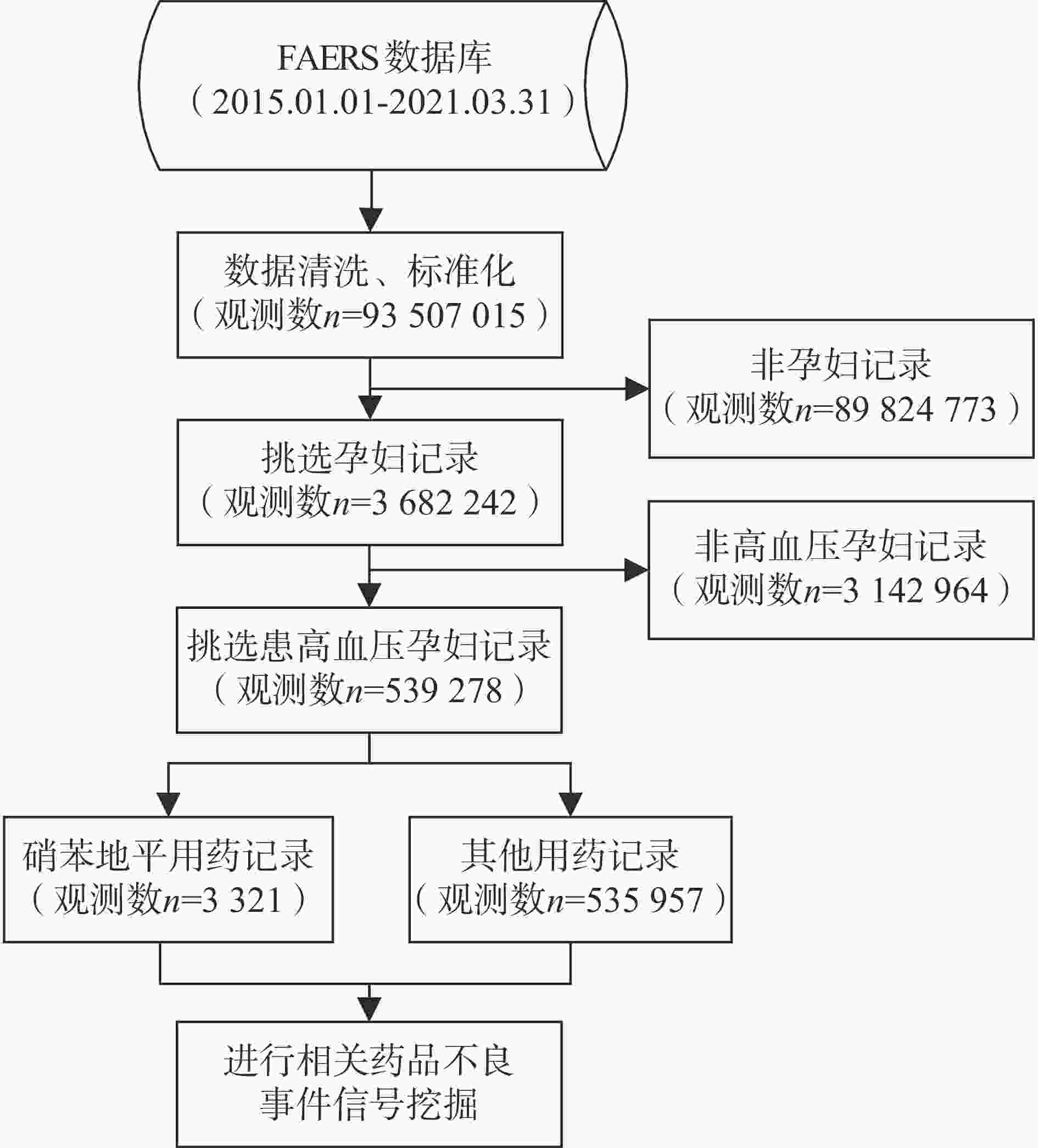
本研究数据来源于美国食品药品监督管理局的不良事件报告系统(FAERS)数据库2015年1月1日至2021年3月31日的数据[7],分步挑选出高血压孕妇相关记录,并对数据开展筛选将其分为硝苯地平用药记录和其他用药记录(简称对照药品),见图1。
-
本研究采用《监管活动医学词典》(MedDRA)24.0中文版和英文版中系统器官分类(SOC)和首选术语(PT)两个等级对药品不良事件进行标准化和汉化[8],文章整体设计和书写参照《基于常规收集健康数据的观察性研究报告规范》(RECORD)[9]。
-
本研究采用不相称测定分析法进行信号挖掘,包括信息成分法(IC)和报告比值法(ROR)[10-11]。当IC法95%置信区间下限IC025高于0或ROR法的95%置信区间下限ROR025大于1时提示该信号为阳性信号。本研究仅对相关药品不良事件频数≥3的不良事件进行信号挖掘,所有分析均采用MedDRA24.0 版本和SAS 9.4 版本完成。
-
FAERS数据库中服用硝苯地平和未服用硝苯地平的高血压孕妇记录基线情况和不良反应结局见表1。对于高血压孕妇,服用硝苯地平的不良事件记录多处在20~40岁(49.59%)年龄段,进一步分析发现25~27岁(23.87%)和35~37岁(14.75%)年龄段的人群所占比重较大,未服用硝苯地平不良事件记录多处在40~60岁(45.85%)年龄段。在2018至2021年,两组不良事件记录均呈现快速上升趋势。在终点结局中,“其他严重事件”和“住院”在服用和未服用硝苯地平组均为主要终点结局事件。
表 1 服用和未服用硝苯地平的高血压孕妇的基线情况及不良反应结局比较
特征 服用硝苯地平组
例数(%)
[n=3 321(0.62%)]未服用硝苯地平组
例数(%)
[n=535 957(99.38%)]年龄(岁) <20 129(3.88) 21 063(3.93) 20~40 1 647(49.59) 79 547(14.84) 40~60 154(4.64) 245 751(45.85) ≥60 2(0.06) 626(0.12) 缺失 1 389(41.82) 188 970(35.26) 年份(年) 2015 125(3.76) 9 010(1.68) 2016 120(3.61) 12 246(2.28) 2017 82(2.47) 19 444(3.63) 2018 290(8.73) 42 604(7.95) 2019 1 019(30.68) 44 907(8.38) 2020 1 417(42.67) 235 271(43.90) 2021Q1* 268(8.07) 172 475(32.18) 终点结局 死亡 97(2.92) 54 908(10.24) 危及生命 160(4.82) 37 359(6.97) 残疾 0(0.00) 45 405(8.47) 住院 644(19.39) 68 979(12.87) 先天异常 183(5.51) 24 614(4.59) 其他严重事件 2 201(66.28) 301 597(56.27) 需要介入以避免
永久损伤的事件0(0.00) 8(0.01) 缺失 36(1.08) 3 087(0.58) *2021年第一季度数据。 -
本研究最终挑选出539 278条高血压孕妇相关记录进行分析。共对102个硝苯地平相关不良事件进行了信号挖掘,共发现70个阳性信号,IC法和ROR法信号挖掘结果基本一致。在各SOC系统分类中,“妊娠期、产褥期及围产期状况”SOC分类阳性不良事件数最多(14/23),见表2。
表 2 硝苯地平不良事件信号按照SOC归类结果
SOC PT 血液及淋巴系统疾病 贫血、血栓性血小板减少性紫癜、血液动力学不稳定、雷诺现象、低血压、血压控制不佳、出血 心脏器官疾病 心动过速、新生儿心律失常、肺动脉瓣狭窄 胃肠系统疾病 舌水肿、口部感觉异常、腹膜出血、腹胀、呕吐、恶心、牙龈肥大 生殖系统及乳腺疾病 阴道出血 肾脏及泌尿系统疾病 氮质血症、蛋白尿、肾功能损害、血尿症、肾盂肾盏扩张、肾病综合征 妊娠期、产褥期及围产期状况 分娩提前、先兆子痫、胎儿生长受限、出生体重偏轻的婴儿、胎儿死亡、小样儿、羊水过多、活产、早产、新生儿黄疸、死产、妊娠高血压、羊水过少、孕产妇病症影响胎儿、胎盘功能不全、溶血、肝酶升高及血小板减少综合征、正常新生儿、自发流产、先兆临产、臀先露、胎盘早剥、胎儿窘迫综合征、胎儿运动减少 全身性疾病及给药部位各种反应 药物无效、病情恶化、耐药、隐匿性症状、药物相互作用、外周水肿 内分泌系统疾病 肾上腺增生 呼吸系统、胸及纵隔疾病 肺水肿、新生儿呼吸窘迫综合征、呼吸困难、呼吸急促、新生儿呼吸急促、新生儿呼吸窘迫、肺性高血压、胸腔积液、呼吸窘迫 各种先天性、家族性、遗传性疾病 动脉导管未闭、多指畸形、房间隔缺损、室间隔缺损 各种手术及医疗操作 剖宫产、机械通气 各种肌肉骨骼及结缔组织疾病 肌无力 各类神经系统疾病 短暂性脑缺血发作、运动障碍、失语、头痛 各类检查 全身血管阻力升高、血压升高、皮质醇增加、结合珠蛋白降低、血小板计数降低、血醛固酮升高、尿游离皮质醇升高、丙氨酸氨基转移酶升高、天门冬氨酸氨基转移酶升高、血促皮质激素减少、血氧饱和度降低、阿氏评分低、血肌酐升高、血红蛋白降低、红细胞计数下降、白细胞计数升高、人绒毛膜促性腺激素阳性、血尿酸升高 感染及侵染类疾病 子宫内膜炎、尿路感染、感染、代谢性酸中毒、高钾血症、低镁血症、体重异常增加、低钾血症 在高血压孕妇中硝苯地平相关的药品不良事件频数方面,分娩提前(IC025=2.87,ROR025=9.52)、先兆子痫(IC025=1.82,ROR025=3.82)和胎儿生长受限(IC025=2.37,ROR025=5.69)等为频数较高的阳性不良事件,见表3。
表 3 高血压孕妇人群中频数前10的硝苯地平相关药品不良事件
排名 MedDRA编码 PT 不良事件例数(例) IC IC025 IC975 ROR ROR025 ROR975 a b c d 1 10036595 分娩提前 738 2 583 14307 521 650 2.99 2.87 3.11 10.35 9.52 11.25 2 10013709 药物无效 63 3 258 8 961 526 996 0.18 −0.24 0.60 1.14 0.88 1.46 3 10036485 先兆子痫 48 3 273 1 471 534 486 2.30 1.82 2.78 5.10 3.82 6.81 4 10070531 胎儿生长受限 42 3 279 811 535 146 2.89 2.37 3.40 7.77 5.69 10.62 5 10067508 出生体重偏轻的婴儿 41 3 280 3 467 532 490 0.91 0.39 1.43 1.90 1.39 2.59 6 10055690 胎儿死亡 41 3 280 492 535 465 3.46 2.93 3.98 11.81 8.57 16.27 7 10041092 小样儿 26 3 295 656 535 301 2.50 1.83 3.16 5.84 3.94 8.65 8 10034130 动脉导管未闭 25 3 296 1 646 534 311 1.24 0.56 1.92 2.39 1.61 3.56 9 10036063 多指畸形 24 3 297 177 535 780 3.82 3.13 4.51 15.42 10.05 23.65 10 10036079 羊水过多 24 3 297 537 535 420 2.63 1.94 3.32 6.44 4.27 9.70 a:高血压孕妇中硝苯地平相关的目标不良事件;b:高血压孕妇中硝苯地平相关的其他药品不良事件;c:高血压孕妇中对照药品相关的目标不良事件;d:高血压孕妇中对照药品相关的其他药品不良事件。 在高血压孕妇中硝苯地平相关的药品不良事件信号强度方面,多指畸形(IC025=3.13,ROR025=10.05)、胎儿死亡(IC025=2.93,ROR025=8.57)和分娩提前(IC025=2.87,ROR025=9.52)等为信号强度较高的阳性不良事件,见表4。
表 4 高血压孕妇人群中信号强度前10的硝苯地平相关药品不良事件
排名 MedDRA编码 PT 不良事件例数(例) IC IC025 IC975 ROR ROR025 ROR975 a b c d 1 10036063 多指畸形 24 3 297 177 535 780 3.82 3.13 4.51 15.42 10.05 23.65 2 10055690 胎儿死亡 41 3 280 492 535 465 3.46 2.93 3.98 11.81 8.57 16.27 3 10036595 分娩提前 738 2 583 14 307 521 650 2.99 2.87 3.11 10.35 9.52 11.25 4 10070531 胎儿生长受限 42 3 279 811 535 146 2.89 2.37 3.40 7.77 5.69 10.62 5 10047107 全身血管阻力升高 15 3 306 170 535 787 3.24 2.35 4.13 10.01 5.90 16.98 6 10011207 皮质醇增加 9 3 312 61 535 896 3.35 2.18 4.53 10.83 5.38 21.83 7 10059866 耐药 15 3 306 209 535 748 3.04 2.16 3.93 8.66 5.12 14.64 8 10021027 低镁血症 8 3 313 48 535 909 3.33 2.08 4.59 10.67 5.04 22.57 9 10018935 腹膜出血 12 3 309 151 535 806 3.06 2.05 4.06 8.73 4.84 15.72 10 10047065 雷诺现象 7 3 314 28 535 929 3.39 2.03 4.75 11.14 4.86 25.52 a:高血压孕妇中硝苯地平相关的目标不良事件;b:高血压孕妇中硝苯地平相关的其他药品不良事件;c:高血压孕妇中对照药品相关的目标不良事件;d:高血压孕妇中对照药品相关的其他药品不良事件。 -
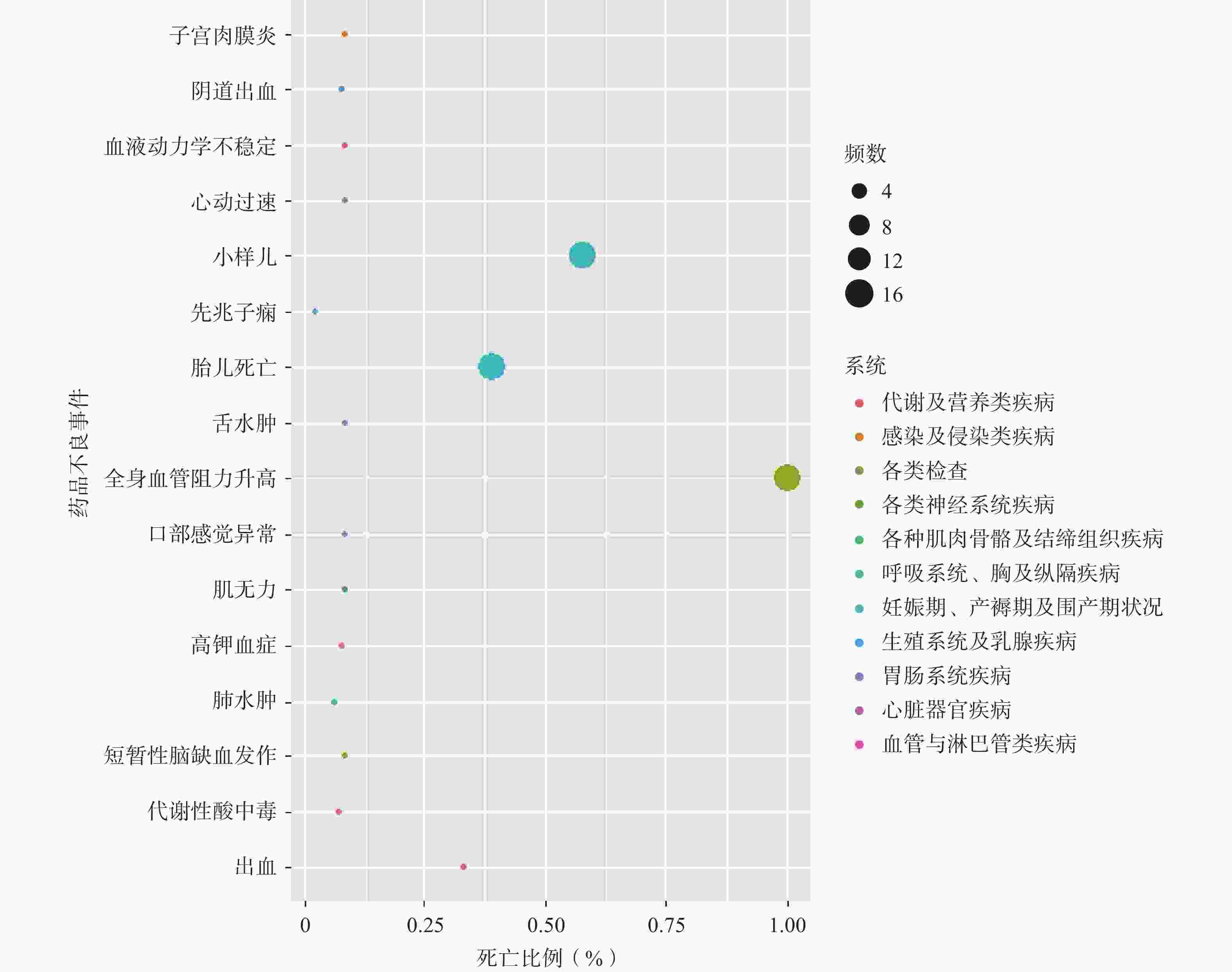
在高血压孕妇人群中硝苯地平相关的药品不良事件死亡比例方面,全身血管阻力升高(100.00%)、小样儿(57.69%)和胎儿死亡(39.02%)等对应的死亡比例和死亡频数均较高,见图2。
-
妊娠期高血压是常见的妊娠期并发症之一,也是导致孕产妇死亡的主要原因之一,严重危害母婴健康,硝苯地平是治疗药物之一。本研究基于2015年1月1日至2021年3月31日FAERS数据库的数据,利用IC和ROR方法对硝苯地平治疗高血压孕妇时潜在不良事件信号进行挖掘。结果显示分娩提前、先兆子痫、胎儿生长受限和出生体重偏轻出现频次较多,多指畸形、胎儿死亡和分娩提前阳性信号强度较高。在高血压孕妇人群中硝苯地平相关的药品不良事件死亡比例方面,全身血管阻力升高、小样儿和胎儿死亡等对应的死亡比例和死亡频数均较高。
分娩提前事件信号频数第1且强度第3,曾有案例报道硝苯地平相关的分娩提前事件[12],发生的可能原因是硝苯地平舒张子宫平滑肌,导致子宫不规则收缩。胎儿生长受限也可能与硝苯地平影响血流供应有关,从而也导致胎儿出生体重偏轻,当然分娩提前也会导致出生胎儿体重偏轻。因此,对于存在早产风险的高血压孕妇,如无禁忌症,可优先选择甲基多巴或拉贝洛尔等安全性较高的药物作为一线降压治疗;若必须使用硝苯地平,应在短期内、低剂量下使用,并密切监测其对子宫收缩及胎儿发育的影响。
先兆子痫事件频数第2,很少有关于高血压孕妇人群硝苯地平相关的先兆子痫的报道,但值得注意的是,高血压常与先兆子痫共同出现,而硝苯地平多用作孕期高血压和先兆子痫的治疗[13-14],因而并不能认为先兆子痫为硝苯地平直接相关的药品不良事件。多指畸形在所有不良信号中强度第1,频数第9。在硝苯地平相关的多指畸形人群记录中,阿司匹林、盐酸拉贝洛尔和奈韦拉平为与硝苯地平联用频率较高的药物,值得注意的是,曾有研究报道小鼠中高剂量阿司匹林相关的多指畸形不良事件[15],多指畸形也未与其他不良事件同时出现,本研究中多指畸形不良事件是否与硝苯地平联用的阿司匹林相关需要后续进一步研究。
胎儿死亡在所有不良信号中强度第2,频数第6,死亡比例第3,有研究表明胎儿死亡与一些严重的不良事件如重度先兆子痫有关[16],本研究进一步分析也发现,胎儿死亡与小样儿、先兆子痫和全身血管阻力升高关系密切,但是否与硝苯地平相关还需研究。
全身血管阻力升高在所有不良信号中死亡比例第1,强度第5,全身血管阻力升高可能多由各种因素相关的血管动力学重建导致[17-18]。进一步分析发现,全身血管阻力升高与胎儿死亡和小样儿等严重不良事件密切相关,但是否与硝苯地平相关仍需进一步研究证实。
小样儿在所有不良信号中死亡比例第2,频数第7。同样,现并无报道高血压孕妇硝苯地平相关的小样儿事件的研究,同时总体关注小样儿的研究本身较少。相关研究显示,胱氨酸氨基肽酶水平波动或与小样儿事件有关[19],进一步研究发现,小样儿与胎儿死亡和全身血管阻力升高等死亡比例前3的事件密切相关,但与硝苯地平是否有关联并不确定。考虑到其较高的频数和孕妇死亡比例,医务人员应对疑似硝苯地平相关的小样儿事件给予充分的关注。
本研究尚存在不足之处:①部分变量如年龄和剂量缺失较多,用药时间未知,并且FAERS数据库存在漏报少报等偏倚问题,可能影响不良事件的评估;②IC和ROR法仅仅是一个统计学关联,并不能确定目标药物与不良事件的因果关系。
综上,硝苯地平在高血压孕妇中存在着一定的药物毒性,临床上应加强药学监护,尤其是在使用硝苯地平治疗高血压孕妇时,应建立药物不良反应监测制度,定期评估孕妇的血压、胎动情况、宫缩频率和胎盘功能等指标。若患者出现异常宫缩、胎儿生长迟缓等情况,应及时干预并调整治疗方案;同时,应开展孕期药物使用宣教,提高患者对药品不良反应早期表现的识别能力。为预防早产风险,建议在孕中期及早期对患者进行早产风险筛查,包括宫颈长度评估和胎膜情况检查,必要时可给予孕激素治疗、补充叶酸,并结合心理干预、营养指导等多维措施,提升妊娠结局的安全性。此外,应加强对孕产妇人群的健康宣教工作,提高其对妊娠期高血压和药物使用风险的认识,鼓励孕妇在专业指导下进行规律体检、科学饮食和适度锻炼,避免盲目使用药物或擅自停药行为,从而全面提升用药依从性和治疗效果。
Drug toxicities of nifedipine in pregnant women with hypertension: a real-world study based on FAERS database
-
摘要:
目的 本研究旨在系统评价硝苯地平在高血压孕妇中的药物毒性,为临床安全用药提供参考借鉴。 方法 采用美国食品药品监督管理局的不良事件报告系统(FAERS)数据库2015年1月1日至2021年3月31日报告的药物使用数据,应用信息成分法(IC)和报告比值法(ROR)进行信号挖掘。 结果 最终挑选出539 278条高血压孕妇相关记录进行分析,共发现70个硝苯地平相关阳性不良事件信号。分娩提前(IC025=2.87,ROR025=9.52)、先兆子痫(IC025=1.82,ROR025=3.82)和胎儿生长受限(IC025=2.37,ROR025=5.69)等为频数较高的阳性不良事件。多指畸形(IC025=3.13,ROR025=10.05)、胎儿死亡(IC025=2.93,ROR025=8.57)和分娩提前(IC025=2.87,ROR025=9.52)等为信号强度较高的不良事件。全身血管阻力升高、小样儿和胎儿死亡等不良事件对应的死亡比例较高。 结论 硝苯地平在高血压孕妇中存在着一定的药物毒性,部分频数和死亡比例高的不良事件需要引起医务人员的重视。 Abstract:Objective To systematically evaluate toxicities of nifedipine in pregnant women with hypertension, and provide references for nifedipine’s clinical safety application. Methods Study was conducted with data from US food and drug administration adverse event reporting system(FAERS) database from January 1, 2015, to March 31, 2021. Information component (IC) and reporting odds ratio(ROR)methods were applied for signal mining. Results Finally, a total of 539278 records of pregnant women with hypertension were selected for analysis, and 70 positive adverse drug event signals were detected. Premature delivery (IC025=2.87, ROR025=9.52), pre-eclampsia (IC025=1.82, ROR025=3.82) and fetal growth restriction (IC025=2.37, ROR025=5.69)were positive adverse events with higher frequency. Polydactyly(IC025=3.13, ROR025=10.05), fetal death(IC025=2.93, ROR025=8.57)and premature delivery(IC025=2.87, ROR025=9.52)were positive adverse events with higher intensity. Vascular resistance systemic increased, small for dates baby and fetal death corresponded to higher death rates.Conclusion Nifedipine-associated drug toxicities were detected in pregnant women with hypertension, and some adverse events with high frequency and high death rate were deserved further attention by medical staffs. -
Key words:
- nifedipine /
- information component /
- reporting odds ratio /
- hypertension /
- pregnant women /
- adverse drug events
-
表 1 服用和未服用硝苯地平的高血压孕妇的基线情况及不良反应结局比较
特征 服用硝苯地平组
例数(%)
[n=3 321(0.62%)]未服用硝苯地平组
例数(%)
[n=535 957(99.38%)]年龄(岁) <20 129(3.88) 21 063(3.93) 20~40 1 647(49.59) 79 547(14.84) 40~60 154(4.64) 245 751(45.85) ≥60 2(0.06) 626(0.12) 缺失 1 389(41.82) 188 970(35.26) 年份(年) 2015 125(3.76) 9 010(1.68) 2016 120(3.61) 12 246(2.28) 2017 82(2.47) 19 444(3.63) 2018 290(8.73) 42 604(7.95) 2019 1 019(30.68) 44 907(8.38) 2020 1 417(42.67) 235 271(43.90) 2021Q1* 268(8.07) 172 475(32.18) 终点结局 死亡 97(2.92) 54 908(10.24) 危及生命 160(4.82) 37 359(6.97) 残疾 0(0.00) 45 405(8.47) 住院 644(19.39) 68 979(12.87) 先天异常 183(5.51) 24 614(4.59) 其他严重事件 2 201(66.28) 301 597(56.27) 需要介入以避免
永久损伤的事件0(0.00) 8(0.01) 缺失 36(1.08) 3 087(0.58) *2021年第一季度数据。 表 2 硝苯地平不良事件信号按照SOC归类结果
SOC PT 血液及淋巴系统疾病 贫血、血栓性血小板减少性紫癜、血液动力学不稳定、雷诺现象、低血压、血压控制不佳、出血 心脏器官疾病 心动过速、新生儿心律失常、肺动脉瓣狭窄 胃肠系统疾病 舌水肿、口部感觉异常、腹膜出血、腹胀、呕吐、恶心、牙龈肥大 生殖系统及乳腺疾病 阴道出血 肾脏及泌尿系统疾病 氮质血症、蛋白尿、肾功能损害、血尿症、肾盂肾盏扩张、肾病综合征 妊娠期、产褥期及围产期状况 分娩提前、先兆子痫、胎儿生长受限、出生体重偏轻的婴儿、胎儿死亡、小样儿、羊水过多、活产、早产、新生儿黄疸、死产、妊娠高血压、羊水过少、孕产妇病症影响胎儿、胎盘功能不全、溶血、肝酶升高及血小板减少综合征、正常新生儿、自发流产、先兆临产、臀先露、胎盘早剥、胎儿窘迫综合征、胎儿运动减少 全身性疾病及给药部位各种反应 药物无效、病情恶化、耐药、隐匿性症状、药物相互作用、外周水肿 内分泌系统疾病 肾上腺增生 呼吸系统、胸及纵隔疾病 肺水肿、新生儿呼吸窘迫综合征、呼吸困难、呼吸急促、新生儿呼吸急促、新生儿呼吸窘迫、肺性高血压、胸腔积液、呼吸窘迫 各种先天性、家族性、遗传性疾病 动脉导管未闭、多指畸形、房间隔缺损、室间隔缺损 各种手术及医疗操作 剖宫产、机械通气 各种肌肉骨骼及结缔组织疾病 肌无力 各类神经系统疾病 短暂性脑缺血发作、运动障碍、失语、头痛 各类检查 全身血管阻力升高、血压升高、皮质醇增加、结合珠蛋白降低、血小板计数降低、血醛固酮升高、尿游离皮质醇升高、丙氨酸氨基转移酶升高、天门冬氨酸氨基转移酶升高、血促皮质激素减少、血氧饱和度降低、阿氏评分低、血肌酐升高、血红蛋白降低、红细胞计数下降、白细胞计数升高、人绒毛膜促性腺激素阳性、血尿酸升高 感染及侵染类疾病 子宫内膜炎、尿路感染、感染、代谢性酸中毒、高钾血症、低镁血症、体重异常增加、低钾血症 表 3 高血压孕妇人群中频数前10的硝苯地平相关药品不良事件
排名 MedDRA编码 PT 不良事件例数(例) IC IC025 IC975 ROR ROR025 ROR975 a b c d 1 10036595 分娩提前 738 2 583 14307 521 650 2.99 2.87 3.11 10.35 9.52 11.25 2 10013709 药物无效 63 3 258 8 961 526 996 0.18 −0.24 0.60 1.14 0.88 1.46 3 10036485 先兆子痫 48 3 273 1 471 534 486 2.30 1.82 2.78 5.10 3.82 6.81 4 10070531 胎儿生长受限 42 3 279 811 535 146 2.89 2.37 3.40 7.77 5.69 10.62 5 10067508 出生体重偏轻的婴儿 41 3 280 3 467 532 490 0.91 0.39 1.43 1.90 1.39 2.59 6 10055690 胎儿死亡 41 3 280 492 535 465 3.46 2.93 3.98 11.81 8.57 16.27 7 10041092 小样儿 26 3 295 656 535 301 2.50 1.83 3.16 5.84 3.94 8.65 8 10034130 动脉导管未闭 25 3 296 1 646 534 311 1.24 0.56 1.92 2.39 1.61 3.56 9 10036063 多指畸形 24 3 297 177 535 780 3.82 3.13 4.51 15.42 10.05 23.65 10 10036079 羊水过多 24 3 297 537 535 420 2.63 1.94 3.32 6.44 4.27 9.70 a:高血压孕妇中硝苯地平相关的目标不良事件;b:高血压孕妇中硝苯地平相关的其他药品不良事件;c:高血压孕妇中对照药品相关的目标不良事件;d:高血压孕妇中对照药品相关的其他药品不良事件。 表 4 高血压孕妇人群中信号强度前10的硝苯地平相关药品不良事件
排名 MedDRA编码 PT 不良事件例数(例) IC IC025 IC975 ROR ROR025 ROR975 a b c d 1 10036063 多指畸形 24 3 297 177 535 780 3.82 3.13 4.51 15.42 10.05 23.65 2 10055690 胎儿死亡 41 3 280 492 535 465 3.46 2.93 3.98 11.81 8.57 16.27 3 10036595 分娩提前 738 2 583 14 307 521 650 2.99 2.87 3.11 10.35 9.52 11.25 4 10070531 胎儿生长受限 42 3 279 811 535 146 2.89 2.37 3.40 7.77 5.69 10.62 5 10047107 全身血管阻力升高 15 3 306 170 535 787 3.24 2.35 4.13 10.01 5.90 16.98 6 10011207 皮质醇增加 9 3 312 61 535 896 3.35 2.18 4.53 10.83 5.38 21.83 7 10059866 耐药 15 3 306 209 535 748 3.04 2.16 3.93 8.66 5.12 14.64 8 10021027 低镁血症 8 3 313 48 535 909 3.33 2.08 4.59 10.67 5.04 22.57 9 10018935 腹膜出血 12 3 309 151 535 806 3.06 2.05 4.06 8.73 4.84 15.72 10 10047065 雷诺现象 7 3 314 28 535 929 3.39 2.03 4.75 11.14 4.86 25.52 a:高血压孕妇中硝苯地平相关的目标不良事件;b:高血压孕妇中硝苯地平相关的其他药品不良事件;c:高血压孕妇中对照药品相关的目标不良事件;d:高血压孕妇中对照药品相关的其他药品不良事件。 -
[1] PRATT K, LORDO R, SELF S, et al. Amlodipine versus nifedipine ER for the management of postpartum hypertension: a noninferiority randomized controlled trial[J]. Am J Obstet Gynecol MFM, 2025, 7(1): 101575. doi: 10.1016/j.ajogmf.2024.101575 [2] LEONARD S A, SIADAT S, MAIN E K, et al. Chronic hypertension during pregnancy: prevalence and treatment in the United States,2008-2021[J]. Hypertension, 2024, 81(8): 1716-1723. doi: 10.1161/HYPERTENSIONAHA.124.22731 [3] SANUSI A A, LEACH J, BOGGESS K, et al. Pregnancy outcomes of nifedipine compared with labetalol for oral treatment of mild chronic hypertension[J]. Obstet Gynecol, 2024, 144(1): 126-134. doi: 10.1097/AOG.0000000000005613 [4] ALAVIFARD S, CHASE R, JANOUDI G, et al. First-line antihypertensive treatment for severe hypertension in pregnancy: a systematic review and network meta-analysis[J]. Pregnancy Hypertens, 2019, 18: 179-187. doi: 10.1016/j.preghy.2019.09.019 [5] SHIMAMOTO K, KIMOTO M, MATSUDA Y, et al. Long-term safety and efficacy of high-dose controlled-release nifedipine(80 mg per day)in Japanese patients with essential hypertension[J]. Hypertens Res, 2015, 38(10): 695-700. doi: 10.1038/hr.2015.54 [6] TUNG Y C, HSU T J, LIN C P, et al. Efficacy and safety outcomes of one generic nifedipine versus ADALAT long-acting nifedipine for hypertension management[J]. J Clin Hypertens, 2020, 22(12): 2296-2305. doi: 10.1111/jch.14070 [7] US Food and Drug Administration. How to make a FOIA request [EB/OL]. (2024-01-10) [2024-09-16]. https://www.fda.gov/regulatory-information/freedom-information/how-make-foia-request. [8] Maintenance and Support Services Organization. Support Documentation: MedDRA Version 24.0(English)[EB/OL]. (2021-03)[2021-06-16]. https://www.meddra.org/how-to-use/support-documentation/english. [9] RECORD WORKING COMMITTEE. RECORD Checklist [EB/OL]. (2015) [2021-06-16]. https://www.record-statement.org/checklist.php. [10] VAN PUIJENBROEK E P, BATE A, LEUFKENS H G M, et al. A comparison of measures of disproportionality for signal detection in spontaneous reporting systems for adverse drug reactions[J]. Pharmacoepidemiol Drug Saf, 2002, 11(1): 3-10. doi: 10.1002/pds.668 [11] BATE A, LINDQUIST M, EDWARDS I R, et al. A bayesian neural network method for adverse drug reaction signal generation[J]. Eur J Clin Pharmacol, 1998, 54(4): 315-321. doi: 10.1007/s002280050466 [12] ZHANG X, LIAO H, ZHU X J, et al. A successful pregnancy in a patient with secondary hypertension caused by adrenal adenoma: a case report[J]. BMC Pregnancy Childbirth, 2019, 19(1): 116. doi: 10.1186/s12884-019-2262-2 [13] DI PASQUO E, GIANNUBILO S R, VALENTINI B, et al. The “preeclampsia and hypertension target treatment” study: a multicenter prospective study to evaluate the effectiveness of the antihypertensive therapy based on maternal hemodynamic findings[J]. Am J Obstet Gynecol MFM, 2024, 6(5): 101368. doi: 10.1016/j.ajogmf.2024.101368 [14] SHI D D, YANG F Z, ZHOU L, et al. Oral nifedipine vs. intravenous labetalol for treatment of pregnancy-induced severe pre-eclampsia[J]. J Clin Pharm Ther, 2016, 41(6): 657-661. doi: 10.1111/jcpt.12439 [15] KLEIN K L, SCOTT W J, WILSON J G. Aspirin-induced teratogenesis: a unique pattern of cell death and subsequent polydactyly in the rat[J]. J Exp Zool, 1981, 216(1): 107-112. doi: 10.1002/jez.1402160111 [16] ARULKUMARAN N, LIGHTSTONE L. Severe pre-eclampsia and hypertensive crises[J]. Best Pract Res Clin Obstet Gynaecol, 2013, 27(6): 877-884. doi: 10.1016/j.bpobgyn.2013.07.003 [17] OHISHI M. Hypertension with diabetes mellitus: physiology and pathology[J]. Hypertens Res, 2018, 41(6): 389-393. doi: 10.1038/s41440-018-0034-4 [18] PASCALL E, TULLOH R M. Pulmonary hypertension in congenital heart disease[J]. Future Cardiol, 2018, 14(4): 343-353. doi: 10.2217/fca-2017-0065 [19] CHAPMAN L, BURROWS-PEAKIN R, REGE V P, et al. Serum cystine aminopeptidase and the small-for-dates baby in hypertensive pregnancy[J]. Br J Obstet Gynaecol, 1976, 83(3): 238-240. doi: 10.1111/j.1471-0528.1976.tb00816.x -




 下载:
下载: