-
蛋白质作为生命体的主要执行者,其稳态性对细胞功能的正常发挥至关重要[1]。蛋白质的合成与降解是调控人体生命活动、维持生理平衡的关键机制[2]。在人体细胞内,主要存在两种蛋白质降解途径:泛素−蛋白酶体途径(ubiquitin-proteasome system, UPS)和溶酶体途径(lysosomal pathway system, LPS)。其中,泛素介导蛋白降解过程,控制着真核细胞中大部分蛋白质的降解,进而调控细胞的增殖、分化、凋亡、DNA修复和蛋白质的转录[3-4]。这一过程不仅涉及人体的免疫应答和病原体致病,还在生长发育、生殖及衰老等生命周期活动中发挥核心的控制作用[5-6]。
线性泛素化修饰是近年来研究发现的一种新型多聚泛素连接方式。去线性泛素化酶(OTU domain DUB with linear linkage specificity,OTULIN)是目前唯一报道可特异性水解线性泛素链的去泛素化酶(deubiquitinating enzymes,DUBs)[7]。OTULIN在机体多种生理和病理过程中具有关键调控作用,广泛参与细胞凋亡、信号转导、胚胎血管生成、免疫应答及炎症反应等生物学过程,并与OTULIN相关自身炎症综合征及肿瘤的发生发展密切相关[8-12]。OTULIN作为唯一能够特异性识别及水解线性泛素链的酶,在调控机体生命活动中具有独特作用,已成为新兴的研究热点,并有望成为治疗相关疾病的潜在靶点[13]。现关于OTULIN的功能研究仍处于初级阶段,迄今为止尚无其小分子配体的相关报道。OTULIN的具体功能尚未明确,新的机制有待进一步深入研究。
本研究基于OTULIN蛋白的结构与功能,构建全新的体外生物活性评价体系。体外分子水平实验因仅存在目标分子,可排除体内复杂环境带来的诸多干扰,是较为理想的实验环境。表达纯化得到线性泛素的底物蛋白,是构建OTULIN体外生物活性评价体系的重要基础。据文献报道,OTULIN作为唯一特异性切割线性泛素化的DUBs,其活性区域位于80~352片段[14],设计了特异性的全新底物蛋白组氨酸标签-泛素分子-泛素分子-flag标签(His-Ub-Ub-Flag),用于构建靶向OTULIN体外酶活评价方法。
-
NanoDrop超微量分光光度计(Thermo)、天平(Sartorius)、纯水仪(Millipore)、低温高速离心机(Eppendorf)、控温摇床(上海知楚仪器有限公司)、超声破碎仪(宁波新艺超声设备有限公司)、水浴锅(群安科学仪器有限公司)、超净台(江苏苏净集团有限公司)、垂直电泳槽(天能,VE-180)、电泳仪(天能,100-
1300 )、电泳槽(上海天能Tanon)、纯水仪(Millipore公司)和往复式脱色摇床(KYLIN-BELL公司)。 -
灭菌水、灭菌枪头、灭菌EP管、灭菌摇菌管、感受态细胞BL21、DH5α,LB培养基、Ni-NTA磁珠、酶蛋白诱导剂、蛋白酶抑制剂、β-D-硫代半乳糖苷(IPTG)、卡那霉素和咪唑。SDS/PAGE胶及电泳液(雅酶,LK309),转膜液5 × Transfer Buffer(BIO-RAD,
10026938 )、PVDF膜(Merck)、速溶型蛋白上样缓冲液5 × Loading buffer(雅酶,LT101S)、双色预染蛋白Marker(雅酶,WJ102)、无蛋白快速封闭液(雅酶,PS108P)、通用型抗体稀释液(雅酶,PS119L)、Alexa Fluor® 680 AffiniPure Goat Anti-Mouse IgG(H+L)(翌圣,33218ES60,1:25 000)、Alexa Fluor® 680 AffiniPure Goat Anti-Rabbit IgG(H+L)(翌圣,33118ES60,1:25 000)和Mouse anti His-Tag mAb(爱博泰克,AE003)。OTULIN质粒、His-Ub-Ub-Flag质粒、考马斯亮蓝快速免脱色染色液(派翠,KB0016)。 -
根据文献方法[15]分析OTULIN与底物蛋白Met1-diUb复合晶体结构(PDB:5OE7,2.95 Å),采用人源Met1-Ub基因序列,设计了首个人源His-Ub-Ub-Flag重组表达质粒,由南京金斯瑞生物科技有限公司进行全基因合成,测序正确。His-Ub-Ub-Flag质粒序列如下所示。
-
MGSSHHHHHHSSGLVPRGSHMQIFVKTLTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTLHLVLRLRGGMQIFVKTLTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTLHLVLRLRGGKLDYKDDDDK。
-
ATGGGCAGCAGCCATCATCATCATCATCACAGCAGCGGCCTGGTGCCGCGCGGCAGCCATATGCAGATCTTCGTGAAAACCCTTACCGGCAAGACCATCACCCTTGAGGTGGAGCCCAGTGACACCATCGAAAATGTGAAGGCCAAGATCCAGGATAAGGAAGGCATTCCCCCCGACCAGCAGAGGCTCATCTTTGCAGGCAAGCAGCTGGAAGATGGCCGTACTCTTTCTGACTACAACATCCAGAAGGAGTCGACCCTGCACCTGGTCCTGCGTCTGAGAGGTGGTATGCAGATTTTCGTGAAAACCCTGACCGGCAAAACCATTACCCTGGAAGTGGAACCGAGCGATACCATTGAAAATGTGAAAGCGAAAATTCAGGATAAAGAAGGCATTCCGCCGGATCAGCAGCGCCTGATTTTTGCGGGCAAACAGCTGGAAGATGGCCGCACCCTGAGCGATTATAACATTCAGAAAGAAAGCACCCTGCATCTGGTGCTGCGCCTGCGCGGCGGCAAGCTTGACTACAAGGACGACGATGACAAGTAA。
-
根据文献方法[16],采用大肠埃希菌BL21(DE3)感受态细胞进行转化。首先,将质粒干粉溶解于40 μl ddH2O中,充分混匀后配制成终浓度为100 ng/μl的质粒溶液。取2 μl质粒溶液加入50 μl BL21(DE3)感受态细胞中,轻轻混匀后置于冰上静置30 min。随后,将感受态细胞于42℃热激90 s,以促进质粒进入细胞内,并立即置于冰上静置。之后加入800 μl LB液体培养基,于37℃、140 r/min摇床中振荡培养1 h,以促进细胞复苏。
复苏结束后,将菌液于3 000 r/min离心2 min,弃去上清液,保留菌体沉淀,并用100 μl LB培养基重悬。由于His-Ub-Ub-Flag质粒具有卡那霉素抗性,取100 μl重悬菌液均匀涂布于含卡那霉素的LB固体培养基平板上,倒置于37℃恒温培养箱中过夜培养。次日观察菌落生长情况,结果显示His-Ub-Ub-Flag质粒已成功转化至BL21(DE3)感受态细胞中,用于后续诱导表达。
-
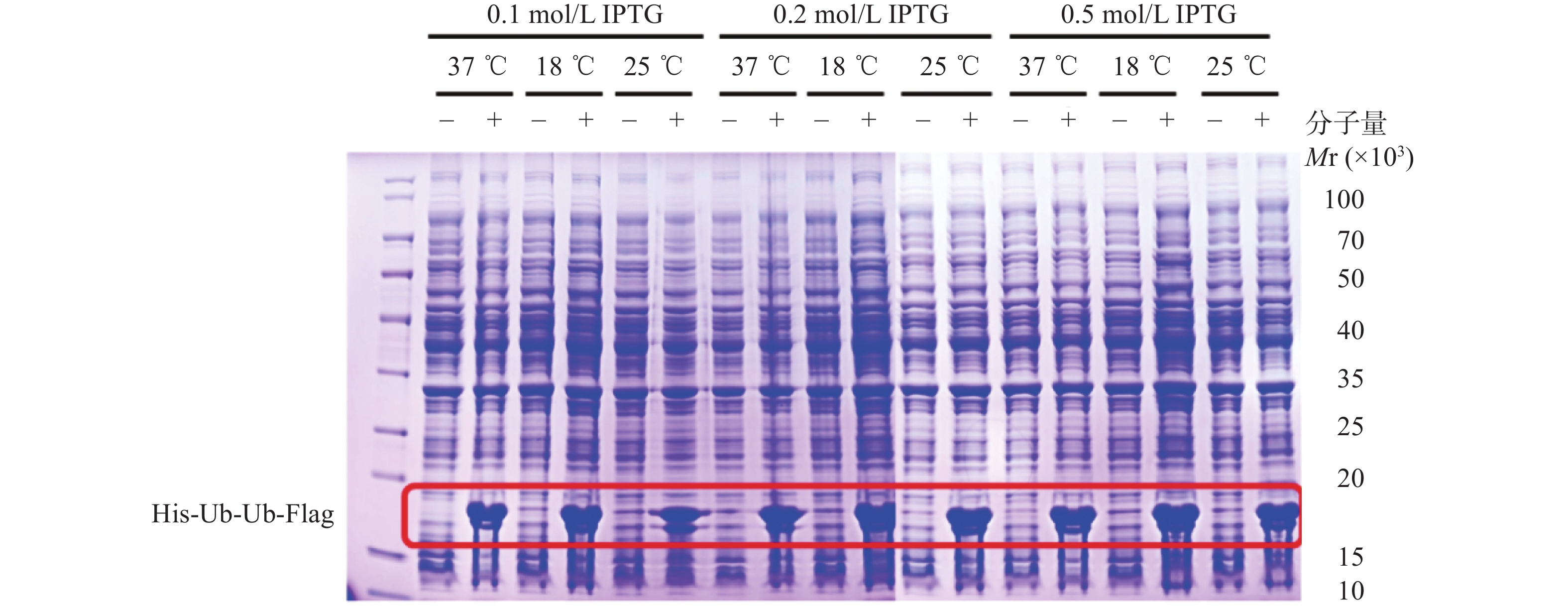
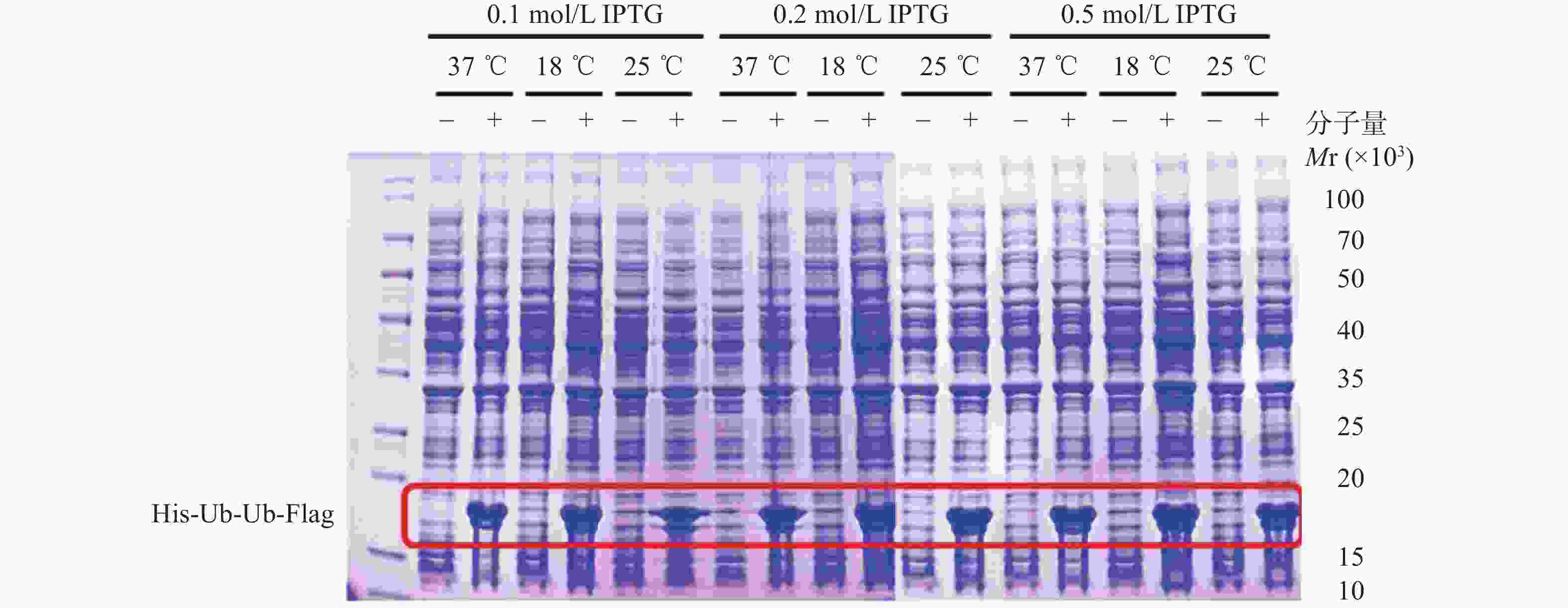
上述质粒转化实验结果显示,His-Ub-Ub-Flag在Escherichia coli (E.coli)的BL21转化效率较高。挑选单克隆菌落,转至3 ml含卡那霉素的LB液体培养基,置于37℃,220 r/min,摇床上震荡过夜,并收集小摇表达后的菌落。经过对蛋白诱导条件的摸索,考察不同浓度的异丙基-β-D-硫代半乳糖苷(Isopropyl-beta-D-thiogalactopyranoside,IPTG),在37、18、25℃温度下的蛋白诱导条件,分别将诱导得到的蛋白,电泳上样后用考马斯亮蓝染色方法检测蛋白纯度,发现最优的蛋白诱导条件为18℃,0.2 mmol/L IPTG,220 r/min,14~16 h(图1)。
-
挑选His-Ub-Ub-Flag质粒的在BL21中的单克隆菌落,取2 ml小摇菌液加入到准备好的具有卡那霉素抗性的400 ml LB液体培养基,置于37℃、220 r/min摇床上振荡过夜。待大摇菌液A值测试为0.6~1之间,加入0.2 mmol/L IPTG,置于18℃下,220 r/min,摇床振荡14~16 h诱导蛋白大量表达。次日,将大摇菌液分装50 ml离心管中,4℃,4 000 r/min,离心20 min。弃上清液,将菌落沉淀置于−80℃保存。
-
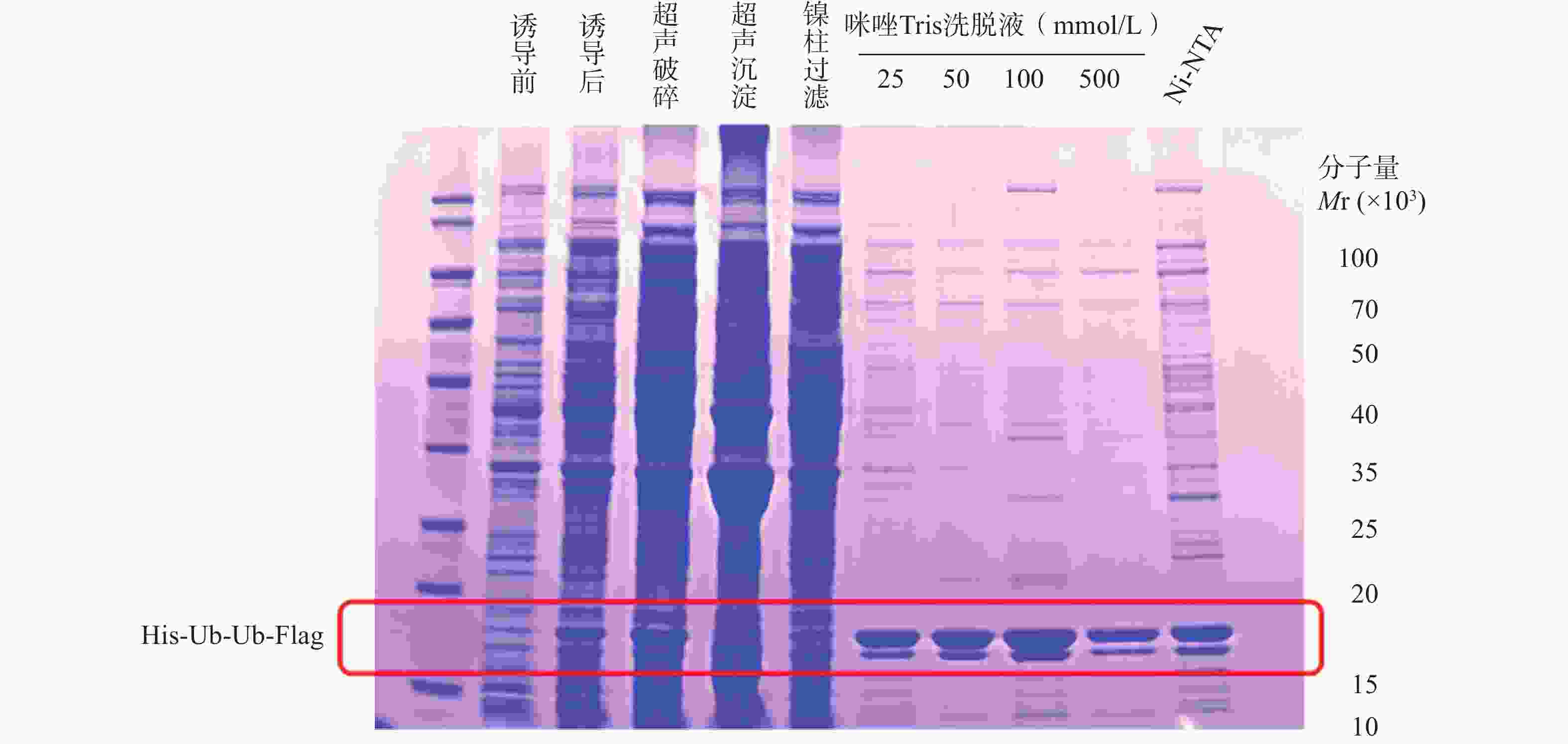
His-Ub-Ub-Flag表达载体携带6 × His Tag,蛋白大量表达后选用Ni2+离子亲和层析柱进行初步纯化。在蛋白纯化实验中,使用适量的蛋白裂解缓冲液buffer A(20 mmol/L Tris,500 mmol/L NaCl,pH 8.0)重悬菌体,离心后弃上清液,再加入适量蛋白酶抑制剂。将菌液置于超声破碎仪,破碎超声至菌液澄清。将菌液置于4℃,13 000 r/min,离心30 min。弃上清液,在沉淀中加入活化后的Ni-NTA磁珠共孵育。离心并弃上清液后,配制不同浓度比例咪唑的Tris buffer洗脱蛋白,反复清洗沉淀4次,洗脱掉不结合的杂蛋白,浓缩后收集目标蛋白。采用NanoDrop检测蛋白浓度,得到本批次His-Ub-Ub-Flag蛋白浓度为1.21 mg/ml。将每步留样蛋白依次上样电泳,用考马斯亮蓝染色法检测蛋白表达纯化结果,洗脱后得到符合分子量的蛋白条带(图2)。
-
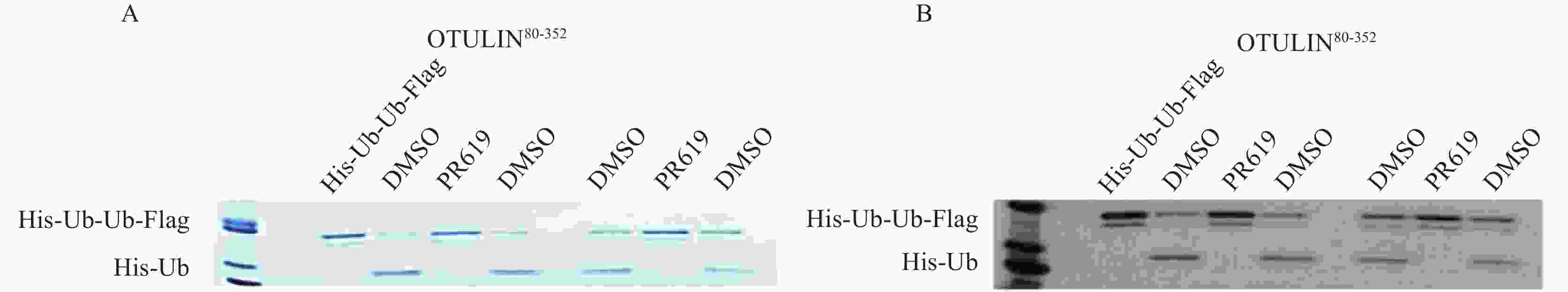
化合物2,6-二氨基-3,5-二硫氰基吡啶(2,6-Diamino-3,5-dithiocyanopyridine,PR619)可诱导细胞中多泛素化蛋白的积累,是非选择性且可逆的去泛素化酶抑制剂。文献报道PR619抑制多个DUBs蛋白的活性,如USP4(EC50=3.93 μmol/L),USP8(EC50=4.90 μmol/L),JOSD2(EC50=1.17 μmol/L),UCH-L3(EC50=2.95 μmol/L)[17-18]。经酶活评价验证,PR619具有浓度依赖性且可稳定抑制OTULIN蛋白的阳性对照药,其对OTULIN蛋白的EC50值为16.8 μmol/L(图3)。
-
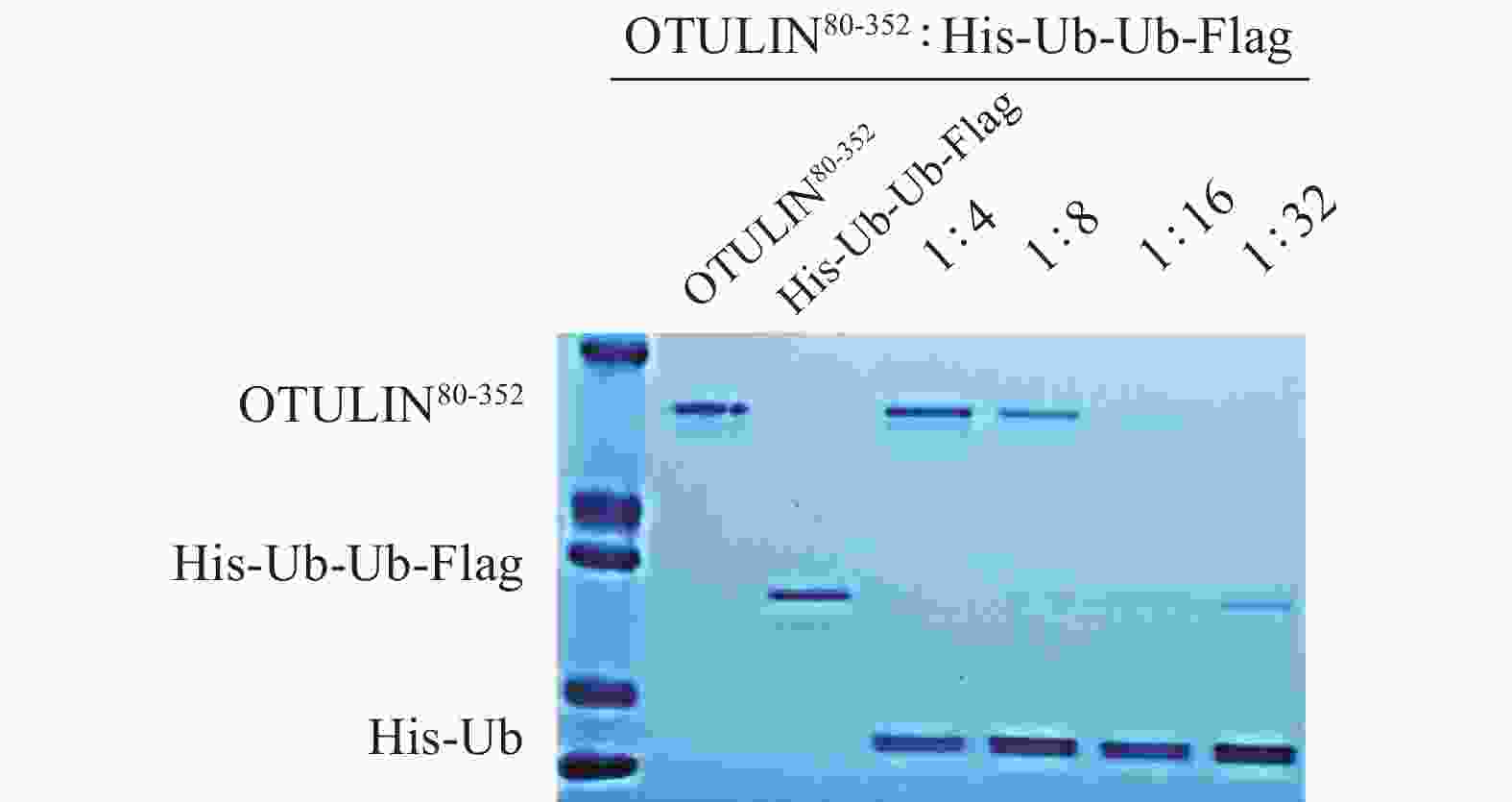
选用OTULIN活性片段(OTULIN80-352,分子量31 000),底物蛋白His-Ub-Ub-Flag,分子量20 500,阳性对照化合物PR619,空白对照DMSO。首先考察酶与底物蛋白在不同用量比下的酶活效率。将OTULIN80-352与PR619室温孵育,再加入底物蛋白His-Ub-Ub-Flag,37℃水浴孵育,电泳检测后用考马斯亮蓝染色法观察结果。根据实验结果,选择OTULIN80-352与底物蛋白His-Ub-Ub-Flag的用量比为1∶16,可清晰见到达酶切反应平衡的蛋白条带(图4)。
-
将30 μmol/L PR619与OTULIN80-352蛋白室温孵育30 min,加入相应的底物蛋白在37℃水浴下反应。电泳检测,考马斯亮蓝染色后对比观察。水浴37℃中反应10 min,酶切下的His-Ub条带不清晰,提示反应作用时间过短,水解不充分。当反应20 min时,可以明显观察到被OTULIN水解后的His-Ub蛋白。当反应30、40、60 min时,并无明显差异。为考察实验操作的一致性,每组条件设置2组DMSO组,为提高实验效率,选择酶水解底物反应条件为37℃,作用20 min,结果见图5。
-
在众多的蛋白质翻译后修饰(post-translational modification,PTM)类型中,线性泛素化因其独特的Met1连接方式,在NF-κB信号通路激活及炎症反应中发挥特异性作用。OTULIN作为该PTM的唯一已知逆转酶,其酶活性的精确调控直接决定了线性泛素化信号的强度与持续时间。为了建立高效的OTULIN活性检测体系,本研究首次成功构建、表达并纯化了线性泛素底物His-Ub-Ub-Flag。通过对酶与底物用量比及反应时间的梯度优化,确立了最佳酶促反应动力学窗口,在OTULIN蛋白与底物蛋白His-Ub-Ub-Flag用量是1∶16,37℃孵育20 min达到反应平衡,并采用广谱去泛素化酶抑制剂PR619作为阳性对照药物进行验证。实验结果显示,阳性对照药物PR619对OTULIN活性表现出明显的剂量依赖性抑制作用,证明了该体系对抑制剂检测的稳定性和灵敏度。利用构建的线性泛素蛋白底物,能有效评价去线性泛素化酶OTULIN的体外分子水平生物活性。
-
新药靶点的发现与确证是现代医药创新的核心驱动力。在众多药物类型中,小分子药物凭借其优良的理化性质及卓越的细胞膜透过能力,在靶向细胞内蛋白方面展现出天然优势。本研究聚焦的去线性泛素化酶OTULIN,作为线性泛素化这一特殊蛋白质翻译后修饰的唯一特异性逆转酶,在维持PTM动态平衡、调控NF-κB信号通路及先天免疫稳态中发挥着不可替代的作用。鉴于OTULIN功能异常与肿瘤及免疫疾病的密切关联,开发针对该靶点的特异性小分子抑制剂具有重要的转化医学价值。
本研究致力于解决OTULIN靶向药物筛选的方法学难题,成功构建了一套稳定、精准的体外活性评价体系,实现了对候选化合物抑制效应的定量评估。该体系的建立,不仅为解析OTULIN介导的PTM去修饰机制提供了有力工具,更为后续针对该潜在新药靶点开展高内涵、高通量的药物筛选提供了全新的技术方法。
Establishment of in vitro biological activity evaluation system for OTULIN
-
摘要:
目的 构建靶向去线性泛素化酶(OTULIN)的体外酶活评价体系,为OTULIN抑制剂筛选提供实验基础。 方法 设计并表达纯化线性泛素底物蛋白His-Ub-Ub-Flag,以OTULIN80-352为研究对象,采用广谱去泛素化,酶抑制剂PR619作为阳性对照,通过优化酶与底物用量比及反应时间,建立OTULIN体外酶活评价体系。 结果 成功获得线性泛素底物蛋白His-Ub-Ub-Flag。PR619可明显抑制OTULIN的酶活性,验证了该体系的可行性。实验确定OTULIN80-352与底物His-Ub-Ub-Flag的最佳用量比为1∶16,在37℃孵育20 min时反应效果较佳。 结论 本研究成功建立了OTULIN体外酶活评价体系,可用于候选化合物对OTULIN酶活抑制作用的评价,为后续OTULIN小分子抑制剂筛选提供了技术支持。 Abstract:Objective To establish an in vitro enzymatic activity evaluation system for OTULIN (OTU domain DUB with linear linkage specificity)and provide an experimental basis for OTULIN inhibitor screening. Methods The linear ubiquitin substrate protein His-Ub-Ub-Flag was designed, expressed, and purified. Using OTULIN80-352 as the target enzyme and PR619 as a positive control, the enzyme-to-substrate ratio and reaction time were optimized to establish an in vitro OTULIN activity evaluation system. Results The linear ubiquitin substrate protein His-Ub-Ub-Flag was successfully obtained. OTULIN activity was significantly inhibited by PR619, which confirmed the feasibility of the assay. The optimal enzyme-to-substrate ratio of OTULIN80-352 to His-Ub-Ub-Flag was 1∶16, and the optimal reaction condition was incubation at 37℃ for 20 min. Conclusion An in vitro enzymatic activity evaluation system for OTULIN was successfully established, which could be used to evaluate the inhibitory effects of candidate compounds on OTULIN activity and provide technical support for subsequent screening of OTULIN small-molecule inhibitors. -
Key words:
- OTULIN /
- linear ubiquitin /
- in vitro bioactivity /
- enzyme activity evaluation
-
[1] RAJALINGAM K, DIKIC I. SnapShot: expanding the ubiquitin code[J]. Cell, 2016, 164(5): 1074-1074. doi: 10.1016/j.cell.2016.02.019 [2] DEBNATH J, GAMMOH N, RYAN K M. Autophagy and autophagy-related pathways in cancer[J]. Nat Rev Mol Cell Biol, 2023, 24(8): 560-575. doi: 10.1038/s41580-023-00585-z [3] MATSUZAWA-ISHIMOTO Y, HWANG S, CADWELL K. Autophagy and inflammation[J]. Annu Rev Immunol, 2018, 36: 73-101. doi: 10.1146/annurev-immunol-042617-053253 [4] DEWSON G, EICHHORN P J A, KOMANDER D. Deubiquitinases in cancer[J]. Nat Rev Cancer, 2023, 23(12): 842-862. doi: 10.1038/s41568-023-00633-y [5] KWON Y T, CIECHANOVER A. The ubiquitin code in the ubiquitin-proteasome system and autophagy[J]. Trends Biochem Sci, 2017, 42(11): 873-886. doi: 10.1016/j.tibs.2017.09.002 [6] Kemp S B, Cheng N, Markosyan N, et al. Efficacy of a small-molecule inhibitor of KrasG12D in immunocompetent models of pancreatic cancer[J]. Cancer Discov, 2023, 13(2): 298-311. doi: 10.1158/2159-8290.CD-22-1066 [7] YAU R, RAPE M. The increasing complexity of the ubiquitin code[J]. Nat Cell Biol, 2016, 18(6): 579-586. doi: 10.1038/ncb3358 [8] ZHANG Y, FU Y S, QIANG L H, et al. Spatiotemporal regulation of STING activity by linear ubiquitination governs antiviral immunity[J]. Adv Sci, 2025, 12(28): 2417660. doi: 10.1002/advs.202417660 [9] ZEIN L, DIETRICH M, BALTA D, et al. Linear ubiquitination at damaged lysosomes induces local NFKB activation and controls cell survival[J]. Autophagy, 2025, 21(5): 1075-1095. doi: 10.1080/15548627.2024.2443945 [10] WIENER R, WOLBERGER C. A new DUB makes linear ubiquitin a party to its own destruction[J]. Cell, 2013, 153(6): 1189-1191. doi: 10.1016/j.cell.2013.05.018 [11] WANG W, LI M Q, PONNUSAMY S, et al. ABL1-dependent OTULIN phosphorylation promotes genotoxic Wnt/β-catenin activation to enhance drug resistance in breast cancers[J]. Nat Commun, 2020, 11(1): 3965. doi: 10.1038/s41467-020-17770-9 [12] HRDINKA M, GYRD-HANSEN M. The Met1-linked ubiquitin machinery: emerging themes of(de)regulation[J]. Mol Cell, 2017, 68(2): 265-280. doi: 10.1016/j.molcel.2017.09.001 [13] JAHAN A S, ELBÆK C R, DAMGAARD R B. Met1-linked ubiquitin signalling in health and disease: inflammation, immunity, cancer, and beyond[J]. Cell Death Differ, 2021, 28(2): 473-492. doi: 10.1038/s41418-020-00676-w [14] HEGER K, WICKLIFFE K E, NDOJA A, et al. OTULIN limits cell death and inflammation by deubiquitinating LUBAC[J]. Nature, 2018, 559(7712): 120-124. doi: 10.1038/s41586-018-0256-2 [15] KEUSEKOTTEN K, ELLIOTT P R, GLOCKNER L, et al. OTULIN antagonizes LUBAC signaling by specifically hydrolyzing Met1-linked polyubiquitin[J]. Cell, 2013, 153(6): 1312-1326. doi: 10.1016/j.cell.2013.05.014 [16] CHEN Y F, WANG L F, CHENG X M, et al. An ultrasensitive system for measuring the USPs and OTULIN activity using Nanoluc as a reporter[J]. Biochem Biophys Res Commun, 2014, 455(3-4): 178-183. doi: 10.1016/j.bbrc.2014.10.139 [17] ALTUN M, KRAMER H B, WILLEMS L I, et al. Activity-based chemical proteomics accelerates inhibitor development for deubiquitylating enzymes[J]. Chem Biol, 2011, 18(11): 1401-1412. doi: 10.1016/j.chembiol.2011.08.018 [18] ZHOU Q, YU X M, DEMIRKAYA E, et al. Biallelic hypomorphic mutations in a linear deubiquitinase define otulipenia, an early-onset autoinflammatory disease[J]. Proc Natl Acad Sci USA, 2016, 113(36): 10127-10132. doi: 10.1073/pnas.1612594113 -




 下载:
下载: