-
癌症治疗是最前沿、最受关注的医学研究之一,传统治疗手段有化疗、放疗、手术切除等,但若治疗不彻底会导致肿瘤的复发或转移,因此亟需更安全有效的治疗策略。近年来,免疫疗法已成为癌症的突破性治疗方法,被广泛应用于临床。免疫疗法旨在激活机体免疫系统,产生抗肿瘤免疫反应来遏制肿瘤的发生、发展和复发。目前,免疫治疗策略有单克隆抗体[1]、免疫检查点抑制[2]、过继细胞疗法[3]以及肿瘤疫苗[4]。鉴于以肿瘤疫苗为代表的免疫疗法在临床中展现出较大潜力,肿瘤疫苗已成为研究者关注的热点。肿瘤疫苗可以有效地将肿瘤特异性抗原(tumor specific antigen,TSAs)递送到抗原呈递细胞(antigen-presenting cells,APC)并激活肿瘤抗原特异性T细胞(tumor antigen-specific T cells,TASTs),建立持久抗肿瘤记忆,减少非特异性杀伤和不良反应,最终诱导局部肿瘤消退甚至根除。
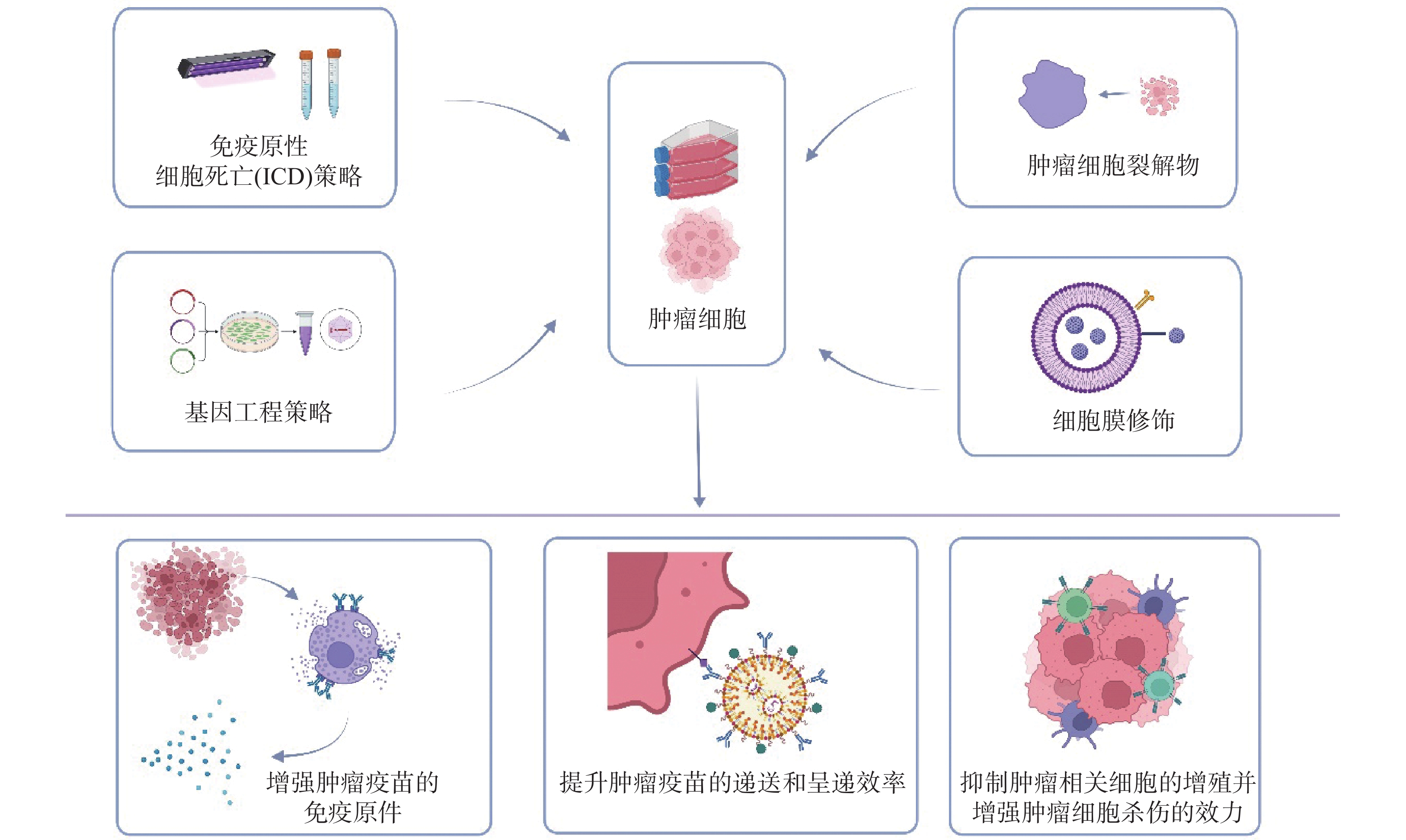
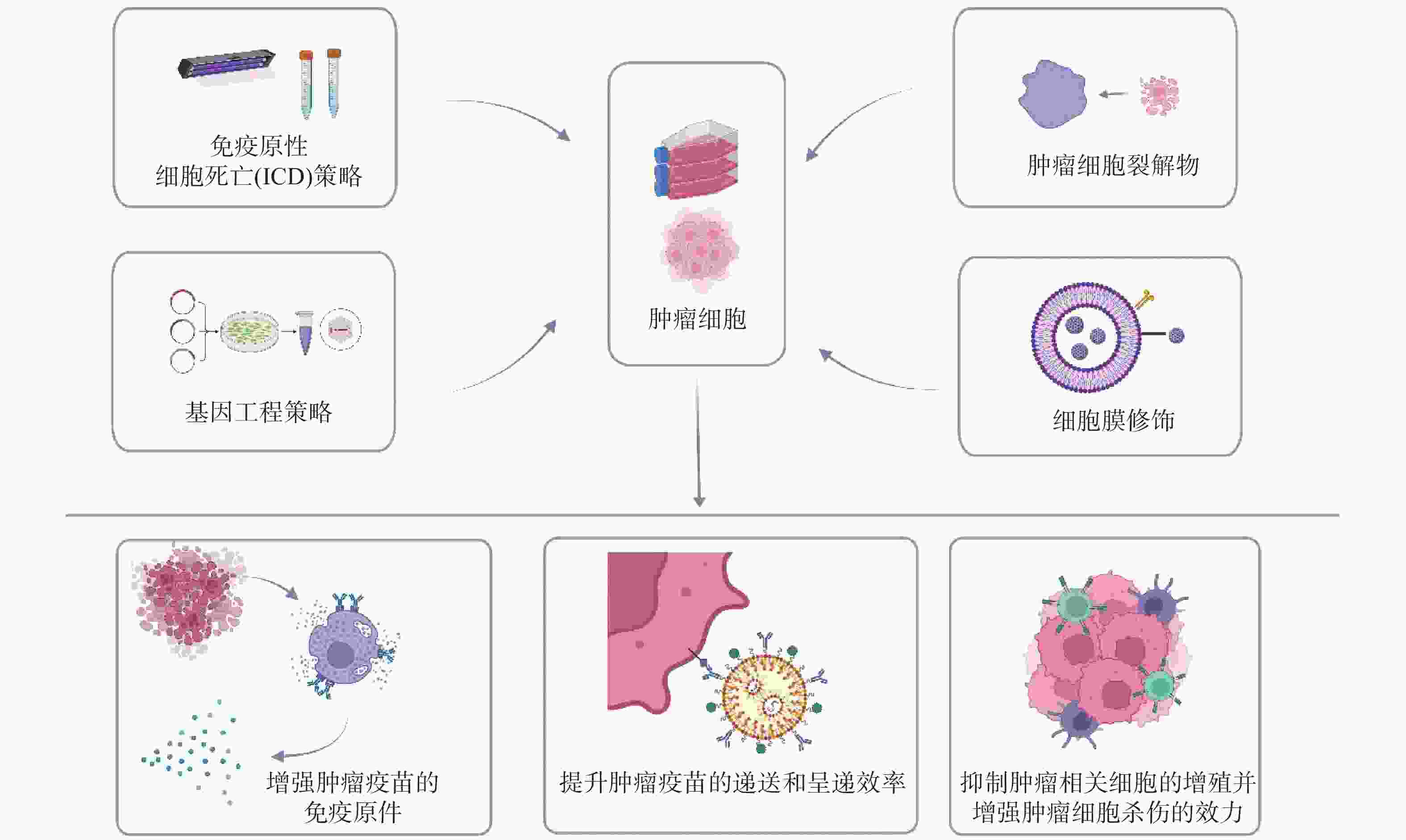
抗原是肿瘤疫苗的主要部分,有效的抗原能够激活TASTs,并诱导对肿瘤靶向免疫反应。肿瘤抗原主要有两种类型:肿瘤相关抗原(tumor-associated antigen,TAAs)和TSAs。TAAs在肿瘤组织中过表达,但在正常组织中表达水平较低;TSAs是由癌症相关的非同义突变或其他基因突变引起的,这些突变导致人类白细胞抗原仅在肿瘤细胞表面呈递突变多肽(新抗原),因此,TSAs能够引起高度特异性抗肿瘤免疫反应[5]。然而,由于突变的不确定性,很少有抗原可以用于制备通用的肿瘤疫苗[6]。肿瘤细胞因自身含有全面的抗原,使得肿瘤细胞非常适合制备成疫苗来诱导肿瘤特异性免疫反应[7],但是肿瘤细胞制备的疫苗仍面临三大挑战:①免疫原性;②免疫逃逸;③有效递送。科学家已开发诸多方法,例如:免疫原性细胞死亡(immunogenic cell death,ICD)、基因工程、细胞膜修饰、肿瘤裂解物等方法来提高肿瘤疫苗的免疫原性[8]和递送效率[9]。基于以上背景,本文回顾全肿瘤细胞疫苗(通过物理、化学等方法,灭活处理自体或异体肿瘤细胞,并尽可能保留肿瘤细胞蛋白,维持肿瘤细胞抗原图谱,从而实现抗肿瘤效果)的最新进展,概述了工程化肿瘤全细胞疫苗(图1)和使用ICD、基因工程、肿瘤细胞裂解物、细胞膜修饰策略制备而成的肿瘤疫苗在治疗过程所呈现出的优势与劣势,并讨论它们的临床进展及应用前景,希望能为后续的肿瘤疫苗研究提供参考。
单纯的肿瘤全细胞疫苗存在免疫原性较低,递送效率差等局限。为了提高疫苗的递送效率、靶向能力和治疗效果,已开发多种工程化策略用于全细胞疫苗的制备[10]。目前的方法有:①诱导肿瘤细胞免疫原性死亡以增强其免疫原性;②通过引入或敲除基因以达到对肿瘤细胞表面蛋白的表达进行基因工程修饰,从而提高肿瘤疫苗的免疫原性;③工程修饰,包括细胞膜修饰和肿瘤细胞裂解物策略,其中,细胞膜修饰通过在疫苗表面嵌入功能化基团或连接纳米粒,以提高疫苗的递送效率、靶向能力和治疗效果,肿瘤细胞裂解物策略通过包载的裂解物提升治疗效果。
-
ICD策略是通过射频消融、微波消融、超声消融、冷冻消融、光动力疗法(photodynamic therapy,PDT)、化学消融等快速肿瘤消融疗法引发肿瘤细胞ICD [11-14],从而激活肿瘤靶向免疫应答,增强治疗效果。
ICD涉及细胞表面组成的变化以及可溶性介质的释放,这些信号作用于树突细胞(dendritic cell,DC),将肿瘤抗原呈递给T细胞,因此癌细胞ICD已经成为改善疫苗免疫原性、增强治疗效果的有效策略之一。Basta等发现暴露于γ射线或裂解与UV照射联用(lysis combined with UV-irradiation,LyUV)的黑素瘤细胞比仅裂解或暴露于UV照射的细胞能够提供更好的抗肿瘤效果。此外,IL-27可以作为佐剂增强γ射线或LyUV制备的肿瘤疫苗的效果[15]。Luo等也证实,与对照组和未照射的Lewis 肺癌细胞(Lewis lung cancer cells,LLC)相比,经过辐照(incoming radiation,IR)的肿瘤细胞裂解物(tumor cell lysate,TCL)具有更强的抗肿瘤作用,显著增加小鼠脾脏成熟DC、总CD 4+ T细胞、上调血清中Ⅱ型干扰素和白细胞介素-4(interleukin-4,IL-4)水平、使肿瘤组织中CD 4+ T细胞和CD 8+ T细胞浸润增加。此外,IR-LLC的裂解物制备成疫苗后,在LLC异种移植小鼠模型中观察到更高的抗肿瘤应答[16]。PDT引发的应激创伤使得肿瘤细胞具有高度免疫原性,这是由于应激反应可以诱导隐藏在肿瘤细胞RNA非翻译区的抗原表达。除了上述几种方式诱导ICD以外,放线菌素D[17]、环磷酰胺[18]、玛贝兰妥单抗[19]等也都展示出效力。因此,基于ICD策略制备的肿瘤疫苗仍具备一定潜力。
-
肿瘤全细胞疫苗因提供广泛的个性化肿瘤抗原(包括TAAs和新抗原)、CD 4+ T细胞和CD 8+ T细胞的表位[20],从而为肿瘤治疗提供优势。未经修饰的肿瘤细胞不会产生强烈的免疫反应[21],因此,增强免疫刺激因子在肿瘤疫苗中的表达至关重要,方法之一就是利用基因工程技术修饰细胞,使细胞可以分泌更多的免疫刺激因子。基因工程(如CRISPR/Cas9技术)作为一种灵活的修饰方法,可以修饰活细胞的遗传信息,通过特异性基因编辑将外源基因引入到受体细胞以改变细胞表型[22]。因此,基因工程可以根据不同的需求开发出更有效的肿瘤全细胞疫苗。例如:粒细胞−巨噬细胞集落刺激因子(granulocyte-macrophage colony-stimulating factor,GM-CSF)基因修饰肿瘤疫苗GVAX,它是一种基因工程疫苗,修饰肿瘤细胞,使肿瘤细胞过表达GM-CSF,过表达的GM-CSF用作免疫佐剂,增强DC的抗原呈递能力并提高DC存活率[23]。
肿瘤含有一种独特的、类似于干细胞的细胞亚群,称为癌症干细胞(cancer stem cells,CSCs),CSCs具有耐药、转移和易复发等特性,基于CSCs的肿瘤疫苗可以有效激活抗肿瘤免疫[24]。肿瘤相关分子黏蛋白1(the transmembrane glycoprotein mucin 1,MUC1)是一种跨膜黏蛋白糖蛋白,在结直肠癌症中过表达,并被确定为免疫疗法的治疗靶点[25]。因此,过表达MUC1结直肠癌的CSCs疫苗具有巨大潜力,它们不仅对CD 4+ T细胞、CD 25+ T细胞亚群表现出抑制作用,还显著增加自然杀伤细胞(natural killer cell,NK)和脾细胞的细胞毒性,靶向杀伤结直肠癌的CSCs[26]。在另一项研究中,过表达GM-CSF的CSCs肿瘤疫苗可以诱导肿瘤组织中更高数量的CD 8+ T细胞浸润。此外,该疫苗还上调肿瘤细胞中细胞程序性死亡−配体1(programmed cell death 1 ligand 1,PD-L1)的表达,导致免疫抵抗。因此,CSCs疫苗与程序性细胞死亡蛋白-1(programmed death-1,PD-1)阻断剂联合使用可以更有效地治疗肿瘤。将链霉亲和素(streptavidin)-GM-CSF[27]表面修饰的膀胱癌CSCs疫苗与PD-1阻断剂联合治疗膀胱癌,可以改善特异性T淋巴细胞的功能。如上所述,基因工程后的肿瘤疫苗可以增强免疫原性、提升其他免疫细胞的抗原呈递能力、抑制肿瘤相关细胞增殖、提升杀伤效力等。
-
细胞膜修饰策略是将肿瘤疫苗与日益成熟的生物材料领域相结合,提升疫苗递送效率和免疫原性,是具有良好前景的工程化策略。肿瘤细胞膜除了能够提供丰富的TAAs,还能逃避免疫系统清除。此外,肿瘤细胞膜因含有一系列官能团,可以使用各种生物材料对其表面进行化学和物理修饰。
许多反应性基团(如胺)可以通过特定反应化学偶联到膜表面,继而将靶向肽或纳米粒偶联到膜表面。
Zhao[28]等将抗PD-1抗体通过还原活化的接头与灭活肿瘤细胞偶联,并通过马来酰亚胺-硫醇偶联载有阿霉素(doxorubicin,DOX)的脂质体。其中,灭活肿瘤细胞提供的TAAs促进药物靶向病灶,诱导抗肿瘤免疫反应。DOX诱导的ICD和抗PD-1抗体协同激活抗肿瘤免疫反应,改善免疫微环境。通过这种方式,将肿瘤细胞设计为可修饰的载体来递送药物和活性分子,丰富了肿瘤疫苗的功能。
化学修饰方法的优点在于可以稳定负载药物并控制药物释放,然而药物负载比例和使用剂量需要不断调整,特别是用于临床转化方面,并且安全性也需要进一步探索和了解。
此外,基于肿瘤细胞膜的固有负电荷性质,疏水分子或带正电的纳米颗粒可以吸附在其表面。类似地,免疫佐剂也可以使用物理方法直接插入细胞的脂质双层膜中[9]。此类物理方法具有良好的安全性、易于制备等优点,然而,大规模生产所需的制备参数难以设定、优化制剂所需时间、人力、物力成本高昂等问题限制了其临床转化。
-
TCL因为拥有多种提高抗肿瘤免疫的TAAs,目前已有多种TCL疫苗被制备并投入研究,并且TCL疫苗可能具有更大的临床益处[29]。由于TCL进入体内后会快速降解,使得APC不能有效吸收这些裂解物。因此,工程策略侧重于修饰TCL,旨在增强其免疫原性。目前已经通过调节肿瘤免疫反应中的关键分子来增强疫苗免疫原性,例如阻断肝癌细胞STAT3信号通路抑制肿瘤细胞增殖、促进肿瘤细胞凋亡。STAT3阻断的TCL疫苗在抗肝细胞癌中的疗效已得到验证[30],并且可以抑制肿瘤生长复发、延长生存期。
抗原的有效递送是肿瘤疫苗治疗成功的关键, Wang等[31]将TCL共价连接到聚多巴胺(polydopamine,PDA)纳米颗粒上(TCL@PDA),促进DC的抗原摄取,增强表面分子表达和细胞因子分泌,延缓肿瘤的发展。TCL含有水溶性和水不溶性抗原,不同于水溶性抗原,水不溶性抗原难以简单装载在疫苗制剂中,如果利用工程化手段使疫苗能够装载水不溶性抗原,就有更多种类的肿瘤抗原被输送到体内。Kong等开发了具有表面甘露糖(mannose,Man)部分的壳聚糖(chitosan,CTS)纳米颗粒(nanoparticles,NPs),用于特异性DC靶向(Man-CTS NPs),再将Man-CTS NP加载由黑素瘤细胞产生的TCL(Man-CTS-TCL NP), Man-CTS-TCL NPs在患有黑素瘤的小鼠中表现出良好治疗效果[32]。
肿瘤疫苗中更高的抗原负载可以诱导更广泛的特异性免疫反应,因此,有研究将TCL同时装载在聚乳酸-羟基乙酸共聚物[poly(lactide-co-glycolide),PLGA]的内部和表面[33]并将免疫佐剂掺入疫苗中以提高效力。这些纳米疫苗实现了良好的预防效果,并且拥有一定的治疗效果,在与抗PD-1抗体联用后,对黑色素瘤小鼠的治愈率从25%增加到40%。另一项研究表明,次氯酸处理可增强TCL的免疫原性[34],使DC具有更高的成熟标志物(特别是CD83)表达,Berti等[29]使用负载次氯酸处理TCL的PLGA纳米颗粒,成功诱导DC成熟。
除了上述例子,基于TCL策略制备的肿瘤疫苗还能联合自体和同种异体肿瘤TCL刺激宿主DC和T细胞[35]、作为抗原来源激活诱导DC和特异性T细胞[36]。多种结果表明,TCL是肿瘤疫苗制备中非常有效的策略之一,其引发的特异性免疫反应和优异的抗肿瘤效率,对肿瘤疫苗的制备具有重要的临床意义。
-
本文归纳部分有代表性的肿瘤疫苗策略在临床中的进展(表1),旨在探究当前肿瘤疫苗的应用前景与面临的挑战。
表 1 肿瘤全细胞疫苗的临床试验
疫苗名称 肿瘤模型 疫苗种类 临床试验阶段 参考文献 GVAX 胰腺导管腺癌 基因工程肿瘤细胞 随机试验 [37] GVAX 乳腺癌 基因工程肿瘤细胞 Ⅰ期临床试验 [39] GVAX 髓系白血病 基因工程肿瘤细胞 Ⅱ期临床试验 [40] GVAX 胰腺导管腺癌 基因工程肿瘤细胞 Ⅱ期临床试验 [41] DC/MM 融合膜 骨髓瘤 DC-肿瘤细胞融合 Ⅱ期临床试验 [42] GBM 6-AD 胶质瘤 肿瘤裂解物 随机试验 [43] DCVax-L 胶质母细胞瘤 肿瘤裂解物 Ⅲ期临床试验 [44] AV-GBM-1 胶质母细胞瘤 肿瘤裂解物 Ⅱ期临床试验 [45] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱ期临床试验 [46] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱb期临床试验 [47] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱb期临床试验 [48] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱb期临床试验 [49] 卵巢癌自体肿瘤疫苗(Vigil) 卵巢癌 自体肿瘤细胞 Ⅱb期临床试验 [50] CSF-470 黑色素瘤 ICD肿瘤细胞 Ⅱ期临床试验 [51] Zheng等制备了由2种同种异体胰腺肿瘤细胞系组成的胰腺GVAX[37],仅接受GVAX治疗的患者中位总生存期(overall survival,OS)有延长的趋势。GM-CSF早在1993年就被Dranoff等[38]证明具有优秀的抗肿瘤效果,并在临床试验中展示出一定的效力。例如,Anderson等[39]从患者处收集的肿瘤细胞,通过腺病毒转导GM-CSF后,用10 000 cGy射线照射后培养,制备成肿瘤疫苗并在Ⅱb期临床实验患者的体内产生了针对多种靶抗原的新型抗体。Ho等[40]在异基因造血干细胞移植(hematopoietic stem cell transplantation,HSCT)后,早期使用经IR、腺病毒转导的自体GVAX疫苗进行接种,在接种后诱导强大的免疫反应。Wu等[41]在Ⅱ期研究中证明GVAX和易普利木单抗在联合治疗转移性胰腺导管腺癌中可以促进T细胞在外周和肿瘤微环境中分化为效应记忆表型,增加肿瘤中的M1巨噬细胞。
随着肿瘤疫苗的发展,肿瘤细胞膜和其他细胞膜融合的杂合膜制备的疫苗也进入研究者的视野,DC/多发性骨髓瘤(multiple myeloma,MM)融合疫苗已被证明可诱导MM反应性淋巴细胞的扩增和自体造血细胞移植后临床反应的巩固。在Ⅱ期试验(NCT 02728102)中,Chung等[42]评估了DC/MM融合疫苗的治疗效果,并最终激活肿瘤特异性免疫。由于TCL拥有多种提高抗肿瘤免疫的TAAs,目前已有多种TCL疫苗被用于临床研究。Ogino等[43]在术后随机试验中使用来自胶质瘤干细胞系GBM6-AD的异体细胞TCL疫苗辅助治疗低级别胶质瘤,发现可以诱导外周血中1型细胞因子和趋化因子上调、激活的CD 8+ T细胞增加,并使疫苗反应性CD 8+ T细胞迁移到肿瘤微环境中。由于TCL所展示出的效果,不少研究者也把目光投向TCL+DC的组合:Liau等[44]在胶质母细胞瘤患者中,测试了负载自体肿瘤TCL的DC疫苗(DCVax-L)联合标准治疗胶质母细胞瘤(glioblastoma,GBM)的Ⅱ期临床试验,DC将肿瘤抗原呈递给免疫系统,诱导特异性抗肿瘤免疫应答,激活宿主的抗肿瘤免疫,从而靶向杀死肿瘤细胞,实现对肿瘤生长的抑制,最终延长患者生存期。Bota等通过将患者自体DC与照射后的自体肿瘤起始细胞裂解物共孵育后制备成AV-GBM-1,2年OS为27%[45]。而Carpenter等研究了负载有自体肿瘤裂解物(tumor lysate,TL)的酵母细胞壁颗粒(yeast cell wall particles,YCWPs)离体激发成熟的自体DC的肿瘤裂解液、颗粒负载的树突状细胞疫苗(tumor lysate, particle-loaded, dendritic cell,TLPLDC)和使用涂有硅酸盐的自体TL负载YCWP进行体内DC负载的疫苗TLPO,在该临床试验中,TLPO和TLPLDC都有效地提升了患者的无病生存期和OS,基于此次临床试验的结果,Carpenter等已经开始着手TLPO和TLPLDC的Ⅲ期临床试验[47-49]。
总的来说,TCL疫苗和GVAX疫苗是目前临床上较为主流的肿瘤疫苗种类,并且大部分都取得了不错的进展,除了验证这2种疫苗所蕴含的巨大潜力外,也从侧面说明其他制备策略仍有需要克服的挑战。
-
本文综述了基于ICD策略制备的肿瘤疫苗、基因工程、细胞膜修饰、TCL疫苗的进展与应用,这些疫苗可以大量递送肿瘤抗原并激活广泛的抗肿瘤免疫反应,尽管大规模临床转化仍存在一定问题,但上述几种改造策略增强了工程化肿瘤全细胞疫苗的靶向性和功能性,拓宽了治疗的选择面。不同的修饰策略可以发挥不同的作用,例如,使用肿瘤细胞膜可以避免纳米颗粒被网状内皮系统清除,延长循环时间,同时肿瘤细胞膜的同源肿瘤靶向特性可以进一步增强其免疫刺激特性。在特定递送方面,基因工程提供了更灵活的选择,通过基因修饰,使疫苗可以在安全性和有效性方面通过临床测试。
值得注意的是,免疫抑制微环境是肿瘤来源细胞及纳米疫苗治疗效果的主要障碍[52]。工程化策略通过释放各种免疫调节因子、靶向肿瘤相关基质细胞、负载不同佐剂、减少肿瘤抑制免疫细胞,使免疫抑制微环境朝着有利于治疗的方向发展。这些免疫因子的表达一方面可以通过基因工程来表达,另一方面可以使用外源刺激诱导。尽管近年来免疫检查点抑制剂在肿瘤免疫治疗中得到了广泛应用,但随着临床试验的增加,其不良反应也随之浮现。与检查点抑制剂相比,大多数肿瘤疫苗可以通过局部调节免疫微环境实现免疫治疗,同时避免全身性的毒副作用。许多肿瘤细胞疫苗及纳米疫苗在动物实验中显示出显著的抗肿瘤功效,但只有少数在临床试验中得到了验证,这表明肿瘤疫苗仍有许多问题需要克服。
目前工程化肿瘤全细胞疫苗的稳定性不可控、质量低、产率低,疫苗要进入临床阶段亟需探索更高质量、大规模制备的方法。此外,疫苗的长期安全性尚未得到深入评估,多数生物材料还未获得临床使用许可,这也成为生物材料设计策略的全细胞疫苗临床应用的主要障碍。
最后,尽管新抗原的个性化免疫治疗是当今主流疫苗的开发策略,但其抗原谱单一,且耗费成本巨大,难以构建较为通用、经济的疫苗策略。相比之下,未来肿瘤全细胞疫苗可以在对肿瘤免疫系统更全面、更深入了解的基础上发展。尽管临床试验中部分肿瘤疫苗表现不如预期,但是拓宽了疫苗制备策略,为将来肿瘤疫苗的制备提供了新的思路,研究者可以通过不断调整和改进工程策略来获得更有效的肿瘤疫苗。
Research progress on engineered tumor whole-cell vaccines
-
摘要: 免疫治疗的出现给癌症治疗带来了新的希望。肿瘤疫苗作为免疫治疗的一种前景策略,其抗原来源可分为已鉴定的单一或多个抗原和未鉴定的全肿瘤抗原。目前主流肿瘤疫苗仍以已鉴定的抗原为基础,但有其局限性,基于全肿瘤抗原制备的肿瘤疫苗仍具有独特的优势。全肿瘤抗原疫苗的低免疫原性影响其临床疗效,因此研究人员采用多种策略来改善其免疫原性,如免疫原性死亡、基因工程改造、细胞膜修饰和肿瘤细胞裂解物等,这些策略展现了极大的临床潜力。本文综述近年基于工程化肿瘤全细胞疫苗的研究进展,并探讨其临床进展和应用前景。Abstract: The emergence of immunotherapy has provided new optimism for cancer treatment. Tumor vaccine, a promising immunotherapy strategy, can be categorized into those with identified single or multiple antigens and those with unidentified whole-tumor antigens as their antigenic sources. Currently, mainstream tumor vaccines are still based on identified antigens. However, due to their limitations, tumor vaccines prepared based on whole tumor antigens have unique advantages. However, the low immunogenicity of whole-tumor antigen vaccines affected their clinical efficacy. To improve the immunogenicity, researchers have employed various strategies such as immunogenic death, genetic engineering modifications, cell membrane modifications, and tumor cell lysates, which demonstrated significant clinical potential. The research progress of engineering whole-cell vaccines based on tumor cells in recent years was reviewed in this paper, with a focus on their clinical progress and application prospects.
-
表 1 肿瘤全细胞疫苗的临床试验
疫苗名称 肿瘤模型 疫苗种类 临床试验阶段 参考文献 GVAX 胰腺导管腺癌 基因工程肿瘤细胞 随机试验 [37] GVAX 乳腺癌 基因工程肿瘤细胞 Ⅰ期临床试验 [39] GVAX 髓系白血病 基因工程肿瘤细胞 Ⅱ期临床试验 [40] GVAX 胰腺导管腺癌 基因工程肿瘤细胞 Ⅱ期临床试验 [41] DC/MM 融合膜 骨髓瘤 DC-肿瘤细胞融合 Ⅱ期临床试验 [42] GBM 6-AD 胶质瘤 肿瘤裂解物 随机试验 [43] DCVax-L 胶质母细胞瘤 肿瘤裂解物 Ⅲ期临床试验 [44] AV-GBM-1 胶质母细胞瘤 肿瘤裂解物 Ⅱ期临床试验 [45] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱ期临床试验 [46] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱb期临床试验 [47] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱb期临床试验 [48] TLPLDC 黑色素瘤 肿瘤裂解物 Ⅱb期临床试验 [49] 卵巢癌自体肿瘤疫苗(Vigil) 卵巢癌 自体肿瘤细胞 Ⅱb期临床试验 [50] CSF-470 黑色素瘤 ICD肿瘤细胞 Ⅱ期临床试验 [51] -
[1] LEWIS G D, LI G M, GUO J, et al. The HER2-directed antibody-drug conjugate DHES0815A in advanced and/or metastatic breast cancer: preclinical characterization and phase 1 trial results[J]. Nat Commun, 2024, 15(1): 466. doi: 10.1038/s41467-023-44533-z [2] DE SAUVAGE M A, TORRINI C, NIEBLAS-BEDOLLA E, et al. The ERK inhibitor LY3214996 augments anti-PD-1 immunotherapy in preclinical mouse models of BRAFV600E melanoma brain metastasis[J]. Neuro Oncol, 2024, 26(5): 889-901. doi: 10.1093/neuonc/noad248 [3] XUE Y E, CHE J Y, JI X M, et al. Recent advances in biomaterial-boosted adoptive cell therapy[J]. Chem Soc Rev, 2022, 51(5): 1766-1794. doi: 10.1039/D1CS00786F [4] FAN T, ZHANG M N, YANG J X, et al. Therapeutic cancer vaccines: advancements, challenges, and prospects[J]. Signal Transduct Target Ther, 2023, 8(1): 450. doi: 10.1038/s41392-023-01674-3 [5] TAGLIAMONTE M, CAVALLUZZO B, MAURIELLO A, et al. Molecular mimicry and cancer vaccine development[J]. Mol Cancer, 2023, 22(1): 75. doi: 10.1186/s12943-023-01776-0 [6] SAHIN U, TÜRECI Ö. Personalized vaccines for cancer immunotherapy[J]. Science, 2018, 359(6382): 1355-1360. doi: 10.1126/science.aar7112 [7] DIAO L, LIU M. Rethinking antigen source: cancer vaccines based on whole tumor cell/tissue lysate or whole tumor cell[J]. Adv Sci, 2023, 10(22): e2300121. doi: 10.1002/advs.202300121 [8] SHIREMAN J M, GONUGUNTA N, ZHAO L, et al. GM-CSF and IL-7 fusion cytokine engineered tumor vaccine generates long-term Th-17 memory cells and increases overall survival in aged syngeneic mouse models of glioblastoma[J]. Aging Cell, 2023, 22(7): e13864. doi: 10.1111/acel.13864 [9] AIKINS M E, XU C, MOON J J. Engineered nanoparticles for cancer vaccination and immunotherapy[J]. Acc Chem Res, 2020, 53(10): 2094-2105. doi: 10.1021/acs.accounts.0c00456 [10] ZHANG X, ZHANG H B, GU J M, et al. Engineered extracellular vesicles for cancer therapy[J]. Adv Mater, 2021, 33(14): e2005709. doi: 10.1002/adma.202005709 [11] KORBELIK M. Radiovaccination strategy for cancer treatment integrating photodynamic therapy-generated vaccines with radiotherapy[J]. Int J Mol Sci, 2022, 23(20): 12263. doi: 10.3390/ijms232012263 [12] GALLUZZI L, HUMEAU J, BUQUÉ A, et al. Immunostimulation with chemotherapy in the era of immune checkpoint inhibitors[J]. Nat Rev Clin Oncol, 2020, 17(12): 725-741. doi: 10.1038/s41571-020-0413-z [13] PETRONI G, BUQUÉ A, ZITVOGEL L, et al. Immunomodulation by targeted anticancer agents[J]. Cancer Cell, 2021, 39(3): 310-345. doi: 10.1016/j.ccell.2020.11.009 [14] RODRIGUEZ-RUIZ M E, VITALE I, HARRINGTON K J, et al. Immunological impact of cell death signaling driven by radiation on the tumor microenvironment[J]. Nat Immunol, 2020, 21(2): 120-134. doi: 10.1038/s41590-019-0561-4 [15] SEAVER K, KOURKO O, GEE K, et al. IL-27 improves prophylactic protection provided by a dead tumor cell vaccine in a mouse melanoma model[J]. Front Immunol, 2022, 13: 884827. doi: 10.3389/fimmu.2022.884827 [16] LUO L M, LV M H, ZHUANG X B, et al. Irradiation increases the immunogenicity of lung cancer cells and irradiation-based tumor cell vaccine elicits tumor-specific T cell responses in vivo[J]. Onco Targets Ther, 2019, 12: 3805-3815. doi: 10.2147/OTT.S197516 [17] HUMEAU J, SAUVAT A, CERRATO G, et al. Inhibition of transcription by dactinomycin reveals a new characteristic of immunogenic cell stress[J]. EMBO Mol Med, 2020, 12(5): e11622. doi: 10.15252/emmm.201911622 [18] AHN I E, BRANDER D M, REN Y, et al. Five-year follow-up of a phase 2 study of ibrutinib plus fludarabine, cyclophosphamide, and rituximab as initial therapy in CLL[J]. Blood Adv, 2024, 8(4): 832-841. doi: 10.1182/bloodadvances.2023011574 [19] MONTES DE OCA R, ALAVI A S, VITALI N, et al. Belantamab mafodotin(GSK2857916)drives immunogenic cell death and immune-mediated antitumor responses in vivo[J]. Mol Cancer Ther, 2021, 20(10): 1941-1955. doi: 10.1158/1535-7163.MCT-21-0035 [20] FIELD C S, HERMANS I F, HUNN M K. Whole tumor cell vaccines for glioma immunotherapy[J]. Immunotherapy, 2016, 8(4): 387-389. doi: 10.2217/imt-2015-0022 [21] WONG K K, LI W A, MOONEY D J, et al. Advances in therapeutic cancer vaccines[J]. Adv Immunol, 2016, 130: 191-249. [22] LUO G F, CHEN W H, ZENG X, et al. Cell primitive-based biomimetic functional materials for enhanced cancer therapy[J]. Chem Soc Rev, 2021, 50(2): 945-985. doi: 10.1039/D0CS00152J [23] TSUJIKAWA T, CROCENZI T, DURHAM J N, et al. Evaluation of cyclophosphamide/GVAX pancreas followed by Listeria-mesothelin(CRS-207)with or without nivolumab in patients with pancreatic cancer[J]. Clin Cancer Res, 2020, 26(14): 3578-3588. doi: 10.1158/1078-0432.CCR-19-3978 [24] BERNARDES DE JESUS B, NEVES B M, FERREIRA M, et al. Strategies for cancer immunotherapy using induced pluripotency stem cells-based vaccines[J]. Cancers, 2020, 12(12): 3581. doi: 10.3390/cancers12123581 [25] GUO M, YOU C Z, DOU J. Role of transmembrane glycoprotein mucin 1(MUC1)in various types of colorectal cancer and therapies: Current research status and updates[J]. Biomed Pharmacother, 2018, 107: 1318-1325. doi: 10.1016/j.biopha.2018.08.109 [26] GUO M, LUO B, PAN M, et al. Colorectal cancer stem cell vaccine with high expression of MUC1 serves as a novel prophylactic vaccine for colorectal cancer[J]. Int Immunopharmacol, 2020, 88: 106850. doi: 10.1016/j.intimp.2020.106850 [27] AI X, WANG S, DUAN Y, et al. Emerging approaches to functionalizing cell membrane-coated nanoparticles[J]. Biochemistry, 2021, 60(13): 941-955. doi: 10.1021/acs.biochem.0c00343 [28] ZHAO Z T, FANG L, XIAO P, et al. Walking dead tumor cells for targeted drug delivery against lung metastasis of triple-negative breast cancer[J]. Adv Mater, 2022, 34(33): e2205462. doi: 10.1002/adma.202205462 [29] BERTI C, GRACIOTTI M, BOARINO A, et al. Polymer nanoparticle-mediated delivery of oxidized tumor lysate-based cancer vaccines[J]. Macromol Biosci, 2022, 22(2): e2100356. doi: 10.1002/mabi.202100356 [30] HAN Q J, WANG Y Q, PANG M, et al. STAT3-blocked whole-cell hepatoma vaccine induces cellular and humoral immune response against HCC[J]. J Exp Clin Cancer Res, 2017, 36(1): 156. doi: 10.1186/s13046-017-0623-0 [31] WANG X L, WANG N, YANG Y, et al. Polydopamine nanoparticles carrying tumor cell lysate as a potential vaccine for colorectal cancer immunotherapy[J]. Biomater Sci, 2019, 7(7): 3062-3075. doi: 10.1039/C9BM00010K [32] SHI G N, ZHANG C N, XU R, et al. Enhanced antitumor immunity by targeting dendritic cells with tumor cell lysate-loaded chitosan nanoparticles vaccine[J]. Biomaterials, 2017, 113: 191-202. doi: 10.1016/j.biomaterials.2016.10.047 [33] MA L, DIAO L, PENG Z F, et al. Immunotherapy and prevention of cancer by nanovaccines loaded with whole-cell components of tumor tissues or cells[J]. Adv Mater, 2021, 33(43): e2104849. doi: 10.1002/adma.202104849 [34] ROUFARSHBAF M, ESMAEIL N, AKBARI V. Comparison of four methods of colon cancer cell lysates preparation for ex vivo maturation of dendritic cells[J]. Res Pharm Sci, 2021, 17(1): 43-52. [35] LI X L, ZENG S, HE H P, et al. A hybrid glioma tumor cell lysate immunotherapy vaccine demonstrates good clinical efficacy in the rat model[J]. Onco Targets Ther, 2020, 13: 8109-8124. doi: 10.2147/OTT.S259516 [36] MISHCHENKO T A, TURUBANOVA V D, GORSHKOVA E N, et al. Targeting immunogenic cell death for glioma immunotherapy[J]. Trends Cancer, 2024, 10(1): 8-11. doi: 10.1016/j.trecan.2023.10.005 [37] ZHENG L, DING D, EDIL B H, et al. Vaccine-induced intratumoral lymphoid aggregates correlate with survival following treatment with a neoadjuvant and adjuvant vaccine in patients with resectable pancreatic adenocarcinoma[J]. Clin Cancer Res, 2021, 27(5): 1278-1286. doi: 10.1158/1078-0432.CCR-20-2974 [38] DRANOFF G, JAFFEE E, LAZENBY A, et al. Vaccination with irradiated tumor cells engineered to secrete murine granulocyte-macrophage colony-stimulating factor stimulates potent, specific, and long-lasting anti-tumor immunity[J]. Proc Natl Acad Sci U S A, 1993, 90(8): 3539-3543. doi: 10.1073/pnas.90.8.3539 [39] ANDERSON K S, ERICK T K, CHEN M X, et al. The feasibility of using an autologous GM-CSF-secreting breast cancer vaccine to induce immunity in patients with stage II-III and metastatic breast cancers[J]. Breast Cancer Res Treat, 2022, 194(1): 65-78. doi: 10.1007/s10549-022-06562-y [40] HO V T, KIM H T, BROCK J, et al. GM-CSF secreting leukemia cell vaccination for MDS/AML after allogeneic HSCT: a randomized, double-blinded, phase 2 trial[J]. Blood Adv, 2022, 6(7): 2183-2194. doi: 10.1182/bloodadvances.2021006255 [41] WU A A, BEVER K M, HO W J, et al. A phase II study of allogeneic GM-CSF-transfected pancreatic tumor vaccine(GVAX)with ipilimumab as maintenance treatment for metastatic pancreatic cancer[J]. Clin Cancer Res, 2020, 26(19): 5129-5139. doi: 10.1158/1078-0432.CCR-20-1025 [42] CHUNG D J, SHAH N, WU J, et al. Randomized phase II trial of dendritic cell/myeloma fusion vaccine with lenalidomide maintenance after upfront autologous hematopoietic cell transplantation for multiple myeloma: BMT CTN 1401[J]. Clin Cancer Res, 2023, 29(23): 4784-4796. doi: 10.1158/1078-0432.CCR-23-0235 [43] OGINO H, TAYLOR J W, NEJO T, et al. Randomized trial of neoadjuvant vaccination with tumor-cell lysate induces T cell response in low-grade gliomas[J]. J Clin Invest, 2022, 132(3): e151239. doi: 10.1172/JCI151239 [44] LIAU L M, ASHKAN K, BREM S, et al. Association of autologous tumor lysate-loaded dendritic cell vaccination with extension of survival among patients with newly diagnosed and recurrent glioblastoma: a phase 3 prospective externally controlled cohort trial[J]. JAMA Oncol, 2023, 9(1): 112-121. doi: 10.1001/jamaoncol.2022.5370 [45] BOTA D A, TAYLOR T H, PICCIONI D E, et al. Phase 2 study of AV-GBM-1(a tumor-initiating cell targeted dendritic cell vaccine)in newly diagnosed Glioblastoma patients: safety and efficacy assessment[J]. J Exp Clin Cancer Res, 2022, 41(1): 344. doi: 10.1186/s13046-022-02552-6 [46] CARPENTER E L, VAN DECAR S, ADAMS A M, et al. Prospective, randomized, double-blind phase 2B trial of the TLPO and TLPLDC vaccines to prevent recurrence of resected stage III/IV melanoma: a prespecified 36-month analysis[J]. J Immunother Cancer, 2023, 11(8): e006665. doi: 10.1136/jitc-2023-006665 [47] ADAMS A M, CARPENTER E L, CLIFTON G T, et al. Divergent clinical outcomes in a phase 2B trial of the TLPLDC vaccine in preventing melanoma recurrence and the impact of dendritic cell collection methodology: a randomized clinical trial[J]. Cancer Immunol Immunother, 2023, 72(3): 697-705. doi: 10.1007/s00262-022-03272-8 [48] CHICK R C, FARIES M B, HALE D F, et al. Multi-institutional, prospective, randomized, double-blind, placebo-controlled phase IIb trial of the tumor lysate, particle-loaded, dendritic cell(TLPLDC)vaccine to prevent recurrence in high-risk melanoma patients: a subgroup analysis[J]. Cancer Med, 2021, 10(13): 4302-4311. doi: 10.1002/cam4.3969 [49] VREELAND T J, CLIFTON G T, HALE D F, et al. A phase IIb randomized controlled trial of the TLPLDC vaccine as adjuvant therapy after surgical resection of stage III/IV melanoma: a primary analysis[J]. Ann Surg Oncol, 2021, 28(11): 6126-6137. doi: 10.1245/s10434-021-09709-1 [50] ROCCONI R P, GROSEN E A, GHAMANDE S A, et al. Gemogenovatucel-T (Vigil) immunotherapy as maintenance in frontline stage III/IV ovarian cancer (VITAL): a randomised, double-blind, placebo-controlled, phase 2b trial[J]. Lancet Oncol, 2020, 21(12): 1661-1672. doi: 10.1016/S1470-2045(20)30533-7 [51] PODAZA E, CARRI I, ARIS M, et al. Evaluation of T-cell responses against shared melanoma associated antigens and predicted neoantigens in cutaneous melanoma patients treated with the CSF-470 allogeneic cell vaccine plus BCG and GM-CSF[J]. Front Immunol, 2020, 11: 1147. doi: 10.3389/fimmu.2020.01147 [52] CHEN C, WANG Z H, DING Y, et al. Tumor microenvironment-mediated immune evasion in hepatocellular carcinoma[J]. Front Immunol, 2023, 14: 1133308. doi: 10.3389/fimmu.2023.1133308 -




 下载:
下载: