-
肌肉疲劳通常指肌肉因反复收缩活动而出现的肌力可逆性下降[1]。与此相关,肌肉在一段时间内重复执行收缩以抵抗疲劳的能力,或是长时间维持特定最大自主收缩百分比的能力也被称为肌肉耐力[2]。军事训练、长时间的战斗或不适当的运动都会引起肌肉疲劳,引发肌肉耐力下降,从而影响军事行动和运动成绩[2]。肌肉疲劳通常是急性的,休息后可缓解;也可以是慢性和持续性的,常继发于衰老、制动、药物或疾病,严重时甚至影响生活质量[3]。由于缺乏特异的靶标,目前并无肌肉耐力提升药物上市,安非他明、莫达非尼和咖啡因可以显著改善疲劳,但实质为中枢兴奋剂,存在成瘾、耐受、影响生物节律等风险[4];人参、红景天等天然产物以及维生素和矿物质等营养物质,效果缓慢且不显著,市场亟需靶点明确的抗疲劳药物。
Orosomucoid(ORM)也称α1-酸性糖蛋白(α1-acid glycoprotein,AGP),是一组主要在肝脏合成的分泌蛋白,小鼠中有3种亚型:ORM1, ORM2 和ORM3,而人体中有2种亚型:ORM1和ORM2,其中,ORM1是主要亚型。团队前期研究发现,ORM1是一种内源性的抗疲劳蛋白[5-6],各种形式的疲劳均可诱导肝脏和血清中的ORM显著增加,如啮齿类动物的强迫游泳、跑台和睡眠剥夺模型,以及慢性疲劳综合征人群[5-6]。且ORM1可以正反馈作用于骨骼肌细胞膜上C-C趋化因子受体5型受体(CCR5),并激活腺苷酸活化蛋白激酶(adenylate-activated protein kinase,AMPK),增加肌糖原含量,从而提升肌肉耐力[5-11]。然而ORM需要从血浆中制备,并通过静脉注射给药[12],故难以成药。因此,我们试图寻找一种可以刺激内源性ORM1增加、进而抗肌肉疲劳的药物。
团队前期通过高通量筛选,发现橄榄油提取物橄榄苦苷具有提升肝细胞ORM1表达的潜力,提示其可能具有抗肌肉疲劳活性。橄榄苦苷作为一种天然酚类化合物,其抗炎、抗氧化、神经保护及抗肿瘤等多种药理作用已被广泛研究[13-16],这为其应用于缓解肌肉疲劳提供了潜在的药理学依据。为本研究将进一步确定橄榄苦苷对ORM蛋白表达的促进作用,并评估橄榄苦苷对肌肉耐力的影响,以期为耐力提升药物研发提供新的候选分子。
-
ORM1、β-Actin、β-Tubulin抗体以及抗兔免疫球蛋白G(IgG)二抗购自武汉三鹰公司;化合物橄榄苦苷(97%)购自上海源叶公司;肝糖原、肌糖原检测试剂盒购自武汉伊莱瑞特生物公司。ORM1 ELISA试剂盒购自美国Abcam公司,其他试剂以及仪器设备由本实验室提供。
-
小鼠肝细胞系AML12,购自武汉普诺赛生命科技有限公司。培养液配方:DMEM/F12、10%FBS、10 μg/ml 胰岛素、5.5 μg/ml转铁蛋白、5 ng/ml硒、40 ng/ml 地塞米松以及 1%青链霉素双抗(P/S)。培养条件:5%CO2、37℃恒温孵育箱。用PBS溶液配置浓度30 mmol/L的橄榄苦苷母液,稀释1 000倍后得到的浓度为30 μmol/L工作液,依次梯度稀释3倍后得到浓度为0.3、1、3、10、30 μmol/L工作液,当细胞生长至对数分裂期即进行给药。
-
C57BL/6J 雄性小鼠109只,周龄6~8周,体重(20±2)g,购自杭州子源实验动物科技有限公司,动物实验许可证号:SYXK(沪)2017-0004。小鼠在恒定温度(22℃)和相对湿度(70%)的环境中饲养,12 h光/暗循环照明,8时至20时为照明时间,小鼠可自由获得食物和水。该实验由海军军医大学动物实验伦理委员会批准,所有动物均得到了人道关怀,实验程序严格按照海军军医大学机构动物护理指南进行。
-
77只小鼠随机分为11组,每组7只。其中6组用于药物量效性研究,根据给药剂量不同分为0、1、3、10、30、100 mg/kg剂量组;剩余5组用于药物时效性研究,根据给药天数不同分为0、1、3、7、14 d组。剩下32只小鼠随机分为4组,每组8只,根据上述结果确定最佳给药时间和剂量后给药,用于研究非运动状态下药物对小鼠的影响。将橄榄苦苷溶于生理盐水中,制备不同浓度的橄榄苦苷溶液,按照容积0.1 ml/10 g,通过灌胃给药的方式,适应性喂养1周后给药。按不同给药剂量对小鼠给药7 d,每天一次,随后进行实验;确定最佳给药剂量后,按计划天数给药,每天一次,随后进行实验。转棒实验结束后,小鼠休息7 d,随后按以往分组重新给药后进行负重强迫游泳实验。
-
小鼠于正式测试前进行3 d的适应性训练,分为3个阶段,3个阶段之间无时间间隙:T1阶段,转棒以加速度5 r/min2从静止开始匀加速至速度为5 r/min;T2阶段,更改加速度为10 r/min2,加速至15 r/min后匀速转动2 min;T3阶段,继续以加速度10 r/min2加速至20 r/min后继续匀速2 min。若小鼠在测试过程中掉落,记录掉落时间,待20 min后重新对掉落小鼠开始实验,记录小鼠在转棒上持续的时间。小鼠在进行适应性实验期间训练小鼠体力,加强小鼠的协调能力。正式实验阶段,T1、T2、T3各阶段加速度不变,结束时匀速速度分别达到5、15、18 r/min,记录小鼠转棒持续时间[17]。
-
小鼠于正式测试前进行3 d适应性训练,将小鼠放置在圆柱形玻璃器皿中,该器皿填充了40 cm深的21~23℃的水,以防止小鼠尾巴接触底部。在每只小鼠尾端3 cm处系上一个金属环,适应性训练的第1、2、3天,小鼠负重自身体重的3%,在水中分别进行10、20、30 min游泳训练。正式测量时,负重5%,测量从小鼠进入水中开始,在沉入水下10 s后结束[18]。
-
取小鼠腓肠肌和比目鱼肌于4%多聚甲醛中固定24 h后,常规石蜡包埋切片处理,随后PAS染色观察肌肉形态及糖原含量。
-
取小鼠肝脏组织20~30 mg,放入2 ml研磨管中,按照1∶10比例加入含有蛋白酶抑制剂和磷酸酶抑制剂的裂解液,研磨离心后取上清液,BCA法蛋白定量后经SDS-PAGE分离,蛋白电转至PVDF膜,将PVDF膜在5%牛奶中封闭1 h,加入1∶1 000的一抗,4℃孵育过夜,TBST洗涤,加入酶标二抗室温1 h,PVDF膜置于化学发光图像分析仪进行拍摄保存。
-
实验数据采用GraphPad Prism 9.0软件进行统计与分析。各组数据以均数±标准差($ \overline{x} $±s)表示,如各组数据满足正态性和方差齐性,两组之间采用独立样本t检验,多组间采用单因素方差分析;如服从正态分布不满足方差齐性,选用Welch矫正后的ANOVA检验;若不服从正态分布,则进行非参数检验,采用Kruskal-Wallish检验法进行比较。整个分析过程中,以P<0.05为差异具有统计学意义。
-
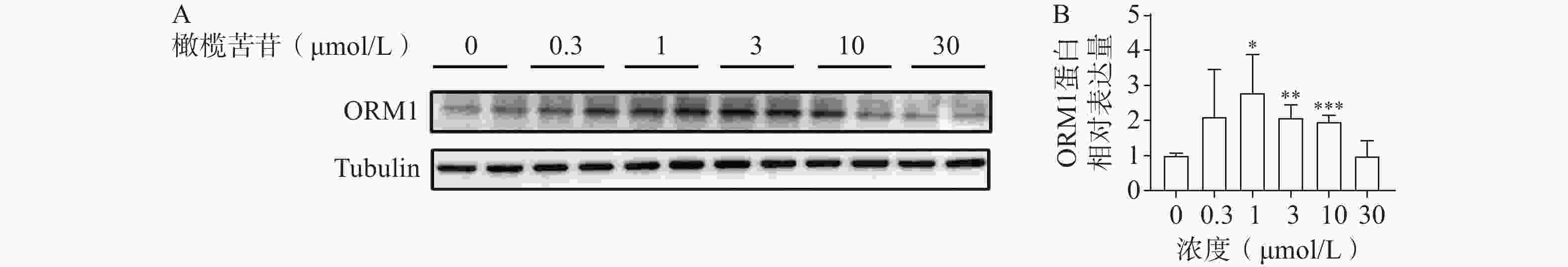
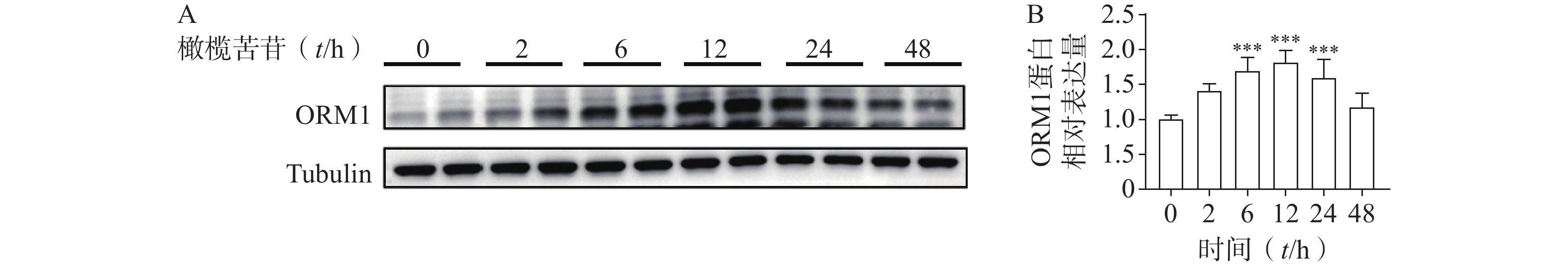
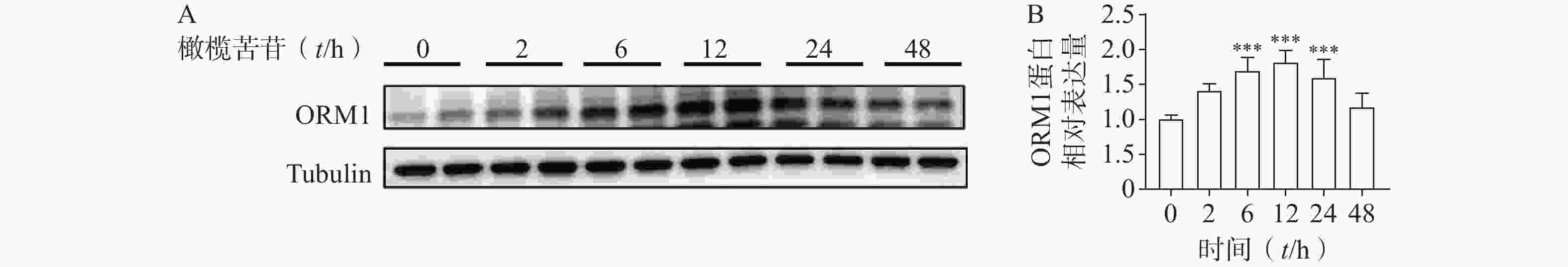
为验证橄榄苦苷能否在肝细胞中提升ORM1表达,首先进行时间-效应研究,即在统一收样前0、2、6、12、24、48 h加入相同浓度的橄榄苦苷,首次给药浓度根据文献报告选用10 μmol/L[19]。结果显示,给橄榄苦苷后2 h即有上升趋势,6~24 h之间,肝细胞中ORM1的含量显著提高,在12 h时,该效应到达高峰(图1A、1B);在确定最佳时间为12 h后,进行剂量-效应研究,即给药浓度设置0.3、1、3、10、30 μmol/L。结果显示,在0.3 μmol/L剂量下即有提升趋势,当橄榄苦苷剂量在1、3 μmol/L时,肝细胞中ORM1的含量显著提高(图2A、2B)。
-
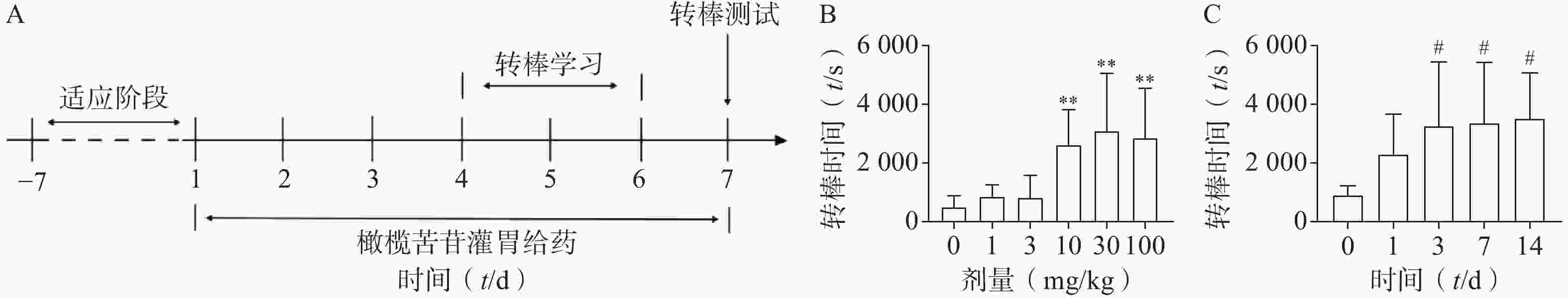
橄榄苦苷在体外实验中能稳定促进抗疲劳靶蛋白ORM1提升,强烈提示该药物具有抗肌肉疲劳的潜力,继续体内实验,研究药物对肌肉耐力的影响。首先采用转棒实验对小鼠进行评估。转棒实验作为一种行为学测试,通过小鼠在转棒上停留时间的变化,来评估运动能力,从而间接反映肌肉疲劳情况[20]。该实验依赖小鼠的平衡协调能力,适应性训练可以帮助小鼠掌握“主动踏步”策略,也是确保实验数据可靠的关键,避免因技能缺失导致的假阳性结果。采用渐进增加转速的方式,每天上午、下午各训练30 min,训练3 d,具体适应给药流程图如图3A所示。不同给药剂量下,小鼠转棒停留时间部分服从正态分布,采用Kruskal-Wallis检验,实验结果显示,在10、30、100 mg/kg的给药剂量下,小鼠在转棒上停留的时间显著延长(图3B);选取30 mg/kg作为最佳剂量,分别给药1、3、7、14 d,小鼠转棒停留时间服从正态分布,但未通过方差齐性检验(P<0.05),选用Welch矫正后的ANOVA检验,结果显示,给药超过1 d以上,小鼠在转棒上停留时间即呈延长趋势,给药≥7 d时差异显著(图3C)。
-
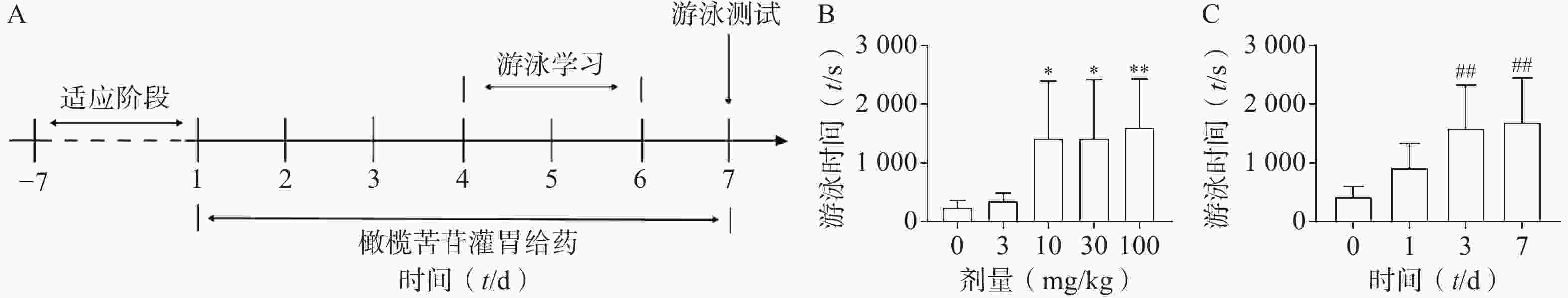
小鼠休息7 d后重新给药,给药结束后进行负重游泳实验(图4A)。负重游泳实验作为一种动物行为学测试,通过测量动物在特定负重下游泳的总时间或力竭时间,可以间接反映其肌肉在持续运动状态下的耐力表现,进而用于评估肌肉疲劳。不同剂量或不同给药时间下,小鼠负重游泳时间均符合正态分布,并通过方差齐性检验(P>0.05),进行单因素方差分析。结果显示,在剂量为10~100 mg/kg,给药7 d的情况下,小鼠游泳时间显著延长(图4B),基于量效实验结果,选取最佳剂量(中间剂量)30 mg/kg进行时效研究。随后,分别给药1、3、7 d发现,小鼠的负重游泳时间呈延长趋势,且当给药时间≥3 d时均存在差异显著(图4C)。
-
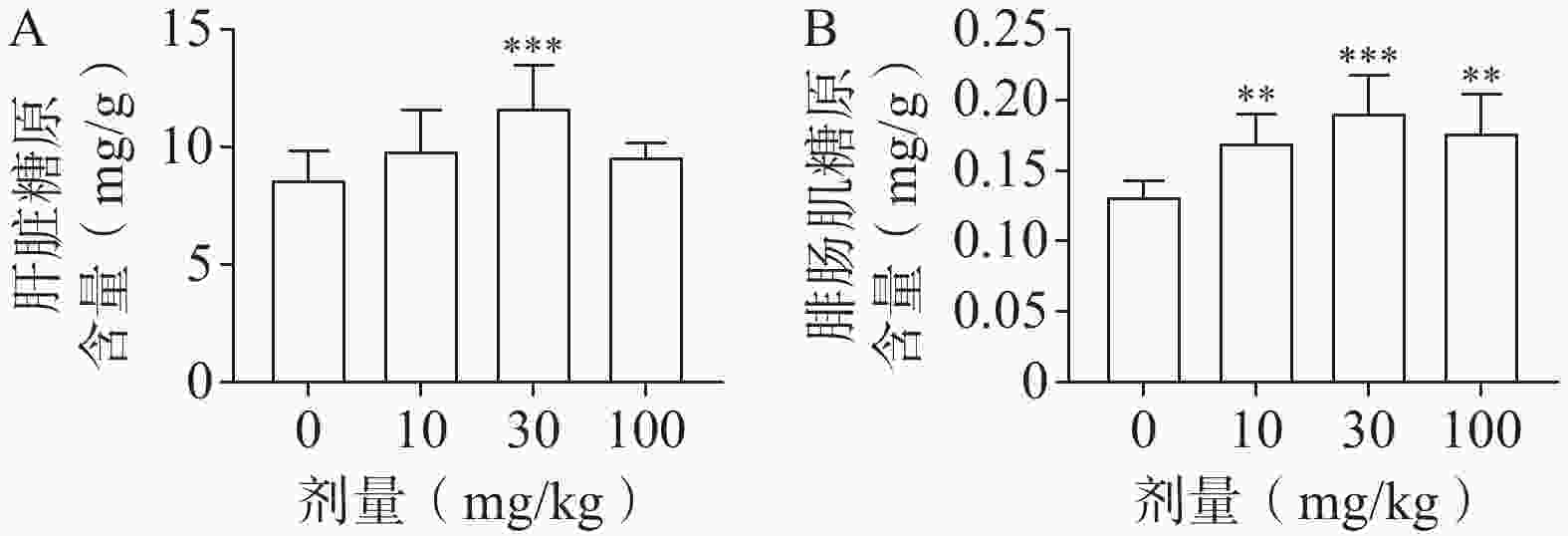
近年来,越来越多的研究证实了糖原与肌肉疲劳之间的关系,糖原作为骨骼肌中的主要能量储备,其水平直接影响肌肉的耐力和疲劳程度,增加糖原含量可以显著改善肌肉耐力[5,21]。本团队前期研究发现,ORM1可以通过增加肌肉糖原含量来提高肌肉耐力。因此,在这里我们试图探索橄榄苦苷是否有类似的效应。采用未进行任何人为运动干预小鼠作为研究对象,通过糖原检测试剂盒检测肝脏和肌肉组织的糖原含量。肝脏或肌肉中糖原含量均符合正态分布,并通过方差齐性检验(P>0.05),采用单因素方差分析发现,橄榄苦苷在30 mg/kg时显著增加肝脏中糖原含量(图5A),在30~100 mg/kg剂量范围内显著增加肌肉糖原含量(图5B);通过碘酸雪夫染色(Periodic Acid-Schiff,PAS),对橄榄苦苷给药后的肌肉组织进行糖原含量的观察。实验结果表明,与0 mg/kg组相比,给药组中代表糖原的洋红色染色部分颜色更深,染色区域明显增大,并在30 mg/kg剂量组最为明显(图6)。
-
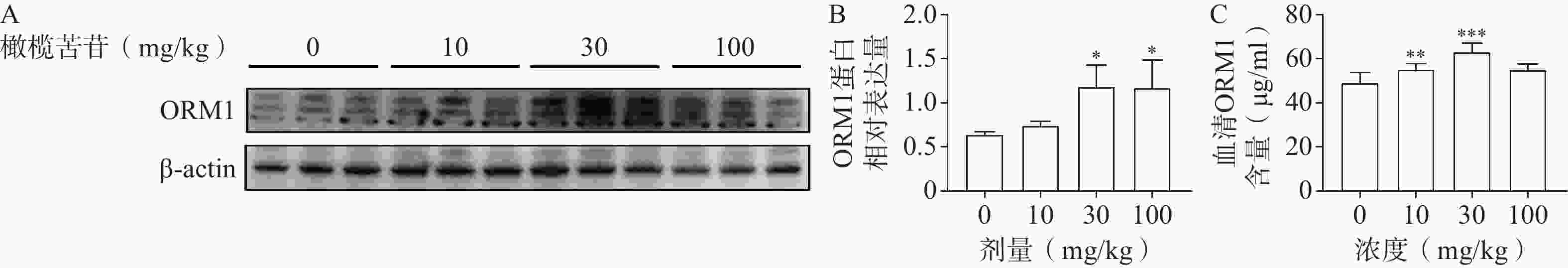
通过2种模型确认橄榄苦苷的抗肌肉疲劳效应后,我们进一步探究橄榄苦苷能否在体内提升ORM1表达。ORM1主要由肝脏分泌,入血后进入效应器官。因此,这里使用蛋白免疫印迹分析技术检测肝脏组织中的ORM1,并使用ELISA技术检测血清中ORM1。选择10、30、100 mg/kg作为研究剂量,无任何人为运动干预小鼠经过适应性饲养后,通过灌胃给药7 d后,解剖小鼠得到血清和肝脏组织并进行检测。所有均符合正态分布,且通过方差齐性检验(P>0.05),采用单因素方差分析发现,肝脏(图7A、7B)和血清(图7C)中的ORM1含量均显著升高。
-
目前,针对肌肉疲劳的特定药物尚未问世,原因在于缺乏明确的靶点。非特定的治疗手段,如营养补充剂、免疫疗法(例如IgG和干扰素α2),以及药物(如类固醇、莫达非尼和咖啡因),虽已在实验中被广泛应用,但在多项研究中往往显示出微弱、无结论或负面的效果[22-26]。自20世纪初以来,研究逐渐揭示了碳水化合物作为运动燃料的重要性,肌肉糖原对运动表现的关键作用在众多研究中得到了充分证实。当糖原储备不足时,肌肉耐力将显著下降。进一步的研究表明,糖原的减少直接导致肌浆网中Ca2+的释放减少,从而影响肌肉的收缩能力与疲劳程度[27]。因此,改善能量代谢,尤其是提升糖原含量,或许是治疗肌肉疲劳的有效途径。
基于团队之前的发现,内源性抗疲劳蛋白ORM1通过CCR5-AMPK通路提升肌肉中的糖原含量与运动耐力。本研究结果表明天然化合物橄榄苦苷不仅展现出抗疲劳的显著效果,同时也能够显著提升体内ORM1蛋白的表达水平及骨骼肌中的糖原储备。此结果提示,橄榄苦苷的抗疲劳功能与调节ORM1的表达密切相关。
综上所述,本研究以橄榄苦苷与靶蛋白ORM1之间的关系为切入点,对小鼠在给药后的运动耐力变化进行了细致评估,明确指出橄榄苦苷能够显著提升肌肉耐力,展现出其抗疲劳的潜力。这为橄榄苦苷在治疗肌肉疲劳方面提供了坚实的科学依据。然而,文中尚未验证橄榄苦苷是否通过ORM1发挥其抗疲劳的功能,未来的研究将进一步采用ORM1基因敲除鼠进行深入评估,以探讨橄榄苦苷对ORM1的具体调控机制。
Study on the role of oleuropein in enhancing muscle endurance
-
摘要:
目的 Orosomucoid1(ORM1)是抗疲劳药物研发新靶标,前期研究提示橄榄苦苷(oleuropein,OLE)是上调ORM1表达的潜在候选分子。本研究将进一步确定橄榄苦苷对ORM1蛋白表达的促进作用,评估其对肌肉耐力的影响。 方法 采用蛋白免疫印迹检测橄榄苦苷对肝细胞和肝组织中ORM1蛋白表达的影响;采用转棒实验、负重游泳实验,评估橄榄苦苷对肌肉耐力的影响;采用试剂盒检测肝脏和肌肉组织中的糖原含量;采用PAS染色观察腓肠肌糖原沉积;采用ELISA试剂盒检测血清ORM1蛋白表达。 结果 橄榄苦苷以时间和剂量依赖的方式增加肝细胞ORM1蛋白表达,同时也以时间和剂量依赖的方式提高小鼠强迫游泳和转棒时间,升高肝组织ORM1表达,增加血清中ORM1含量,并提升肝脏和肌肉组织中的糖原含量。 结论 橄榄苦苷可能通过增加体内ORM1的表达水平,提升骨骼肌糖原储备,从而增强肌肉耐力。 Abstract:Objective Orosomucoid1 (ORM1) is a novel target in the quest for anti-fatigue pharmacotherapy. Preliminary investigations have illuminated oleuropein (OLE) as a promising candidate molecule, poised to enhance ORM1 expression. To elucidate the influence of OLE on ORM1 protein expression and assess its ramifications on muscle endurance. Methods The impact of OLE on ORM1 protein expressions within hepatocytes and liver tissue was meticulously quantified through Western blotting; the effects of OLE on muscle endurance were evaluated via the rotarod and forced swimming tests; glycogen content within liver and muscle tissues was determined utilizing a specialized kit; and PAS staining was employed to visualize glycogen deposition in the gastrocnemius muscle. Results OLE demonstrated a capacity to elevate ORM1 protein expression in hepatocytes in a time- and dose-dependent manner, concurrently prolonging the duration of swimming and rotarod performance in mice, also in a time- and dose-dependent manner. Furthermore, OLE augmented ORM1 expression in liver tissue, elevated serum ORM1 levels, and enhanced glycogen reserves within the liver and muscle. Conclusion OLE may serve to amplify muscle endurance by elevating ORM1 levels in vivo and augmenting glycogen stores within skeletal muscle. -
Key words:
- oleuropein /
- muscle fatigue /
- orosomucoid1(ORM1) /
- glycogen /
- muscle endurance
-
-
[1] ALLEN D G, LAMB G D, WESTERBLAD H. Skeletal muscle fatigue: cellular mechanisms[J]. Physiol Rev, 2008, 88(1): 287-332. doi: 10.1152/physrev.00015.2007 [2] WAN J J, QIN Z, WANG P Y, et al. Muscle fatigue: general understanding and treatment[J]. Exp Mol Med, 2017, 49(10): e384. doi: 10.1038/emm.2017.194 [3] CONSTANTIN-TEODOSIU D, CONSTANTIN D. Molecular mechanisms of muscle fatigue[J]. Int J Mol Sci, 2021, 22(21): 11587. doi: 10.3390/ijms222111587 [4] KIM D. Practical use and risk of modafinil, a novel waking drug[J]. Environ Health Toxicol, 2012, 27: e2012007. doi: 10.5620/eht.2012.27.e2012007 [5] SUN Y, ZHANG Z X, LIU X. Orosomucoid(ORM)as a potential biomarker for the diagnosis of chronic fatigue syndrome (CFS)[J]. CNS Neurosci Ther, 2016, 22(3): 251-252. [6] LEI H, SUN Y, LUO Z M, et al. Fatigue-induced orosomucoid 1 acts on C-C chemokine receptor type 5 to enhance muscle endurance[J]. Sci Rep, 2016, 6: 18839. doi: 10.1038/srep18839 [7] BERGER E G, ALPERT E, SCHMID K, et al. Immunohistochemical localization of alpha1-acid-glycoprotein in human liver parenchymal cells[J]. Histochemistry, 1977, 51(4): 293-296. doi: 10.1007/BF00494364 [8] LEE Y S, CHOI J W, HWANG I, et al. Adipocytokine orosomucoid integrates inflammatory and metabolic signals to preserve energy homeostasis by resolving immoderate inflammation[J]. J Biol Chem, 2010, 285(29): 22174-22185. doi: 10.1074/jbc.M109.085464 [9] CORREALE M, BRUNETTI N D, DE GENNARO L, et al. Acute phase proteins in atherosclerosis(acute coronary syndrome)[J]. Cardiovasc Hematol Agents Med Chem, 2008, 6(4): 272-277. [10] BARANIUK J N, CASADO B, MAIBACH H, et al. A Chronic Fatigue Syndrome - related proteome in human cerebrospinal fluid[J]. BMC Neurol, 2005, 5: 22. doi: 10.1186/1471-2377-5-22 [11] QIN Z, WAN J J, SUN Y, et al. ORM promotes skeletal muscle glycogen accumulation via CCR5-activated AMPK pathway in mice[J]. Front Pharmacol, 2016, 7: 302. doi: 10.3389/fphar.2016.00302 [12] LUO Z M, LEI H, SUN Y, et al. Orosomucoid, an acute response protein with multiple modulating activities[J]. J Physiol Biochem, 2015, 71(2): 329-340. doi: 10.1007/s13105-015-0389-9 [13] MARTORELL M, FORMAN K, CASTRO N, et al. Potential therapeutic effects of oleuropein aglycone in Alzheimer’s disease[J]. Curr Pharm Biotechnol, 2016, 17(11): 994-1001. doi: 10.2174/1389201017666160725120656 [14] BEDOUHENE S, MOULTI-MATI F, DANG P M, et al. Oleuropein and hydroxytyrosol inhibit the N-formyl-methionyl-leucyl-phenylalanine-induced neutrophil degranulation and chemotaxis via AKT, p38, and ERK1/2 MAP-Kinase inhibition[J]. Inflammopharmacology, 2017, 25(6): 673-680. doi: 10.1007/s10787-017-0367-7 [15] KIM M H, MIN J S, LEE J Y, et al. Oleuropein isolated from Fraxinus rhynchophylla inhibits glutamate-induced neuronal cell death by attenuating mitochondrial dysfunction[J]. Nutr Neurosci, 2018, 21(7): 520-528. doi: 10.1080/1028415X.2017.1317449 [16] AHMAD FAROOQI A, FAYYAZ S, SILVA A S, et al. Oleuropein and cancer chemoprevention: the link is hot[J]. Molecules, 2017, 22(5): 705. doi: 10.3390/molecules22050705 [17] 尚培骏, 姬乃春, 杨锦雯, 等. 基于APP/PS1双转基因小鼠与野生型小鼠比较综述学习记忆相关行为学实验优缺点和注意事项[J]. 中国实验动物学报, 2023, 31(8): 969-984. [18] YANG Z Q, SUNIL C, JAYACHANDRAN M, et al. Anti-fatigue effect of aqueous extract of Hechong(Tylorrhynchus heterochaetus)via AMPK linked pathway[J]. Food Chem Toxicol, 2020, 135: 111043. doi: 10.1016/j.fct.2019.111043 [19] AMANI F, ALLAHBAKHSHIAN FARSANI M, GHOLAMI M, et al. The protective effect of oleuropein against radiation-induced cytotoxicity, apoptosis, and genetic damage in cultured human lymphocytes[J]. Int J Radiat Biol, 2021, 97(2): 179-193. doi: 10.1080/09553002.2020.1793014 [20] HERRERA J J, MCALLISTER C M, SZCZESNIAK D, et al. High-intensity exercise training using a rotarod instrument(RotaHIIT)significantly improves exercise capacity in mice[J]. Physiol Rep, 2024, 12(9): e15997. [21] CHEN F, ZHANG Z, ZHANG H M, et al. Activation of α7 nicotinic acetylcholine receptor improves muscle endurance by upregulating orosomucoid expression and glycogen content in mice[J]. J Cell Biochem, 2024, 125(9): e30630. doi: 10.1002/jcb.30630 [22] LUKASKI H C. Vitamin and mineral status: effects on physical performance[J]. Nutrition, 2004, 20(7-8): 632-644. doi: 10.1016/j.nut.2004.04.001 [23] KRISHNAMURTHI R V, FEIGIN V L, FOROUZANFAR M H, et al. Global and regional burden of first-ever ischaemic and haemorrhagic stroke during 1990-2010: findings from the Global Burden of Disease Study 2010[J]. Lancet Glob Health, 2013, 1(5): e259-e281. doi: 10.1016/S2214-109X(13)70089-5 [24] LEE J S, KIM H G, HAN J M, et al. Anti-fatigue effect of Myelophil in a chronic forced exercise mouse model[J]. Eur J Pharmacol, 2015, 764: 100-108. doi: 10.1016/j.ejphar.2015.06.055 [25] XU Y X, ZHANG J J. Evaluation of anti-fatigue activity of total saponins of Radix notoginseng[J]. Indian J Med Res, 2013, 137(1): 151-155. [26] LEDINEK A H, SAJKO M C, ROT U. Evaluating the effects of amantadin, modafinil and acetyl-L-carnitine on fatigue in multiple sclerosis: result of a pilot randomized, blind study[J]. Clin Neurol Neurosurg, 2013, 115(Suppl 1): S86-S89. [27] ØRTENBLAD N, WESTERBLAD H, NIELSEN J. Muscle glycogen stores and fatigue[J]. J Physiol, 2013, 591(18): 4405-4413. doi: 10.1113/jphysiol.2013.251629 -




 下载:
下载: