-
疏肝通络胶囊为空军特色医学中心(本院)药剂科生产的医院制剂,批准文号为:空制字(2022)F002022。处方由蒺藜、柴胡、菟丝子、石菖蒲、远志、水蛭等6味药材组成,具有疏肝理气,活血通络,补肾振痿,肝肾通调的功能[1]。临床上用于治疗功能性阳痿和动脉供血不足性阳痿[1-2]。为了更好地控制该制剂的质量,采用薄层色谱(thin layer chromatography,TLC)法对药材柴胡、远志和石菖蒲的活性成分进行定性鉴别。以处方中君药柴胡的主要活性成分柴胡皂苷a为定量指标[3-4]进行含量测定,以期完善疏肝通络胶囊的质量标准。
-
Agilent HP 1100型高效液相色谱仪(Agilent Technologies),JA3003型电子天平(上海恒平科学仪器有限公司),XS205DU型电子分析天平(瑞士梅特勒-托利多仪器有限公司),KQ-500DE型超声波清洗器(昆山市超声仪器有限公司),水浴锅(东南仪诚仪器有限公司)。
-
柴胡对照药材(批号:120992-201109,中国食品药品检定研究院)、远志对照药材(批号:120989-201107,中国食品药品检定研究院)、石菖蒲对照药材(批号:121098-201406,中国食品药品检定研究院)、柴胡皂苷a对照品(纯度:92.0%,批号:110777-201309,中国食品药品检定研究院)、疏肝通络胶囊(批号:151210、151211、151212,由本院药剂科制剂室生产,规格:0.25 g/粒,每盒40粒),乙腈、甲醇(色谱纯,Fisher公司),其他试剂均为分析纯,水为超纯水。
-
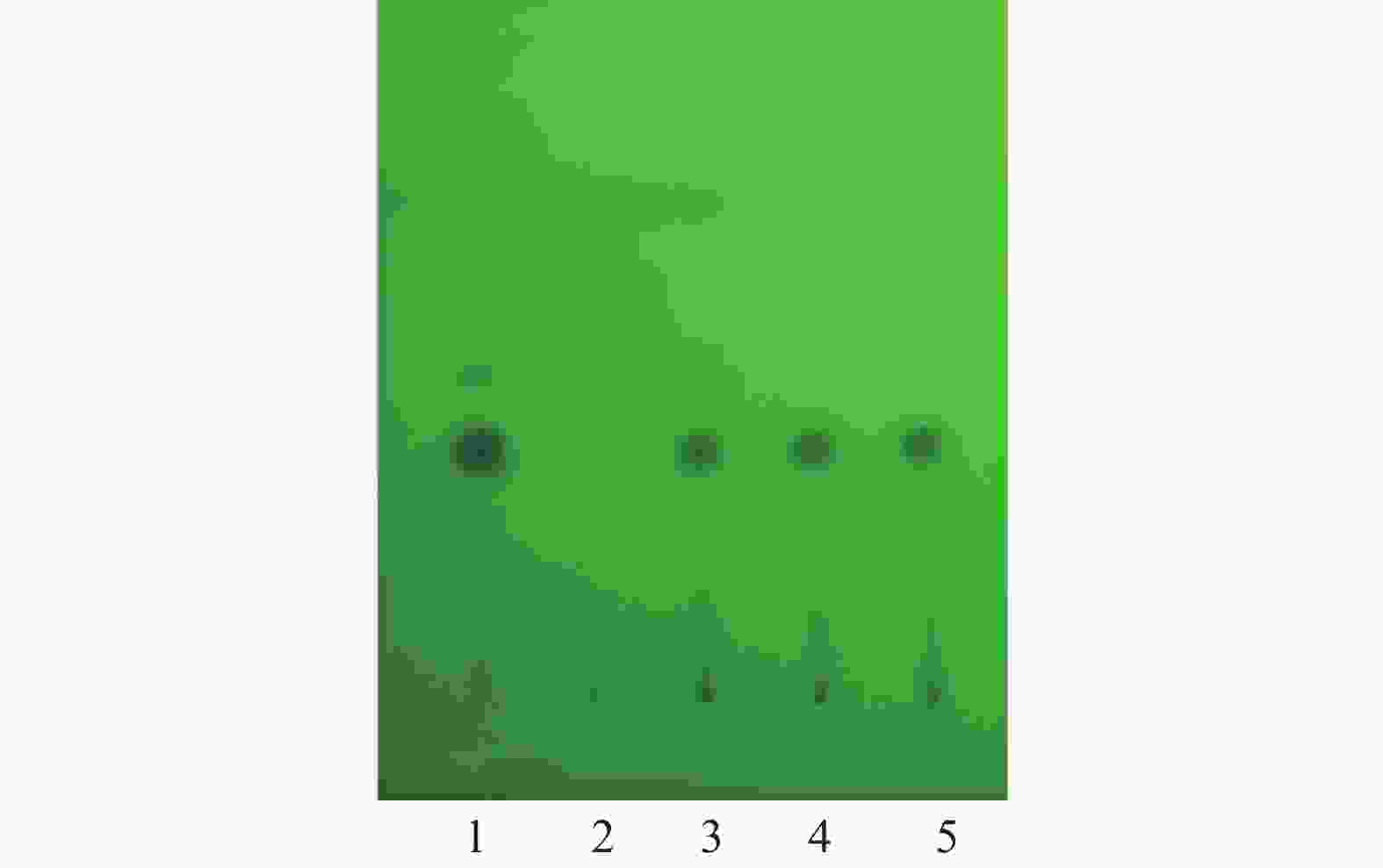
取疏肝通络胶囊内容物2.0 g,加水30 ml,制成混悬液,用三氯甲烷50 ml萃取,取水层再用正丁醇50 ml萃取,正丁醇液减压浓缩至干,用甲醇1 ml溶解,作为供试品溶液。另取柴胡对照药材1 g,加水20 ml煎煮1 h,滤过,滤液用正丁醇40 ml萃取,正丁醇液减压浓缩至干,加甲醇1 ml溶解,作为对照药材溶液。按处方制备缺柴胡的阴性样品,按供试品溶液的制备方法操作,制备阴性对照溶液。照TLC法(《中国药典》2025年版四部通则0502)试验[5],取上述3种溶液,分别点于同一块用羧甲基纤维素钠(CMC-Na)为黏合剂的硅胶G薄层板上,以三氯甲烷−甲醇−水(6∶1∶0.1)为展开剂,展开、晾干,喷洒2%香草醛浓硫酸溶液,80℃加热显色,供试品色谱中与对照药材色谱相应位置上,显相同的蓝色斑点[6-7],且阴性无干扰,结果见图1。
-
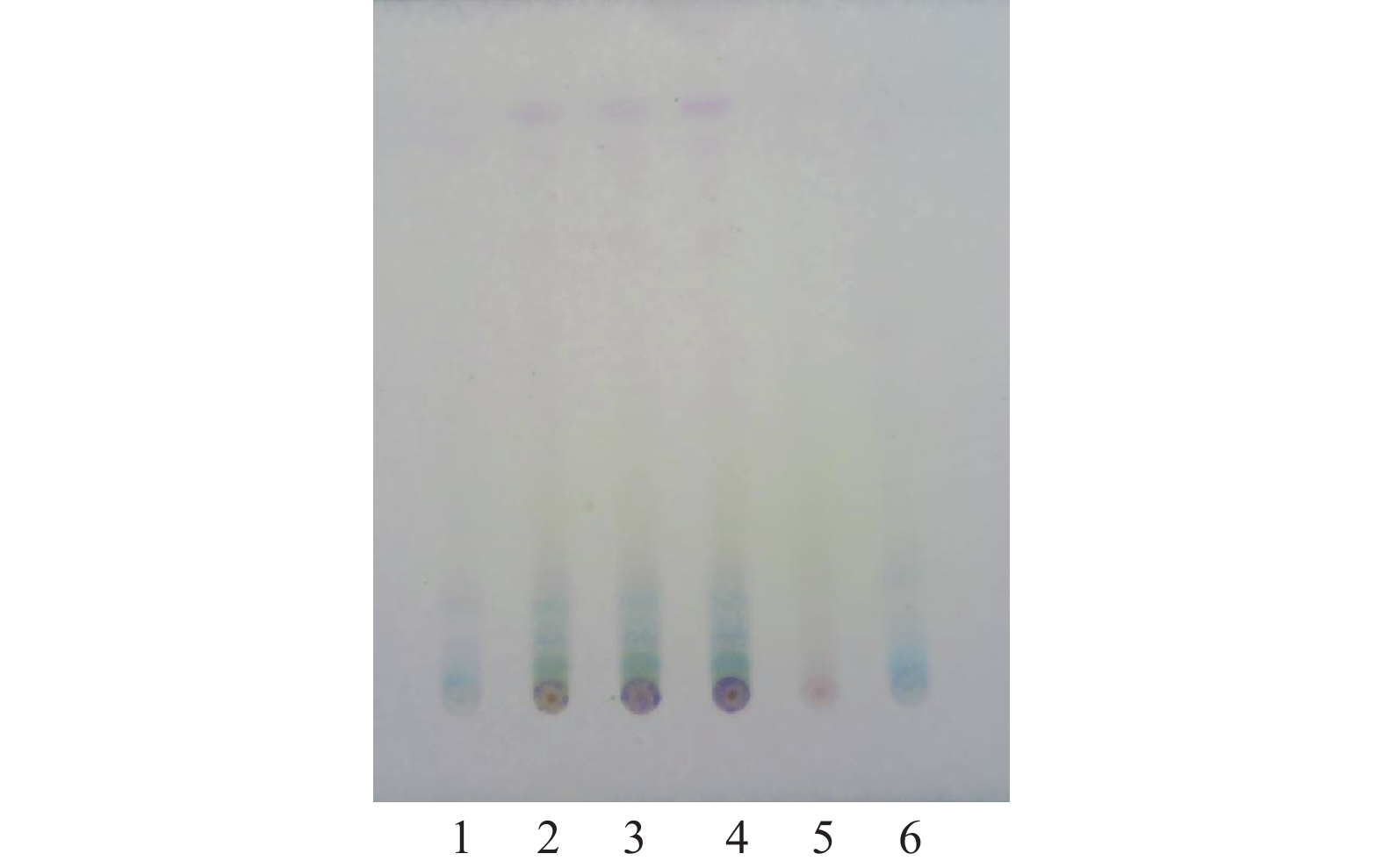
取疏肝通络胶囊内容物10.0 g,加水30 ml,制成混悬液,用乙酸乙酯50 ml萃取,弃去上层乙酸乙酯,水层加盐酸3 ml,加热回流3 h,取出放凉,用乙酸乙酯50 ml萃取,回收乙酸乙酯至干,加甲醇1 ml溶解,作为供试品溶液。另取远志对照药材1 g,用70%乙醇20 ml浸泡24 h,滤过,滤液减压回收乙醇,残渣加水20 ml,盐酸2 ml,加热回流水解3 h,取出放凉,用乙酸乙酯40 ml萃取,回收乙酸乙酯至干,残渣用1 ml甲醇溶解,作为对照药材溶液。按处方制备缺远志的阴性样品,按供试品溶液的制备方法操作,制备阴性对照溶液。照TLC法(《中国药典》2025年版四部通则0502)试验,取上述3种溶液,分别点于同一块用CMC-Na为黏合剂的硅胶GF254板上,以石油醚−乙酸乙酯−冰醋酸(8∶2∶0.5)为展开剂展开,晾干,置紫外光灯(254 nm)下检视,在供试品色谱中,与对照药材色谱相应位置上,显相同颜色的斑点[8-9],结果见图2。
-
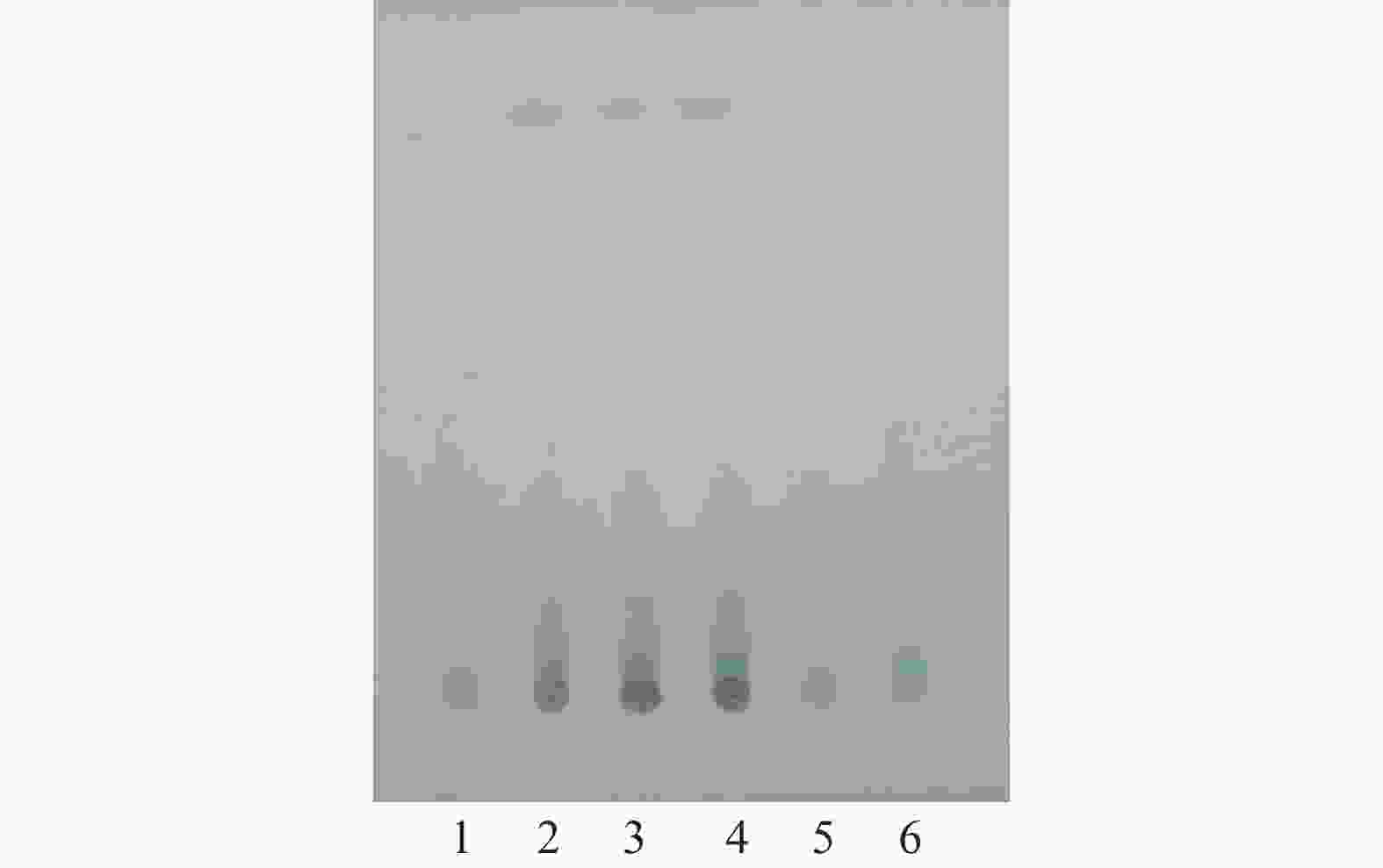
取疏肝通络胶囊内容物1.0 g,加石油醚(60~90℃)20 ml,加热回流1 h,滤过,滤液蒸干,残渣加石油醚(60~90℃)1 ml使溶解,作为供试品溶液。另取石菖蒲对照药材0.3 g,同法制成对照药材溶液。按处方制备缺石菖蒲的阴性样品,按供试品溶液的制备方法操作,制备阴性对照溶液。照TLC法(《中国药典》2025年版四部通则0502)试验,吸取上述3种溶液,分别点于同一CMC−Na为黏合剂的硅胶GF254板上,以环己烷−乙酸乙酯(4∶1)为展开剂,展开,晾干,置紫外光灯(254 nm)下检视,在供试品色谱中,与对照药材色谱相应位置上,显相同颜色的主斑点[10],结果见图3。
-
色谱柱为Venusil XBP C18柱(4.6 mm×150 mm,5 μm),流动相:乙腈−水(40∶60,V/V),流速:1.0 ml/min,柱温:30℃,检测波长:210 nm,进样量:20 μl[11-12]。
-
取柴胡皂苷a对照品适量,精密称定,加甲醇溶解稀释,制成浓度为500 μg/ml的对照品储备液。
-
取本品5粒内容物研磨均匀,取粉末0.6 g,精密称定,置具塞锥形瓶中,加入含5%浓氨试液的甲醇溶液25 ml,密塞,超声处理30 min,滤过,用甲醇20 ml分2次洗涤容器及药渣,洗液与滤液合并,回收溶剂至干。残渣加甲醇溶解,转移至10 ml量瓶中,定容至刻度,摇匀滤过,取续滤液,即得。
-
按疏肝通络胶囊处方及制剂工艺,制备缺少柴胡药材的阴性样品,按“2.2.3”项下方法制备阴性对照溶液。
-
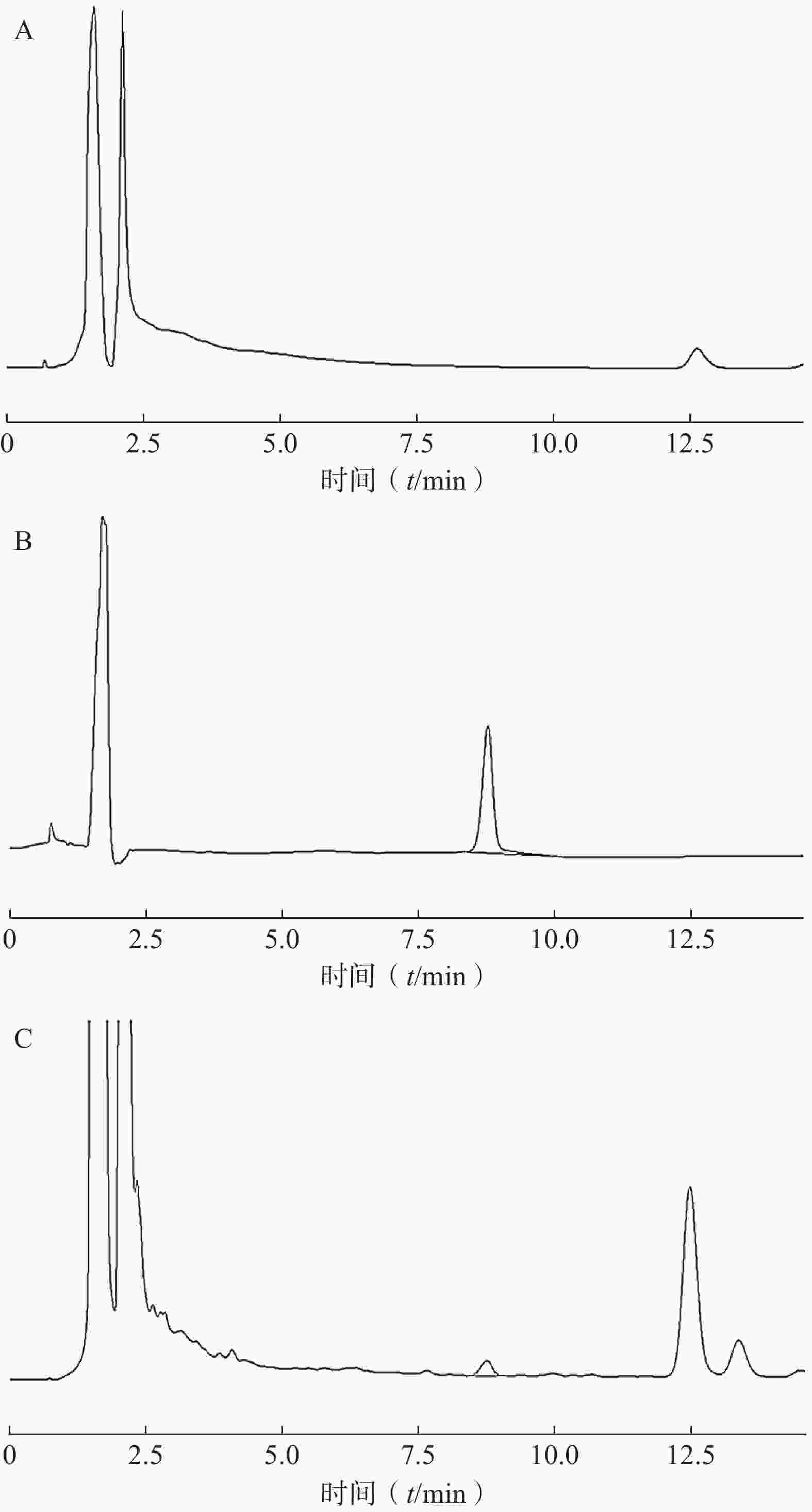
分别精密吸取阴性对照溶液、柴胡皂苷a 对照品溶液、供试品溶液各20 μl,按“2.2.1”项下色谱条件进样,记录色谱图。实验结果表明,该方法专属性良好,阴性对照溶液相应位置没有吸收峰,表明其他成分对测定无干扰,结果见图4。
-
分别精密吸取“2.2.2”项下的对照品储备液适量,分别配制成不同浓度(μg/ml)的对照品溶液,按“2.2.1”项下色谱条件分析,计算峰面积,以柴胡皂苷a峰面积(Y)为纵坐标,柴胡皂苷a浓度(X,μg/ml)为横坐标,进行线性回归,绘制标准曲线。结果表明,柴胡皂苷a在25.0~500.0 μg/ml浓度范围内线性关系良好,回归方程为Y = 305.02X+ 2 189.4,r=0.999 9。
-
精密吸取250 μg/ml的对照品溶液,重复进样6次,按“2.2.1”项下色谱条件进行测定,记录峰面积。结果显示,柴胡皂苷a峰面积的RSD值为0.32 %,说明仪器精密度良好,符合含量测定的要求。
-
取同一批号疏肝通络胶囊样品6份(批号:151211),按“2.2.3”项下方法制备供试品溶液,滤过,取续滤液,按“2.2.1”项下色谱条件进行测定,记录峰面积并计算含量,结果显示:柴胡皂苷a的平均含量为3.068 mg/g,RSD为2.67%,表明该方法的重复性良好。
-
取“2.2.3”项下方法制备的供试品溶液(批号:
151211 ),分别于0、2、4、6、8、12、24 h时按“2.2.1”项下色谱条件进行测定,记录峰面积,结果柴胡皂苷a峰面积的RSD为1.28%,表明供试品溶液在24 h内稳定。 -
取同一批次已知含量的样品9份(批号:151211),分别精密加入柴胡皂苷a对照品溶液,按“2.2.3”项下方法,配制低、中、高3种不同浓度的溶液,每个浓度平行配制3份。滤过,取续滤液按“2.2.1”项下色谱条件进行测定,记录峰面积并计算加样回收率。结果显示,柴胡皂苷a的平均加样回收率为97.00%,RSD值为2.60%,说明该方法回收率符合要求,结果见表1。
表 1 疏肝通络胶囊中柴胡皂苷a的加样回收率试验结果(n=9)
取样量(m/g) 柴胡皂苷a含量(m/mg) 加入量(m/mg) 测得量(m/mg) 回收率(%) 平均回收率(%) RSD值(%) 0.600 1 1.798 1.600 3.359 97.52 97.00 2.60 0.600 0 1.798 1.600 3.382 98.97 0.600 1 1.798 1.600 3.401 100.14 0.600 1 1.798 2.000 3.646 92.40 0.600 1 1.798 2.000 3.802 100.16 0.600 1 1.798 2.000 3.706 95.40 0.600 1 1.798 2.400 4.118 96.64 0.600 1 1.798 2.400 4.086 95.33 0.600 1 1.798 2.400 4.113 96.44 -
取疏肝通络胶囊3批(批号分别为:
151210 、151211 和151212 ),按“2.2.3”项下方法制备供试品溶液,按“2.2.1”项下色谱条件进行测定,记录峰面积并计算含量,结果见表2。表 2 疏肝通络胶囊中柴胡皂苷a含量测定结果($ \overline{x}\pm s, $n=6)
批号 柴胡皂苷a含量(mg/粒) 平均含量(mg/粒) 151210 0.7384 0.7357 ±0.0040.7329 151211 0.8065 0.8192 ±0.0180.8318 151212 0.7955 0.7923 ±0.0050.7890 -
皂苷类成分大多没有紫外吸收,且样品处理较复杂。而柴胡皂苷a和柴胡皂苷d仅在紫外末端有吸收,检测结果易受试剂干扰,故不易进行定量。目前,柴胡皂苷的测定方法主要为HPLC法,流动相多为甲醇−水,乙腈−水进行梯度洗脱。本研究参照2025年版《中国药典(一部)》柴胡项下柴胡皂苷a和柴胡皂苷d含量测定的流动相条件:乙腈−水75%→10%(0~50 min)10%(50~55 min)[13-14],并结合其他相关文献[15],最终采用“2.2.1”项下的洗脱条件。同时按照药典规定的波长,选择210 nm为测定波长。结果显示,柴胡皂苷a在210 nm处无杂质峰干扰,峰形对称,分离度良好。
-
参考2025版《中国药典(一部)》中柴胡的含量测定方法,本实验首选浓氨试液作为基础提取溶剂。同时,以成分个数和含量为依据,分别采用5%浓氨试液的甲醇溶液和5%浓氨试液的乙醇溶液对疏肝通络胶囊进行提取,结果表明5%浓氨试液的甲醇溶液提取成分多,峰分离度好,相对含量高。超声时间选择20、30、40 min进行考察,结果发现超声时间30、40 min效果优于20 min。最终,本实验选择5%浓氨试液的甲醇溶液作为提取溶剂,超声提取30 min。
-
在对疏肝通络胶囊中各味中药进行鉴别时,笔者对蒺藜、菟丝子进行了TLC鉴别,结果显示供试品色谱与对照药材色谱相应位置上无相同特征斑点或者斑点不明显,故未纳入标准。《中国药典》2025年版所收载成方制剂中柴胡的薄层鉴别多采用正丁醇振摇萃取,本实验将样品经三氯甲烷脱脂处理后同法进行萃取处理,能够有效减少杂质成分的干扰。柴胡、远志、石菖蒲对照药材色谱图与供试品色谱图在相同位置上显示相同颜色的斑点,后续可增加标准对照品以进一步鉴别。
-
疏肝通络胶囊处方中蒺藜、柴胡为君药,菟丝子为臣药,配伍石菖蒲、远志、水蛭等佐药。以柴胡为君药的复方,以抗抑郁、抗炎、抗肿瘤、治疗肝病、治疗肺病等为其主要作用[16],且柴胡皂苷a和柴胡皂苷d是其发挥药效的主要成分[17-19]。研究发现,柴胡皂苷a和柴胡皂苷d在胃酸条件和肠道菌群作用下代谢成不同的皂苷/皂苷元[20],其中,柴胡皂苷a的原型药物在血浆、尿液、粪便等样本中均有检出,而柴胡皂苷d在胃液环境中孵育30 min即可完全转化为柴胡皂苷b2[21],有关其原型药物的研究未见报道。同时,柴胡皂苷会引起不同程度的肝、神经、心脏损伤以及溶血毒性,以柴胡皂苷d的毒性最强[22]。综合考虑药效、药动学及毒性作用,本试验采用柴胡皂苷a作为含量测定项。
不论是单体提取物、复方制剂还是中药汤剂,蒺藜均被大量应用于勃起功能障碍。蒺藜总皂苷是其主要活性成分。经体内代谢研究发现,蒺藜总皂苷大多被水解代谢为极性较小的苷元类成分。基于蒺藜总皂苷复杂的体内代谢过程,本文未对其具体的单体成分进行定量分析。
本研究对院内制剂疏肝通络胶囊中柴胡皂苷a的含量进行测定,方法简单快速,准确可靠,稳定性和重现性好,可行性强。同时完善了疏肝通络胶囊中主要药材的TLC鉴别,为评价和控制疏肝通络胶囊的质量提供了科学依据。
Identification and content determination of active components in Shugantongluo capsules
-
摘要:
目的 建立疏肝通络胶囊的薄层色谱鉴别和含量测定方法,为疏肝通络胶囊的质量控制提供方法学参考和借鉴。 方法 采用薄层色谱(TLC)法对胶囊中柴胡、远志和石菖蒲进行定性鉴别;采用HPLC法测定柴胡皂苷a的含量,色谱柱为Venusil XBP C18 柱(4.6 mm×150 mm,5 μm);流动相为乙腈−水(40∶60,V/V),流速:1.0 ml/min,柱温:30℃,检测波长:210 nm,进样量:20 μl。 结果 TLC鉴别图斑点显色清晰,分离效果良好,专属性强。柴胡皂苷a在25.00~500.0 μg/ml范围内浓度与峰面积线性关系良好(r=0.999 9);平均回收率为97.00%,RSD为2.60%。 结论 该方法操作简便、结果准确、专属性和重复性良好,可用于疏肝通络胶囊的质量控制。 Abstract:Objective To establish the method of thin layer chromatography (TLC) for identification and content quantitative determination of Shugantongluo capsules, and provide methodological reference for the quality control of Shugantongluo capsules. Methods Bupleuriradix, polygala tenuifolia yuanzhi, and acorus tatarinowii rhizoma were identified by TLC qualitatively. The content of Saikosaponin-a was determined by HPLC method. The chromatography was performed on Venusil XBP C18(L) (4.6 mm×150 mm, 5 μm) with a stable temperature of 30℃. The mobile phase in isocratic elution consists of acetonitrile-water (40∶60, V/V) at the flow rate of 1.0 ml/min with an injection volume of 20 μl. The detection wavelength was set at 210 nm. Results Clear spots were obtained with good separation in TLC identification which was highly specific. The Saikosaponin-a at the range of 25.00-500.0 μg/ml was linear with peak area (r=0.999 9), the average recovery rate was 97.00%, and RSD was 2.60%. Conclusion These methods was easy to operate with accurate results, with good specificity and reproducibility, which can be uesd for the quality control for Shugantongluo capsules. -
Key words:
- Shugantongluo capsules /
- TLC /
- HPLC /
- Saikosaponin-a
-
表 1 疏肝通络胶囊中柴胡皂苷a的加样回收率试验结果(n=9)
取样量(m/g) 柴胡皂苷a含量(m/mg) 加入量(m/mg) 测得量(m/mg) 回收率(%) 平均回收率(%) RSD值(%) 0.600 1 1.798 1.600 3.359 97.52 97.00 2.60 0.600 0 1.798 1.600 3.382 98.97 0.600 1 1.798 1.600 3.401 100.14 0.600 1 1.798 2.000 3.646 92.40 0.600 1 1.798 2.000 3.802 100.16 0.600 1 1.798 2.000 3.706 95.40 0.600 1 1.798 2.400 4.118 96.64 0.600 1 1.798 2.400 4.086 95.33 0.600 1 1.798 2.400 4.113 96.44 表 2 疏肝通络胶囊中柴胡皂苷a含量测定结果($ \overline{x}\pm s, $n=6)
批号 柴胡皂苷a含量(mg/粒) 平均含量(mg/粒) 151210 0.7384 0.7357 ±0.0040.7329 151211 0.8065 0.8192 ±0.0180.8318 151212 0.7955 0.7923 ±0.0050.7890 -
[1] 韦仕福, 胡海翔, 徐少强, 等. 疏肝通络胶囊治疗勃起功能障碍的临床观察[J]. 中国性科学, 2017, 26(7): 81-83. [2] SAEED M, MUNAWAR M, BI J B, et al. Promising phytopharmacology, nutritional potential, health benefits, and traditional usage of Tribulus terrestris L. herb[J]. Heliyon, 2024, 10(4): e25549. doi: 10.1016/j.heliyon.2024.e25549 [3] 张晓利, 胡威利, 吴银, 等. 柴胡皂苷A对糖尿病大鼠肾结构和功能的保护作用及机制研究[J]. 广州中医药大学学报, 2020, 37(7): 1347-1353. doi: 10.13359/j.cnki.gzxbtcm.2020.07.026 [4] 江楠, 于靖, 杨莉, 等. 中药柴胡皂苷药理作用的研究进展[J]. 环球中医药, 2018, 11(5): 796-800. doi: 10.3969/j.issn.1674-1749.2018.05.047 [5] 国家药典委员会. 中华人民共和国药典(四部)[S]. 北京: 中国医药科技出版社, 2025: 101. [6] 王畅. 柴桂解郁开心颗粒的制备工艺及质量标准研究[D]. 长春: 长春中医药大学, 2018. [7] 杨净尧, 邱智东, 王仁广, 等. 柴桂解郁颗粒质量标准研究[J]. 长春中医药大学学报, 2020, 36(3): 491-494. doi: 10.13463/j.cnki.cczyy.2020.03.025 [8] 潘杰, 甘杰华, 郑晓英, 等. 蜜远志配方颗粒质量标准的研究[J]. 中成药, 2017, 39(4): 751-755. doi: 10.3969/j.issn.1001-1528.2017.04.018 [9] 杨超, 邓晓鸿, 周娟. 复方桔梗止咳片的质量标准研究[J]. 中国药房, 2019, 30(22): 3074-3078. doi: 10.6039/j.issn.1001-0408.2019.22.10 [10] 黎奕明, 眭道顺. 石菖蒲的薄层鉴别及β-细辛醚的含量测定[J]. 中药新药与临床药理, 2009, 20(4): 369-370. doi: 10.3321/j.issn:1003-9783.2009.04.024 [11] 王永杰. HPLC-DAD同时测定柴胡口服液中2种柴胡皂苷的含量[J]. 微量元素与健康研究, 2021, 38(1): 57-59. [12] 苟小军, 黄强. HPLC法测定柴胡疏肝胶囊中柴胡皂苷a、d的含量[J]. 现代中药研究与实践, 2014, 28(5): 65-67. [13] 姬莎莎, 刘红波, 朱华旭, 等. 北柴胡标准汤剂的制备与质量评价研究[J]. 现代中医药, 2023, 43(2): 102-108. doi: 10.13424/j.cnki.mtcm.2023.02.021 [14] 国家药典委员会. 中华人民共和国药典(一部)[S]. 北京: 中国医药科技出版社, 2025: 301. [15] 杨新雪, 梁进京, 董蕊. 柴胡-白芍药对配方颗粒指纹图谱的建立及多指标性成分含量测定[J]. 天然产物研究与开发, 2024, 36(4): 572-580. [16] 王震寰, 赵幻希, 赵孟雅, 等. 柴胡皂苷A·D与柴胡复方药理活性和机制的研究进展[J]. 安徽农业科学, 2023, 51(20): 25-28,35. [17] 黄冬芳, 韦金玉, 梁洁, 等. 柴胡质量标志物的预测分析[J]. 中华中医药学刊, 2021, 39(10): 126-132. doi: 10.13193/j.issn.1673-7717.2023.04.006 [18] SANDS B, YUN S, MENDENHALL A R. Introns control stochastic allele expression bias[J]. Nat Commun, 2021, 12(1): 6527. doi: 10.1038/s41467-021-26798-4 [19] ZHU Y C, LAI Y. Pharmacological properties and derivatives of saikosaponins-a review of recent studies[J]. J Pharm Pharmacol, 2023, 75(7): 898-909. doi: 10.1093/jpp/rgad052 [20] 宋登鹏, 王雪芹, 王永慧, 等. 柴胡皂苷类化合物体内代谢途径及其代谢产物的研究进展[J]. 药物评价研究, 2019, 42(7): 1460-1465. [21] Shimizu K, Amagaya S, Ogihara Y. Structural transformation of saikosaponins by gastric juice and intestinal flora[J]. J Pharmacobiodyn, 1985, 8(9): 718-725. doi: 10.1248/bpb1978.8.718 [22] 仇慧鑫, 张淑敏, 舒乐新, 等. 柴胡的毒性辨析及影响因素研究进展[J]. 中草药, 2023, 54(18): 6150-6158. -




 下载:
下载: