-
溃疡性结肠炎(ulcerative colitis,UC)是一种损害结直肠黏膜的慢性、非特异性炎症反应,以腹痛、腹泻、黏液脓血便为主要临床症状[1]。近20年来,UC全球患病率逐年升高,到2025年我国UC患者将达150万例[2]。UC的诊断、治疗复杂而昂贵,经典西药5-氨基水杨酸制剂、糖皮质激素、免疫抑制剂和生物制剂仅可缓解患者症状,且存在周期长、副作用大、价格昂贵等缺点。研究表明,中药,特别是中药成方制剂,有助于缓解UC患者临床症状、增强美沙拉嗪药物疗效、减轻患者激素依赖、提高患者生活质量,这为UC的治疗提供了新的选择。愈肠颗粒是上海长海医院自研制剂,主要用于治疗慢性结肠炎,由白豆蔻、大血藤、党参等九味中药配伍而成。愈肠颗粒在临床应用20多年,疗效确切,价格低廉,深受广大患者信任。已有研究表明,它增加2,4,6-三硝基苯磺酸(TNBS)处理的UC大鼠的体质量,改善UC大鼠便血和腹泻症状,降低UC大鼠结肠损伤程度,促进溃疡愈合[3]。然而,愈肠颗粒治疗UC的分子机制尚不清楚。因此,本研究拟应用网络药理学和分子对接技术研究愈肠颗粒治疗UC的分子机制,为UC的治疗提供参考。
-
应用TCMSP 数据库(http://tcmspw.com/tcmsp.php)[4]和Herbal Ingredients' Targets Platform(HIT,http://www.badd-cao.net:
2345 /)[5-6]数据库检索愈肠颗粒八味主要中药豆蔻、大血藤、党参、黄柏、羌活、乌梅、乌药和薏苡仁的活性成分,其中赤石脂为矿物质,未进入研究范围。以参数口服吸收利用度(OB)≥ 30%、药物相似性(DL)≥ 0.18为标准,筛选获得愈肠颗粒的活性成分。使用TCMSP和HIT两个数据库研究愈肠颗粒作用靶点,应用UniProt 数据库(https://www.uniprot.org)确认、规范靶点信息,最终获取愈肠颗粒的作用靶点信息。 -
以ulcerative colitis为关键词在Gene Cards 数据库(https://www.genecards.org)、CTD数据库(https://ctdbase.org/)和DisGeNET 数 据 库 (http://www.disgenet.org)检索UC疾病相关靶点,整理、合并结果,删去重复值,获得UC的疾病靶点。
-
应用Venny 2.1.0 可视化平台(https://bioinfogp.cnb.csic.es/tools/venny/)获取愈肠颗粒作用靶点与UC疾病靶点的交集靶点,其为愈肠颗粒治疗UC的潜在作用靶点。将愈肠颗粒的组方中药、活性成分及交集靶点导入到Cytoscape3.10.1软件,绘制中药-活性成分-交集靶点可视化网络。应用Network Analyzer插件对该网络进行拓扑分析,研究愈肠颗粒治疗UC的核心活性成分。
-
应用STRING(https://string-db.org)数据库分析交集靶点,以蛋白质种类为“Homo sapiens”,置信度(medium confidence)≥0.4为筛选条件,隐藏游离节点,构建交集靶点的蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络。利用Cytoscape3.10软件的CytoNCA插件工具对交集靶点进行拓扑学分析,研究愈肠颗粒治疗UC的关键靶点。
-
应用David数据库(https://david.ncifcrf.gov)对交集靶点进行GO功能和KEGG通路富集分析。利用微生信在线工具(http://www.bioinformatics.com.cn/)绘制GO条形图与KEGG气泡图,并进行可视化分析。
-
将“中药-活性成分-交集靶点”网络中介中心度值排名前5位的核心活性成分和PPI 网络中介中心度值排名前5位关键靶点进行分子对接。应用PubChem 数据库(https://pubchem.ncbi.nlm.nih.gov)下载核心活性成分2D结构的sdf格式文件,利用PDB数据库(https://www.rcsb.org)下载关键靶点三维晶体结构,应用MOE软件进行分子对接,根据Score打分结果进行分析。
-
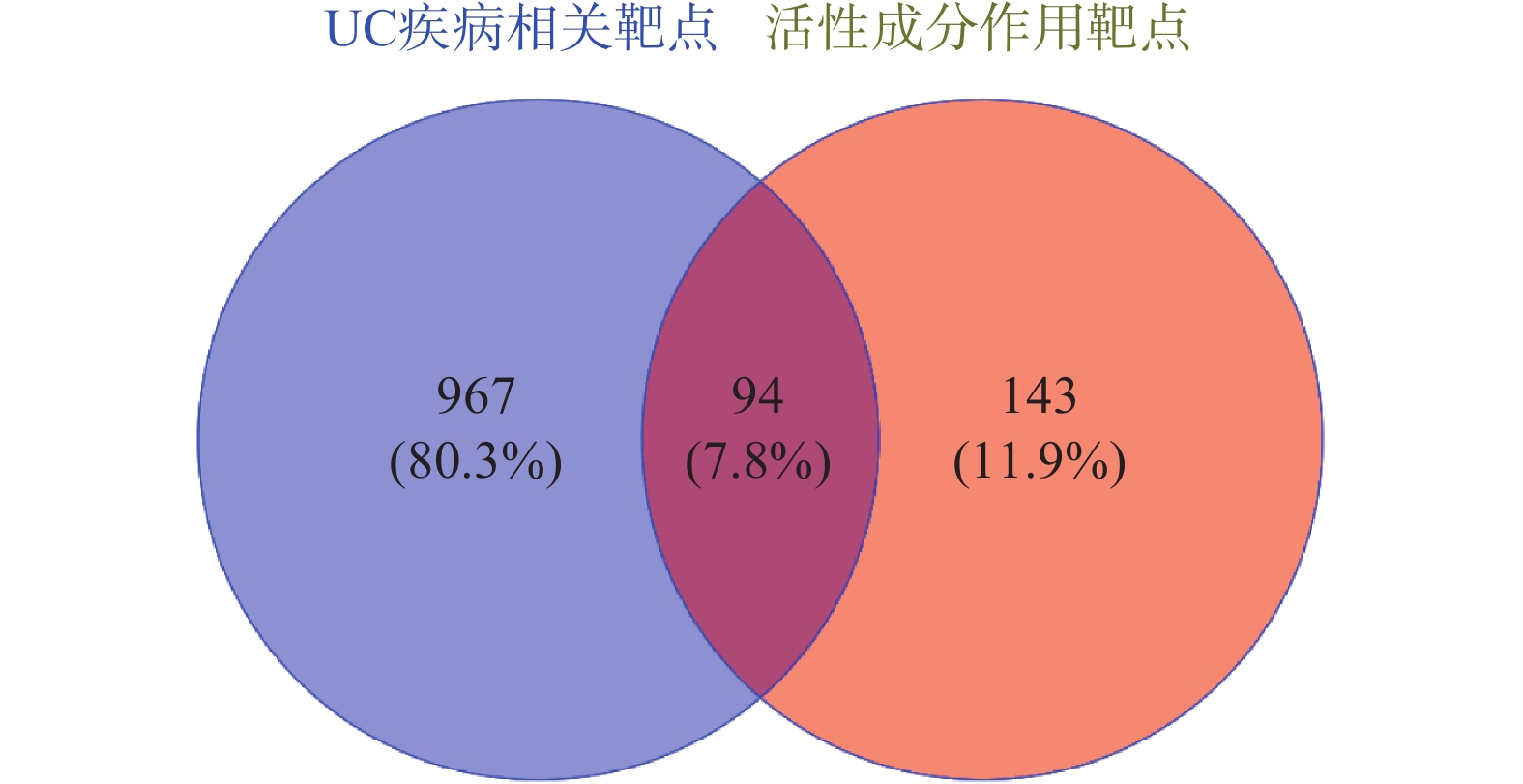
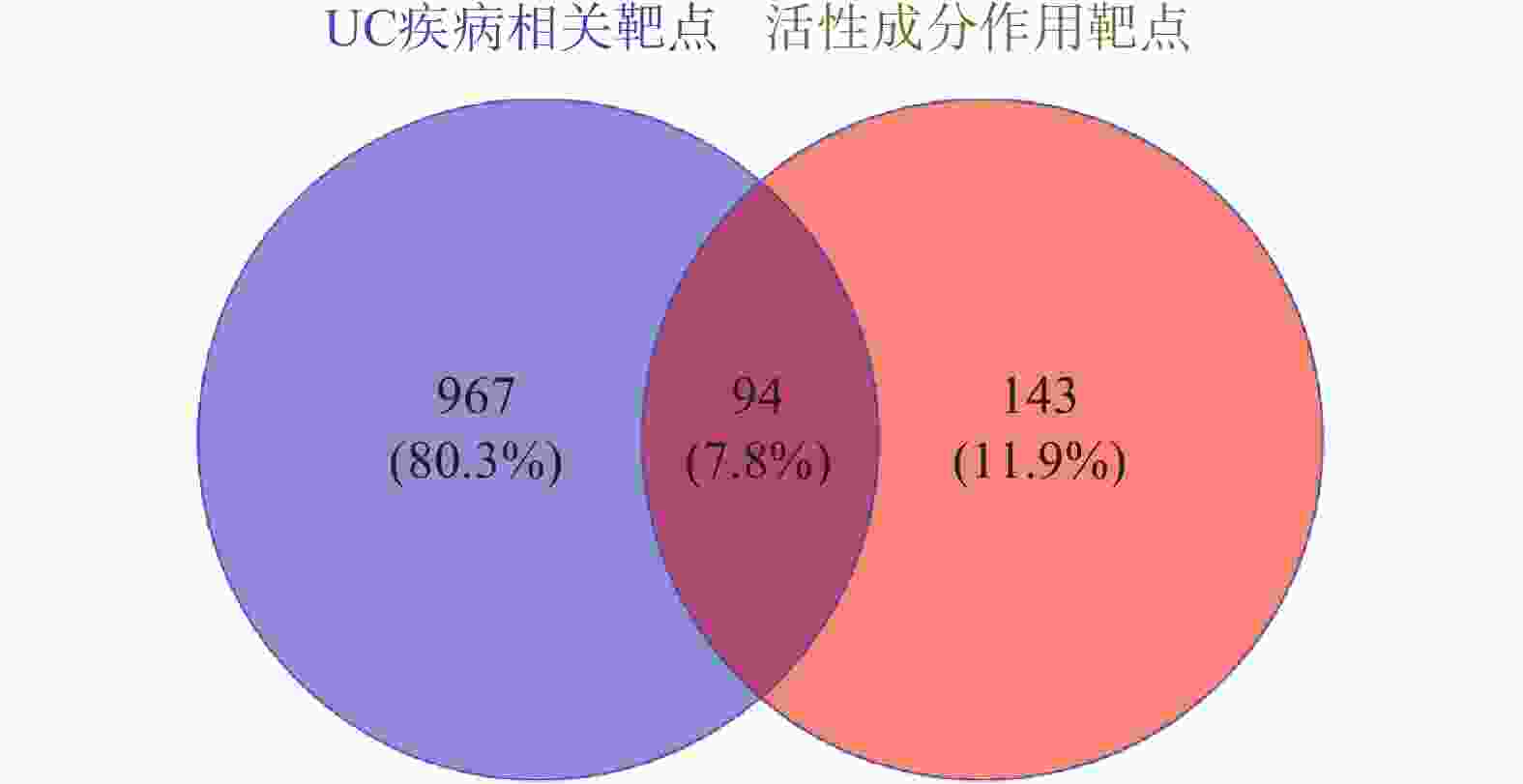
应用TCMSP和HIT数据库检索愈肠颗粒活性成分和作用靶点,基于OB、DL条件筛选,删去重复值,共获取98个活性成分及 237个作用靶点;使用GeneCards、CTD和DisGeNET数据库检索筛选共获得UC疾病靶点
1061 个;应用Venny2.1.0可视化平台绘制维恩图,获取二者交集靶点。结果如图1所示,愈肠颗粒与UC的交集靶点共94个,这表明愈肠颗粒可通过多靶点作用于UC。 -
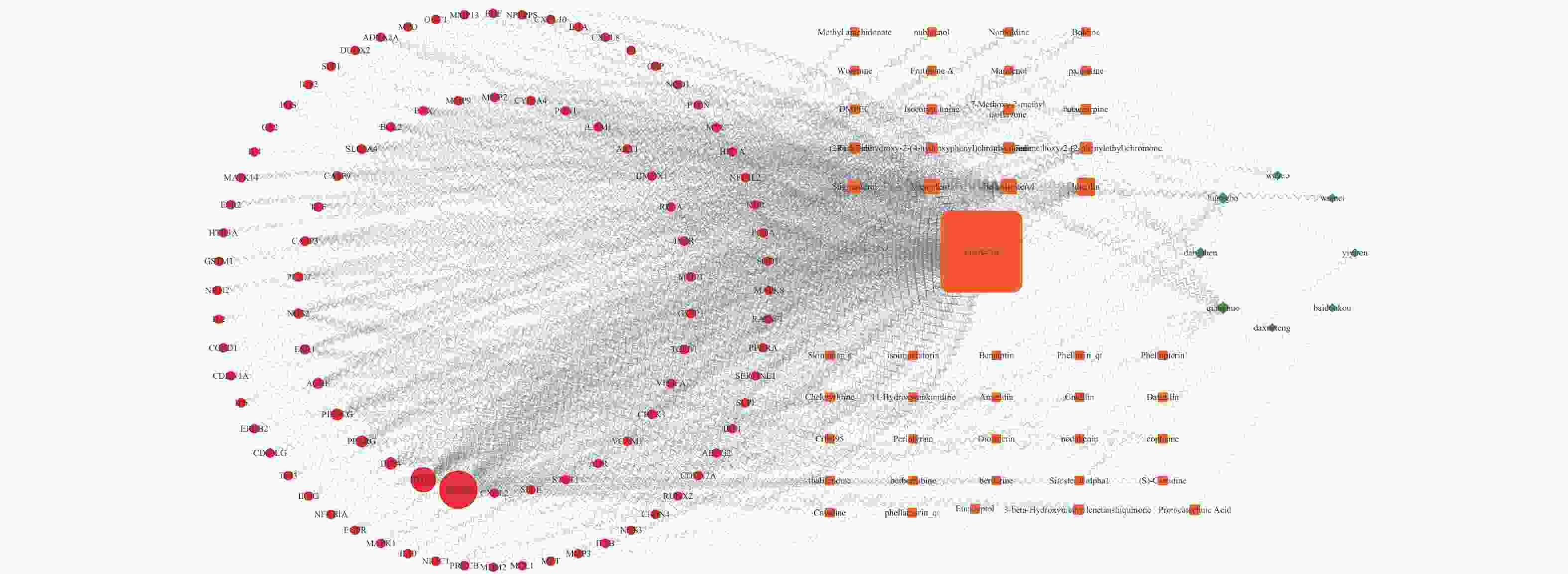
采用Cytoscape3.10.1软件绘制中药-活性成分-交集靶点网络图,通过Network Analyzer插件的中介中心度值分析该网络。中介中心度值越大,网络节点面积越大,相关性越强。该网络共有8味中药,包括羌活、党参、黄柏、乌药、乌梅、薏苡仁、白豆蔻和大血藤(绿色棱形),46味中药成分(橙色方形)和94个交集靶点(红色圆形)。结果表明,羌活、党参、黄柏3味中药面积相对较大,中介中心度值较高,其可能为愈肠颗粒治疗UC的主要活性成分;槲皮素、木犀草素、β-谷甾醇、豆甾醇、山奈酚的面积相对较大,其可能为愈肠颗粒治疗UC的核心活性成分(图2)。进一步研究发现,每味中药对应多个活性成分,每个活性成分作用于多个靶点,这表明愈肠颗粒可通过多成分、多靶点治疗UC。其中,槲皮素的面积最大、颜色最深、链接最多,可能是愈肠颗粒治疗UC最关键的核心活性成分。
-
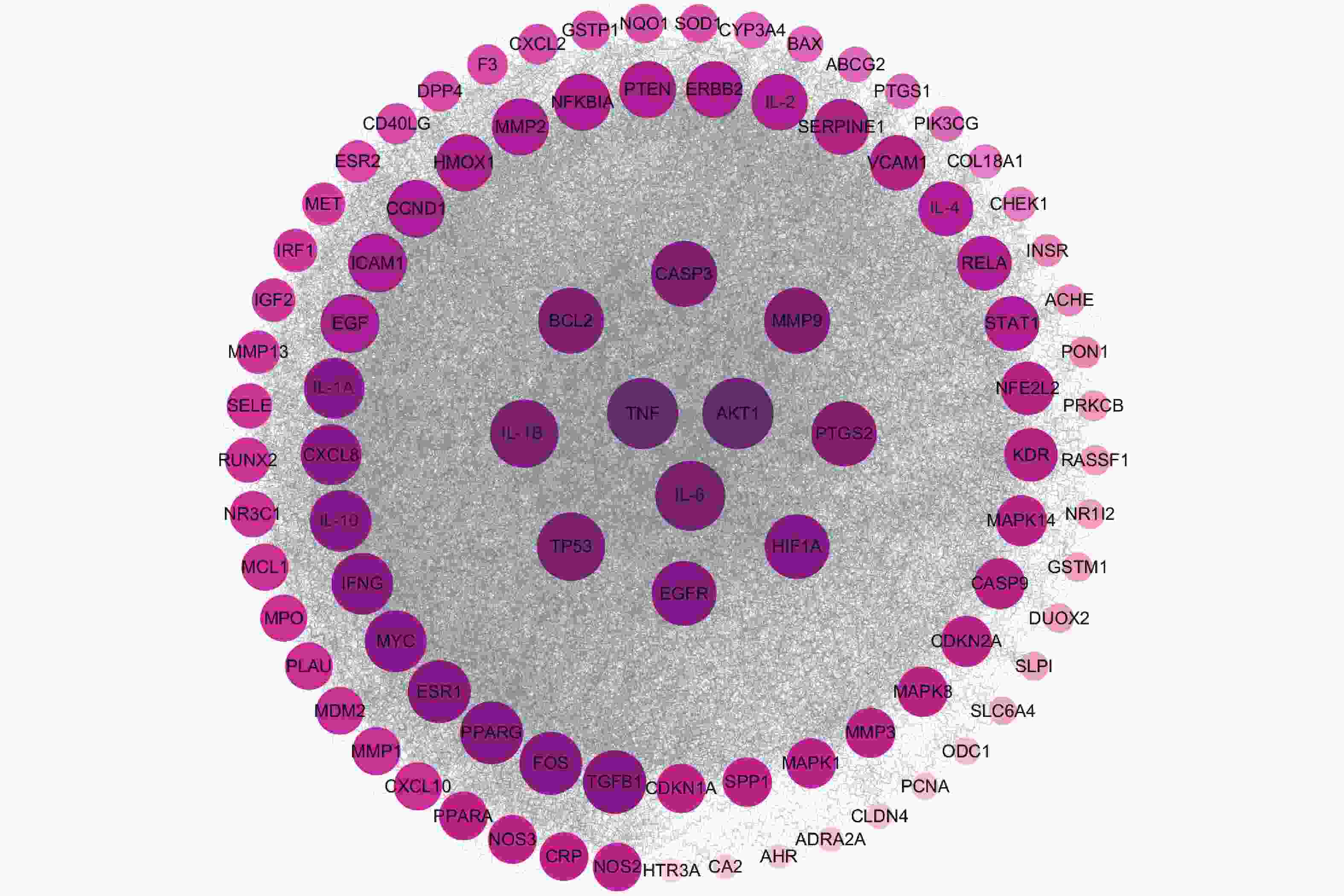
应用STRING网站分析交集靶点,绘制PPI网络图,并使用Cytoscape3.10.1软件根据中介中心度值分析PPI关系网络。中介中心度值越大,该节点面积越大、连线越多、颜色越深、相关性越强。如图3所示,肿瘤坏死因子(TNF)、丝氨酸/苏氨酸蛋白激酶1(serine/threonine-protein kinase,AKT1)、肿瘤蛋白p53(tumor protein p53,TP53)、白介素-6(interleukin-6,IL-6)和IL-1β面积相对较大,颜色相对较深,相关性相对较强,为愈肠颗粒治疗UC的核心靶点;其中以TNF面积最大,颜色最深,相关性最强,可能为愈肠颗粒治疗UC最重要的关键靶点。
-
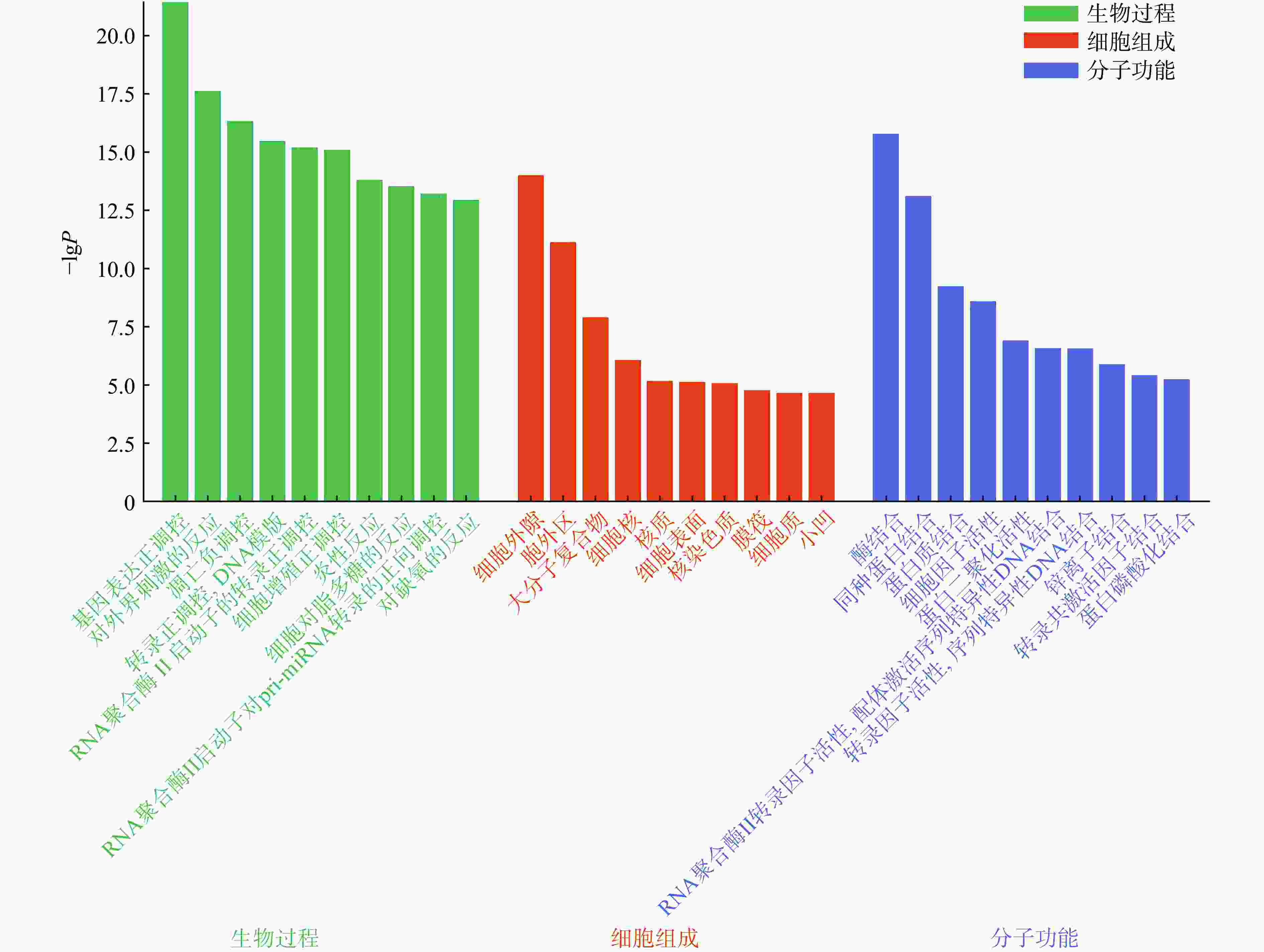
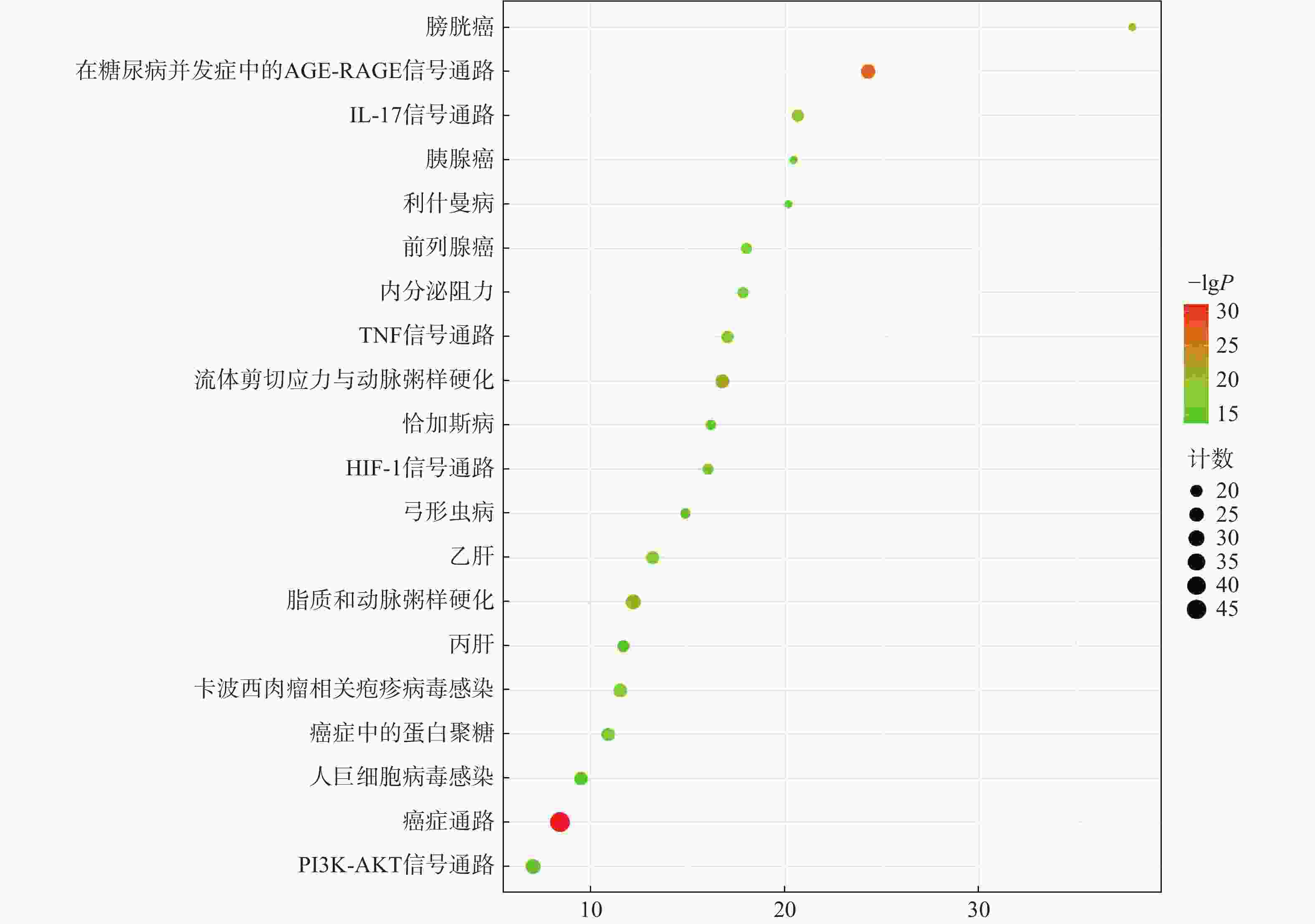
应用David网站对交集靶点进行GO和KEGG通路富集分析,共获得611个生物过程、50个细胞组分、104 个分子功能和158 条信号通路。利用微生信在线平台分析P值前10位生物过程(biological process,BP),细胞组成(cellular component,CC),分子功能(molecular function,MF)条目,并进行可视化。结果如图4所示,BP主要涉及基因表达正向调控、应激、细胞凋亡的负向调控等条目,CC主要涉及细胞外隙、细胞外区域、大分子复合物等条目,MF主要涉及酶结合位点、相同蛋白质结合、蛋白结合等条目。同理,选取P值取前20位KEGG的条目进行可视化分析,结果表明癌症、AGE-RAGE在糖尿病并发症中的作用、脂质和动脉粥样硬化、IL-17和TNF信号通路等条目是愈肠颗粒治疗UC的主要通路等条目,具体见图5。这表明,愈肠颗粒可以通过多细胞组分、多分子功能、多生物学过程和多信号通路作用于UC。
-
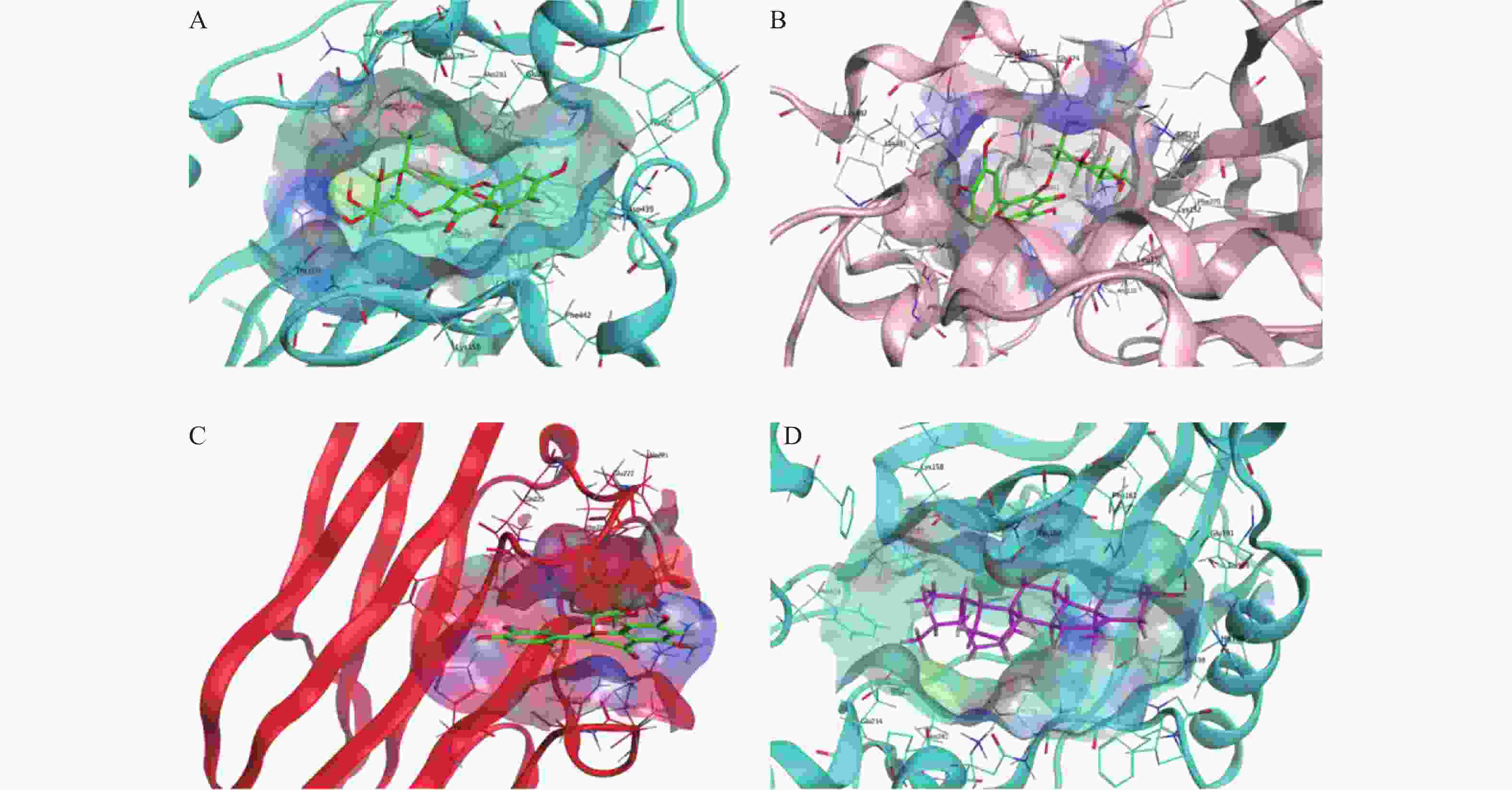
根据中介中心度值,将核心活性成分槲皮素、木犀草素、β-谷甾醇、豆甾醇和山奈酚与关键靶点TNF、AKT1、TP53、IL-6和IL-1β分别进行分子对接,以Score评分研究其相互作用的活性。结果表明,核心活性成分与关键靶点均能对接成功,且亲和力较好,具体见表1。槲皮素与TNF、AKT1和TP53,豆甾醇与AKT1的Score评分均< −7 kcal/mol,相对较低,选择其绘制“靶蛋白-活性分子”对接模式图,具体见图6。这进一步表明,愈肠颗粒可以通过多靶点、多活性成分缓解UC,其中,槲皮素可能是其治疗UC的最关键活性成分。且,其与核心靶点TNF、AKT1和TP53相互作用的Score评分皆大于7。
表 1 愈肠颗粒治疗溃疡性结肠炎的关键活性成分与核心靶点的分子对接Score评分(kcal/mol)
核心靶点 槲皮素 木犀草素 β-谷甾醇 豆甾醇 山奈酚 TNF 7.11 6.07 5.55 5.10 5.53 AKT1 7.65 5.98 6.96 7.00 5.93 TP53 7.19 5.67 6.78 6.51 5.44 IL-6 6.23 5.46 5.90 5.91 5.48 IL-1β 5.99 5.48 5.66 5.87 5.32 -
中医认为,UC属于“肠痈”、“痢疾”、“肛痈”等范畴,与肝、脾、肾等脏腑紧密相关,其在治疗时应注意健脾补肾[7-10]。愈肠颗粒源于(《医学正传》卷三)的“愈肠方”,由白豆蔻、大血藤、党参、黄柏、羌活、乌梅、乌药、薏苡仁和赤石脂9味中药配伍而成。白豆蔻化湿行气,温中止呕,开胃消食,缓解湿阻气滞;大血藤清热解毒,祛风止痛,用于肠痈腹痛;党参补脾益肺,生津养血,治疗脾胃虚弱;黄柏清热燥湿,泻火解毒,缓解湿热泻痢、疮疡肿毒;羌活解表散寒,祛风胜湿,解除风寒湿痹;乌梅涩肠止泻,用于久泻,久痢,腹痛;乌药行气止痛,温肾散寒,治疗寒凝气滞胸腹诸痛证;薏苡仁利水,健脾止泻,除痹,排脓,解毒散结,治疗脾虚泄泻、湿痹拘挛、肠痈。9味中药相互配伍,协同作用,发挥健脾益气,涩肠止泻的作用,然而其具体作用机制尚不明确。
分析中药-活性成分-潜在作用靶点的网络图可知,槲皮素、木犀草素、β-谷甾醇、豆甾醇、山奈酚等活性成分可能是愈肠颗粒治疗UC的核心活性成分,且槲皮素可能是最重要的核心活性成分。目前研究表明,槲皮素可以减缓UC疾病进程[11]。Wang等[12]研究表明槲皮素可以通过增强多环芳烃受体介导的紧密连接,修复肠屏障功能障碍,减轻UC的症状。在DSS处理的UC小鼠中,槲皮素可以通过影响STAT1/PPARγ的平衡改善UC[13]。木犀草素可用于治疗UC[14]。其可以减轻DSS处理的UC大鼠的炎症状态,并调节微生态[15]。Li等[16]研究发现,木犀草素可能通过SHP-1抑制STAT3来保护UC大鼠肠上皮屏障功能。通过抑制巨噬细胞活化和趋化,木犀草素可改善UC小鼠状态[17]。木犀草素可以通过维持NCR-ILC3/NCR+ILC3平衡来修复受损的肠屏障,从而减轻UC[18]。通过调节免疫反应、氧化应激和代谢谱,木犀草素在大鼠UC中发挥重要作用[19]。木犀草素也通过抑制ERK介导的炎症反应、细胞凋亡和自噬,缓解UC小鼠疾病状态[20]。β-谷甾醇对致病菌的多重作用是治疗结肠炎症的一种新方法[21]。β-谷甾醇可显著缓解UC小鼠的体质量减轻、改善UC小鼠结肠长度和镜下外观。该化合物可依赖浓度降低UC小鼠肠组织中TNF-α、IL-6和IL-1β的水平。其处理肠上皮细胞显著增加抗菌肽的表达并降低细胞内鼠伤寒沙门菌的存活率。β-谷甾醇可以通过抑制NLRP3/Caspase-1/gsdmd介导的细胞焦亡,减轻DSS诱导的实验性结肠炎[22]。山奈酚通过恢复肠道菌群和抑制LPS-TLR4-NF-KB轴减轻UC小鼠疾病状态[23]。饮食山奈酚可抑制DSS诱导的UC小鼠的炎症状态[24]。5种核心活性成分在UC的治疗中发挥重要作用,这表明愈肠颗粒可能通过多种活性成分治疗UC,然而具体的机制仍需生物学实验验证。
PPI网络表明,TNF、AKT1、TP53、IL-6和IL-1β可能为愈肠颗粒治疗UC的关键靶点。TNF-α是UC发病机制中重要的促炎细胞因子。英夫利西单抗等TNF-α单克隆单抗已被用于治疗UC。半夏泻心汤通过抑制丝氨酸-苏氨酸蛋白激酶(Akt)/丝裂原活化蛋白激酶(MAPK)信号通路改善DSS诱导的UC[25]。日本人群中UC黏膜发展为早期结直肠肿瘤的基因组图谱显示,UC患者TP53基因突变是导致结直肠癌的一条途径[26]。Friis-ottessen等[27]研究发现,UC患者的TP53基因出现突变。IL-6与IL-1β是常见促炎细胞因子,多种中西药物、小分子都可以通过降低IL-6和IL-1β的水平缓解UC的状态。关键活性成分槲皮素、木犀草素、β-谷甾醇、豆甾醇、山奈酚与关键靶点TNF、AKT1、TP53、IL-6和IL-1β分子对接分值较高,这为我们进一步的研究提供了参考。本研究表明愈肠颗粒可通过多活性成分和多靶点治疗UC,具体的机制仍需生物学验证。
Exploring the mechanism of Yuchang granule on ulcerative colitis based on network pharmacology and molecular docking
-
摘要:
目的 利用网络药理学及分子对接技术研究愈肠颗粒治疗溃疡性结肠炎(UC)的分子机制。 方法 应用TCMSP和HIT数据库检索筛选愈肠颗粒活性成分和作用靶点,利用GeneCards、CTD和DisGeNET数据库获取UC疾病相关靶点;取二者交集靶点作为愈肠颗粒治疗UC的潜在作用靶点。应用Cytoscape 3.10.1软件构建“中药-活性成分-交集靶点”网络,获取核心活性成分。将交集靶点导入STRING数据库中进行蛋白质-蛋白质相互作用(PPI)网络分析,筛选关键靶点。应用DAVID数据库对交集靶点进行GO功能和KEGG通路富集分析,并使用微生信在线工具进行可视化分析,获取主要通路。将核心活性成分和关键靶点进行分子对接验证作用机制。 结果 研究共得到98个活性成分和 94个交集靶点,交集靶点共涉及 611 个生物过程、50 个细胞组分、104 个分子功能以及 158 条信号通路。槲皮素、木犀草素、β-谷甾醇、豆甾醇、山奈酚为核心活性成分,其中槲皮素可能为最关键的核心活性成分;肿瘤坏死因子(TNF)、丝氨酸/苏氨酸蛋白激酶1(AKT1)、肿瘤蛋白p53(TP53)、白介素-6(IL-6) 和IL-1β为关键靶点;癌症、AGE-RAGE在糖尿病并发症中的作用、脂质和动脉粥样硬化、IL-17和TNF信号通路等为主要信号通路。核心活性成分与关键靶点结合活性均良好,其中槲皮素与TNF、AKT1和TP53,豆甾醇与AKT1结合效果最好。 结论 愈肠颗粒通过多成分、多靶点、多通路发挥对UC的治疗作用。 Abstract:Objective To determine the molecular mechanism of Yuchang granule (YCG) against ulcerative colitis (UC) by network pharmacology-based approach combined with molecular docking. Methods TCMSP and HIT database were utilized to search the active components and potential targets of YCG. The effective targets of UC were obtained by GeneCards, CTD, and DisGeNET databases. Venn Diagram was exploited to receive common targets of YCG and UC. Network maps of the TCM of YCG-active component-common targets were constructed by the Cytoscape software to gain key active components. Protein-protein interaction (PPI) of common targets was constructed by the STRING database obtaining core common targets. The mechanism and therapeutic effects of YCG on UC were explored via gene ontology (GO) and the biological pathway (KEGG) enrichment analyses. Molecular docking technology was carried out to verify the combination of core active components with key common targets. Results 98 active components and 237 potential targets were sieved from YCG, and 1061 effective targets were screened from UC. 94 common targets of YCG and UC were regarded as potential therapeutic targets. Bioinformatics analysis revealed that quercetin, luteolin, β-quebrachol, stigmasterol, and kaempferol may be the potential candidate agents. Tumor necrosis factor (TNF), serine/threonine-protein kinase (AKT1), tumor protein p53 (TP53), interleukin-6 (IL-6) and IL-1β could become potential therapeutic targets. KEGG showed pathways in cancer, AGE-RAGE signaling pathway in diabetic complications, TNF signaling pathway, and IL-17 signaling pathway might play an important role in YCG against UC. Molecular docking results showed that quercetin combined well with TNF, AKT1, and TP53. And stigmasterol did well with AKT1.Conclusion This study comprehensively illustrated the potential candidate agents, potential therapeutic targets, and pathways of YCG against UC. It also illustrated that YCG could act on multiple targets through multi-pathway treating UC. -
Key words:
- Yuchang granules /
- ulcerative colitis /
- network pharmacology /
- molecular docking /
- mechanisms
-
表 1 愈肠颗粒治疗溃疡性结肠炎的关键活性成分与核心靶点的分子对接Score评分(kcal/mol)
核心靶点 槲皮素 木犀草素 β-谷甾醇 豆甾醇 山奈酚 TNF 7.11 6.07 5.55 5.10 5.53 AKT1 7.65 5.98 6.96 7.00 5.93 TP53 7.19 5.67 6.78 6.51 5.44 IL-6 6.23 5.46 5.90 5.91 5.48 IL-1β 5.99 5.48 5.66 5.87 5.32 -
[1] RUBIN D T, ANANTHAKRISHNAN A N, SIEGEL C A, et al. ACG clinical guideline: ulcerative colitis in adults[J]. Am J Gastroenterol, 2019, 114(3): 384-413. doi: 10.14309/ajg.0000000000000152 [2] MOLLER F T, ANDERSEN V, WOHLFAHRT J, et al. Familial risk of inflammatory bowel disease: a population-based cohort study 1977-2011[J]. Am J Gastroenterol, 2015, 110(4): 564-571. doi: 10.1038/ajg.2015.50 [3] 邵雪庆. 治疗慢性结肠炎新药-愈肠颗粒的制剂及药效学研究[D]. 上海: 海军军医大学, 2018. [4] RU J L, LI P, WANG J N, et al. TCMSP: a database of systems pharmacology for drug discovery from herbal medicines[J]. J Cheminform, 2014, 6: 13. doi: 10.1186/1758-2946-6-13 [5] YE H, YE L, KANG H, et al. HIT: linking herbal active ingredients to targets[J]. Nucleic Acids Res, 2011, 39(Database issue): D1055-D1059. [6] YAN D Y, ZHENG G H, WANG C C, et al. HIT 2.0: an enhanced platform for Herbal Ingredients’ Targets[J]. Nucleic Acids Res, 2022, 50(D1): D1238-D1243. doi: 10.1093/nar/gkab1011 [7] 杨洁, 张明明, 于道远, 等. 代红雨教授治疗炎症性肠病经验浅谈[J]. 四川中医, 2023, 41(11): 1-3. doi: 10.3969/j.issn.1000-3649.2023.11.sczy202311001 [8] 雷露, 吕沛然, 张宁, 等. 中医治疗炎症性肠病机制的研究进展[J]. 中医药学报, 2024, 52(2): 116-121. [9] 凌海慧, 梁棻, 刘蓉, 等. 中医药保护肠黏膜屏障治疗炎症性肠病的研究进展[J]. 天津中医药, 2018, 35(9): 718-720. [10] 秦广宁, 刘耀远, 高宁, 等. 张伯礼基于 “湿浊痰饮类病” 学说分期论治极早发型炎症性肠病经验[J]. 中医杂志, 2023, 64(22): 2282-2286. [11] WUSHOUER X, AXIMUJIANG K, KADEER N, et al. Effect of huankuile on colon injury in rats with ulcerative colitis by reducing TNF-α and MMP9[J]. Eur J Med Res, 2024, 29(1): 102. doi: 10.1186/s40001-024-01695-w [12] WANG X J, XIE X T, LI Y Y, et al. Quercetin ameliorates ulcerative colitis by activating aryl hydrocarbon receptor to improve intestinal barrier integrity[J]. Phytother Res, 2024, 38(1): 253-264. doi: 10.1002/ptr.8027 [13] ZHOU H F, YANG C, LI J Y, et al. Quercetin serves as the major component of Xiang-Lian Pill to ameliorate ulcerative colitis via tipping the balance of STAT1/PPARγ and dictating the alternative activation of macrophage[J]. J Ethnopharmacol, 2023, 313: 116557. doi: 10.1016/j.jep.2023.116557 [14] KIM W S, SONG H Y, HAN J M, et al. GLM, a novel luteolin derivative, attenuates inflammatory responses in dendritic cells: Therapeutic potential against ulcerative colitis[J]. Biochem Biophys Res Commun, 2019, 518(1): 87-93. doi: 10.1016/j.bbrc.2019.08.012 [15] LI B L, DU P L, DU Y, et al. Luteolin alleviates inflammation and modulates gut microbiota in ulcerative colitis rats[J]. Life Sci, 2021, 269: 119008. doi: 10.1016/j.lfs.2020.119008 [16] LI B L, ZHAO D Y, DU P L, et al. Luteolin alleviates ulcerative colitis through SHP-1/STAT3 pathway[J]. Inflamm Res, 2021, 70(6): 705-717. doi: 10.1007/s00011-021-01468-9 [17] XUE L, JIN X, JI T, et al. Luteolin ameliorates DSS-induced colitis in mice via suppressing macrophage activation and chemotaxis[J]. Int Immunopharmacol, 2023, 124(pt b): 110996. [18] XIE X Q, ZHAO M, HUANG S W, et al. Luteolin alleviates ulcerative colitis by restoring the balance of NCR−ILC3/NCR+ILC3 to repairing impaired intestinal barrier[J]. Int Immunopharmacol, 2022, 112: 109251. doi: 10.1016/j.intimp.2022.109251 [19] LI B, GUO Y, JIA X, et al. Luteolin alleviates ulcerative colitis in rats via regulating immune response, oxidative stress, and metabolic profiling[J]. Open Med(Wars), 2023, 18(1): 20230785. doi: 10.1515/med-2023-0785 [20] VUKELIĆ I, DETEL D, BATIČIĆ L, et al. Luteolin ameliorates experimental colitis in mice through ERK-mediated suppression of inflammation, apoptosis and autophagy[J]. Food Chem Toxicol, 2020, 145: 111680. doi: 10.1016/j.fct.2020.111680 [21] DING K, TAN Y Y, DING Y, et al. β-Sitosterol improves experimental colitis in mice with a target against pathogenic bacteria[J]. J Cell Biochem, 2019, 120(4): 5687-5694. doi: 10.1002/jcb.27853 [22] ZHANG D, GE F, JI J, et al. β-sitosterol alleviates dextran sulfate sodium-induced experimental colitis via inhibition of NLRP3/Caspase-1/GSDMD-mediated pyroptosis[J]. Front Pharmacol, 2023, 14: 1218477. doi: 10.3389/fphar.2023.1218477 [23] QU Y F, LI X Y, XU F Y, et al. Kaempferol alleviates murine experimental colitis by restoring gut microbiota and inhibiting the LPS-TLR4-NF-κB axis[J]. Front Immunol, 2021, 12: 679897. doi: 10.3389/fimmu.2021.679897 [24] PARK M Y, JI G E, SUNG M K. Dietary kaempferol suppresses inflammation of dextran sulfate sodium-induced colitis in mice[J]. Dig Dis Sci, 2012, 57(2): 355-363. doi: 10.1007/s10620-011-1883-8 [25] JI W L, LIU W, HUO Y, et al. Banxia Xiexin Decoction ameliorates dextran sulfate sodium(DSS)-induced ulcerative colitis via inhibiting serine-threonine protein kinase(Akt)/mitogen-activated protein kinase(MAPK)signaling pathway[J]. Biotechnol Appl Biochem, 2023, 70(4): 1530-1542. doi: 10.1002/bab.2451 [26] MATSUMOTO K, URABE Y, OKA S, et al. Genomic landscape of early-stage colorectal neoplasia developing from the ulcerative colitis mucosa in the Japanese population[J]. Inflamm Bowel Dis, 2021, 27(5): 686-696. doi: 10.1093/ibd/izaa268 [27] FRIIS-OTTESSEN M, BURUM-AUENSEN E, SCHJØLBERG A R, et al. TP53/p53 alterations and Aurora A expression in progressor and non-progressor colectomies from patients with longstanding ulcerative colitis[J]. Int J Mol Med, 2015, 35(1): 24-30. doi: 10.3892/ijmm.2014.1974 -




 下载:
下载: