-
粉-液双室袋是采用特定工艺将药物和注射用溶剂独立封装在不同的两个腔室中的一种静脉注射用产品,在医护人员紧缺或战备、紧急救援等情况下,其优势突出[1]。1996年,日本研制出世界首个粉-液双室袋产品——头孢唑林钠氯化钠注射剂[2]。2015年,原中国食品药品监督管理总局出台首个《粉液双室袋产品技术审评要点》[3],国内首个粉-液双室袋产品(注射用头孢他啶/氯化钠注射液)于2019年获得药品注册批件,正式上市。粉-液双室袋因其结构上的创新,给药预处理步骤简化在使用上具有独特的优势,因此粉-液双室袋产品自上市后就受到了广泛的关注。但对于这样一个新产品,是否真正安全有效,是否具有成本-效益,与市场上正在使用的传统粉针剂相比是否具有明显的优势等问题目前均未得到解答,利益各方大都采取观望的态度。
为促进粉-液双室袋产品临床合理应用,依据国家卫健委2020年发布的《药品临床综合评价管理指南(试行)》[4],通过对文献资料进行调研,提取粉-液双室袋常用评价指标,以传统粉针产品为对照,从安全性、有效性、经济性、适宜性、可及性、创新性6个维度对粉-液双室袋产品进行综合评价。
-
以“双室袋” “双腔袋” “多室袋” “多腔袋” “Multi chamber bag”和“dual chamber bag”等为关键词,在中国知网、万方数据、维普、PubMed 、Web of Science等数据库中进行系统文献检索,对发表年度不设限制。表1为具体的检索式及相应检索结果。
表 1 检索式及检索结果
检索条件 各数据库检索结果 中国知网 万方数据 维普 PubMed Web of Science (主题=双室袋 + 粉液双室袋)OR(主题=双腔袋)
OR(主题=多室袋)OR(主题=多腔袋)80 ((((任意字段=双室袋 OR 任意字段=粉液双室袋)OR 任意字段=多室袋)OR 任意字段=双腔袋)OR 任意字段=多腔袋) 189 主题=(双室袋)OR 主题=(粉液双室袋)OR 主题=(多室袋)
OR 主题=(双腔袋)OR 主题=(多腔袋)6740 (Multi chamber bag)OR(dual chamber bag) 42 (Multi chamber bag)OR (dual chamber bag) 166 -
纳入标准:①研究对象为粉-液双室袋;②内容为安全性、有效性、经济性、适用性、创新性、可及性的研究;③文献类型为随机对照试验或观察实验;④有参考价值的多室袋研究文献。
排除标准:①研究对象为液-液双室袋;②内容为生产工艺、设备、分装技术和其他无关内容;③文献类型为综述、会议论文、专利、成果;④重复文献、不可下载文献。
-
文献由2名研究员独立、同步进行筛选。参考中国医药包装协会发布的《基础输液临床使用评估指南(试行)》[5]和国家卫健委发布的《药品临床综合评价管理指南(试行)》[4]提取文献中的可用指标。如产生争议,由课题组成员讨论决定。
-
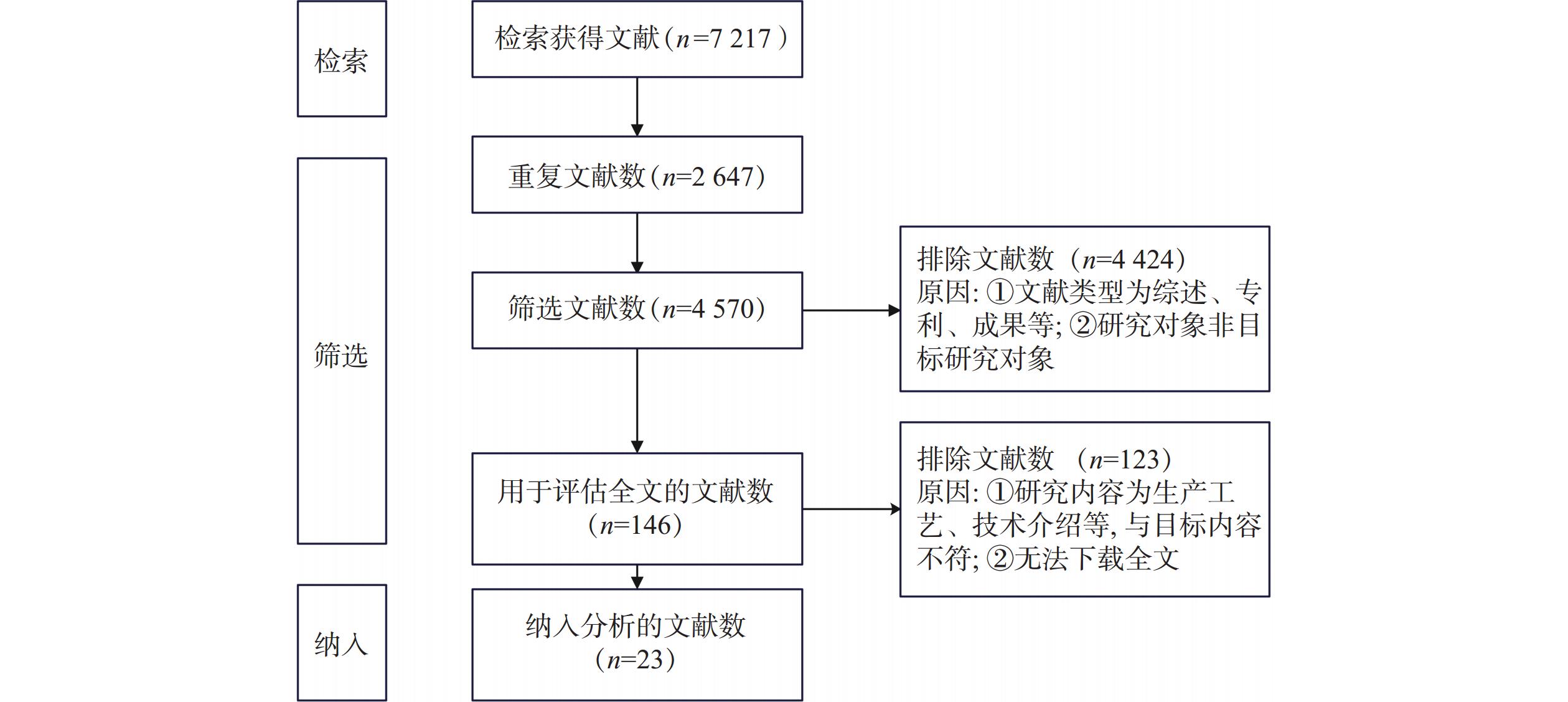
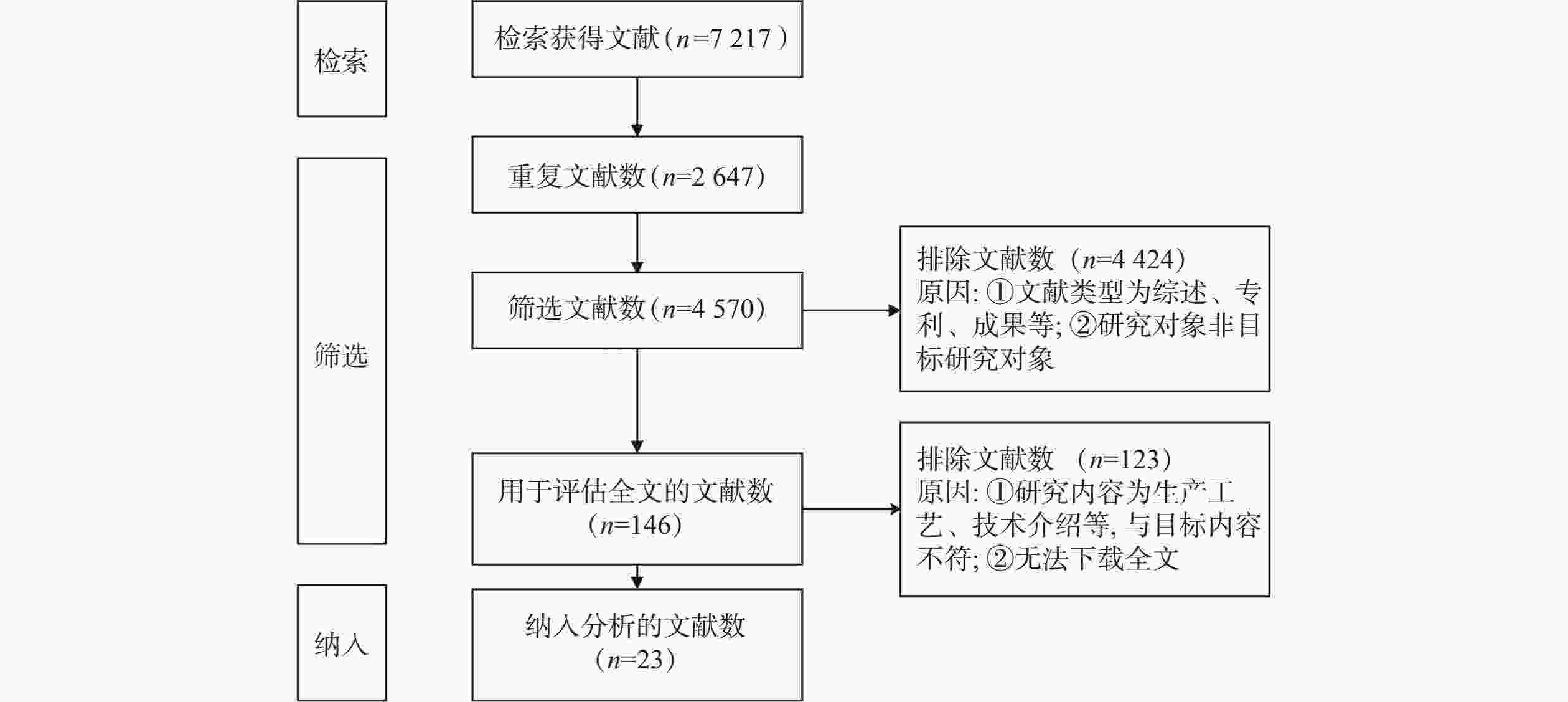
系统检索文献得
7217 篇,排除重复文献2647 篇、文献类型为综述、会议论文等4424 篇、文献内容为生产工艺和技术介绍等123篇,最终纳入分析文献23篇,其中英文文献2篇,中文文献21篇。具体筛选过程如图1。 -
文献中使用的评价指标涉及5个维度,经过整合、汇总,见表2。由于双室袋产品和传统粉针剂的药物成分、给药途径一致,仅包装和给药预处理存在区别,故有效性、安全性两个维度仅包括与包装和给药预处理相关的指标。其中,虽配制过程刺伤、划伤等为操作失误,但双室袋产品简化了药液配制过程,无需使用注射器辅助配制,可完全避免意外伤害,与传统粉针剂存在差异,故纳入为安全性指标。
表 2 已发表文献使用的评价指标
评价维度 判别可用指标 有效性 药液稳定性、配制浓度准确性、药液残留量 安全性 不溶性微粒、刺伤划伤等意外事情发生率 经济性 配制成本a、废弃物重量、住院成本、血液感染发生率 适宜性 配制时间、平均医护人员人力占用、包装重量和
储运体积b、环境适应性、废弃物处理难易程度可及性 生产厂家数量、产品原材料供应能力、患者可负担性 a:为药液成本、配制用品以及配制人工成本的总和;b:包括药液配制过程所需用品储运体积总和,传统粉针剂产品的配制用品包括注射器、西林瓶粉针、配制用溶剂等,粉-液双室袋产品仅包括产品本身。 -
于庆坤等[6-12]研究结果显示,与传统粉针剂相比,双室袋产品的药液含量随时间变化小,配制的实际浓度更接近理论浓度,无残留药液,具体见表3和表4。
表 3 药液配置后5 h的稳定性对比[7]
产品名称 不同温度时的百分含量(%) 4℃ 25℃ 非PVC粉-液双室袋产品 96.33 96.32 玻璃瓶粉针产品 95.37 95.79 -
静脉输液中的不溶性微粒会造成血栓和静脉炎[13],药典规定用于静脉注射、滴注的药品需检查不溶性微粒。双室袋法配制过程不溶性微粒无明显增加[8,10,14-15],详见表5。以18名护士为观察对象,粉针配制过程1名护士被划伤,双室袋配制过程无人员刺伤、划伤[10]。粉-液双室袋以非PVC多层共挤膜为膜材,其强光照射实验表明0.9%氯化钠、5%葡萄糖、葡萄糖氯化钠、复方氯化钠注射液与膜材相容性良好,稳定性试验表明非PVC多层共挤膜的水蒸气渗透、透光率、pH、易氧化物检测均符合规定[14,16]。
表 5 配制过程不溶性微粒比较
文献作者 样品 不溶性微粒数(个/ml) ≥5 ≥8 ≥10 ≥12 ≥25 ≥100 李英等[15]a 粉针输液产品 318 66 21 6 0 0 配制增加微粒数b 285 55 15 3 0 0 双室袋输液产品 2 0 0 0 0 0 双室袋增加微粒数c 0 0 0 0 0 0 沈敏娜等[16]a 粉针输液产品 322 68 23 7 0 0 配制增加微粒数 289 55 17 5 0 0 双室袋输液产品 3 1 0 0 0 0 双室袋增加微粒数c 0 0 0 0 0 0 王宇航等[8]a 粉针输液产品 240 326.5 43 24 7 0 双室袋输液产品 240 2 0 0 0 0 罗莉等[10]d 粉针输液产品 219.52±84.73 43.93±21.68 14.93±7.96 4.05±2.60 0.01±0.04 双室袋输液产品 3.49±0.95 0.39±0.19 0.20±0.11 0.13±0.09 0.03±0.03 a:实验重复配制(均≥100份),由于数据资料不服从正态分布,选中位数表征平均水平,表中均为中位数值;b:增加微粒数=溶液微粒数−(粉体+液体),表示溶配方法增加的不溶性微粒;c:双室袋法配置的不溶性微粒增加数计算结果为负值,由于混合前为取出粉末后在非封闭的环境中进行溶解测试,而混合后则是在封闭的袋内进行开通溶解后测试,从而导致粉体检测结果高于混合液的情况出现,因此即配型双室袋法配置的不溶性微粒增加数视为零;d:本实验所取数据为不溶性微粒数范围值。 -
在纳入的双室袋产品相关经济性研究[8,17-18]中考虑到的成本指标包括配制成本(包括配制环境、设备以及环境维护费、人工成本、耗材成本)、废弃物重量,效果/效益以血液感染(BSI)为指标。采用双室袋输液,药液配制过程得到简化,一方面可节省储存场所、人工及耗材成本,一方面产生的废弃物减少,废弃物处理费会有所减少。王宇航等[8]通过计算发现按照4.82元/kg的垃圾清理费算,每年可减少废弃物处理费约7万元。此外,双室袋输液配制过程减少与空气的接触,可在一定程度上减少输液后血液感染的发生率。苗雅楠等[17]发现在
1000 例患者中,输液系统由半开放式转换为全密闭输液系统可减少172例血液感染。已上市的粉-液双室袋产品与对应的传统粉针相比,有效期相同,对于储备来说,两者轮换周期一致。 -
对于易溶于水但在水溶液中不稳定的药物一般选择制成注射用无菌粉针,此类产品在使用前需要与特定的配制用溶剂临时配制注射用溶液。与粉针剂西林瓶产品运用的药液配制方法相比,双室袋法输液预处理环节有所简化,能明显缩短药液配制时间[8,10,19],具体见表6,在医护资源匮乏(如应急医学救援)时,可减少医护人员人力的占用。此外双室袋为全密闭输液系统,对环境的耐受性强。
-
可及性包括可获得和可负担两方面的要求。双室袋产品的药液与传统粉针一致,包装材料有所不同,目前双室袋包材审批通过已登记的有15项(1项为进口),双室袋产品生产厂家超过5家,产品大都为头孢类抗感染药物,在生产供应方面,可以满足可及性的要求。此外,2022年《国家基本医疗保险药品目录》的协议期内谈判药品部分有5个粉-液双室输液产品被纳入,为医保乙类药品,可达到患者可负担的要求。
-
截止到2023年4月,与粉-液双室输液袋有关的发明专利有22项,实用新型专利89项,外观专利5项,包括生产、灌装、检漏等方面。粉-液双室袋产品能缩短配液时间,简化输液预处理过程,降低了输液对环境的要求,顺应了突发事件应急医学救援与创伤急救的需求。
-
本研究采用系统综述的方法对现有文献信息分析提取,得到的指标可作为评价指标池的一部分,后续可用于建立粉-液双室袋产品综合评价指标体系。
粉-液双室袋产品与传统粉针药效成分、给药途径相同,我国对药品上市后包装变更无临床试验的要求[20],已发表文献中均未报告其有效性、安全性的临床结局指标,且两者仅在包材和给药预处理方面存在差异,故纳入的有效性指标只包括药物学工艺重现性,安全性指标只包括不良事件或风险的比较指标。除列出指标外,安全性评价还需考虑渗漏隐患、破损率、误配、错配发生率等。经济性评价具有时间性,存在偏倚风险,仍需对此类产品进行更为可靠的经济学研究。适用性的考查应注重产品在紧急救援使用时缩短抢救时间,节约医护资源的能力。粉-液双室袋的技术壁垒较高,可及性方面不如传统粉针剂,但符合可及性的基本要求。
粉-液双室袋属于全封闭式输液系统,无空气通路,细菌污染降低,减少了输液反应的发生[21]。药液配制时间明显缩短,提高救援成功率[22];无需临时计算溶剂用量,配制准确度高,无药液残留,且对环境、技术要求不高,降低了人工、设施及耗材成本;无需借助注射器反复穿刺橡胶塞,不溶性微粒显著减少,刺伤、划伤等意外事情可避免。虽单价高于传统粉针产品,但其在废弃物处理成本、人工成本以及输液后静脉炎发生率的减少方面展现出了一定的优势。此外国内双室袋产品的生产企业超过5家,且在原材料上摆脱了对进口的依赖,5种粉-液双室袋产品已纳入医保目录,符合可及性要求。
粉-液双室袋为新兴产品,仅有23篇符合纳入条件。外文文献较少,仅纳入2篇。因多室袋与双室袋原理一致,故将以多室袋为研究对象的文献也纳入。期待随着粉-液双室袋在我国广泛应用,未来可获得高质量、精细化的研究数据,以开展更全面、可靠的综合评价研究。
Comprehensive evaluation of powder-liquid double-chamber bag products: a systematic review
-
摘要:
目的 以传统粉针剂为对照,对粉-液双室袋产品进行综合评估。 方法 采用系统综述法,收集粉-液双室袋文献资料,提取常用评价指标,评估粉-液双室袋产品的使用价值,与传统粉针剂产品进行综合比较。 结果 共纳入文献23篇,评估使用的有效性指标为药液稳定性、配制浓度准确性、药液残留量;安全性指标为不溶性微粒、刺伤划伤发生率;经济性指标为配制成本、废弃物重量、住院成本、血液感染发生率;适用性指标为配制时间、平均医护人员人力占用、包装重量和储运体积、环境适应性、废弃物处理难易程度;可及性指标为生产厂家数量、原料供应能力、患者可承担性。通过文献证据对其评估,表明粉-液双室袋稳定性、浓度准确性高于传统粉针剂,并已实现国产供应。双室袋法配制药液可减少输液反应,能缩短药液配制时间。 结论 相比于传统粉针产品,粉-液双室袋在有效性、安全性、经济性、适宜性、创新性维度均具备优势,可及性维度符合要求。 Abstract:Objective To evaluate the advantages of powder-liquid double-chamber bag products compared with traditional powder injection. Methods The systematic review method was used to collect the literature on powder-liquid double-chamber bag, extract common evaluation indicators, evaluate the use value of powder-liquid double-chamber bag products, and conduct a comprehensive comparison with traditional powder injection products. Results A total of 23 articles were included in the literature. The effectiveness indicators used for evaluation were the stability of the liquid medicine, the accuracy of the preparation concentration, and the residual amount of the liquid medicine; the safety indicators were the incidence of insoluble particles and the incidence of punctures and scratches. The economic indicators were preparation cost, occupied volume of preparation supplies, waste weight, hospitalization cost and incidence of blood infection. The applicability indicators were preparation time, average occupation of medical staff, packaging weight and storage and transportation volume, environmental adaptability, and ease of waste disposal. Accessibility indicators are the number of manufacturers, raw material supply capacity, and patient affordability. Through the evaluation of literature evidence, it was found that the stability and concentration accuracy of the powder-liquid double-chamber bag were higher than those of the traditional powder injection, and the domestic supply had been achieved. The double-chamber bag method can reduce the infusion reaction and shorten the preparation time of the liquid medicine. Conclusion Compared with traditional powder injectabler products, powder-liquid double-chamber bags have advantages in the dimensions of effectiveness, safety, economy, suitability and innovation, and the accessibility dimension meets the requirements. -
Key words:
- powder-liquid double chamber bag /
- comprehensive evaluation /
- injection
-
表 1 检索式及检索结果
检索条件 各数据库检索结果 中国知网 万方数据 维普 PubMed Web of Science (主题=双室袋 + 粉液双室袋)OR(主题=双腔袋)
OR(主题=多室袋)OR(主题=多腔袋)80 ((((任意字段=双室袋 OR 任意字段=粉液双室袋)OR 任意字段=多室袋)OR 任意字段=双腔袋)OR 任意字段=多腔袋) 189 主题=(双室袋)OR 主题=(粉液双室袋)OR 主题=(多室袋)
OR 主题=(双腔袋)OR 主题=(多腔袋)6740 (Multi chamber bag)OR(dual chamber bag) 42 (Multi chamber bag)OR (dual chamber bag) 166 表 2 已发表文献使用的评价指标
评价维度 判别可用指标 有效性 药液稳定性、配制浓度准确性、药液残留量 安全性 不溶性微粒、刺伤划伤等意外事情发生率 经济性 配制成本a、废弃物重量、住院成本、血液感染发生率 适宜性 配制时间、平均医护人员人力占用、包装重量和
储运体积b、环境适应性、废弃物处理难易程度可及性 生产厂家数量、产品原材料供应能力、患者可负担性 a:为药液成本、配制用品以及配制人工成本的总和;b:包括药液配制过程所需用品储运体积总和,传统粉针剂产品的配制用品包括注射器、西林瓶粉针、配制用溶剂等,粉-液双室袋产品仅包括产品本身。 表 3 药液配置后5 h的稳定性对比[7]
产品名称 不同温度时的百分含量(%) 4℃ 25℃ 非PVC粉-液双室袋产品 96.33 96.32 玻璃瓶粉针产品 95.37 95.79 表 4 配制浓度准确性以及药液残留量的比较
表 5 配制过程不溶性微粒比较
文献作者 样品 不溶性微粒数(个/ml) ≥5 ≥8 ≥10 ≥12 ≥25 ≥100 李英等[15]a 粉针输液产品 318 66 21 6 0 0 配制增加微粒数b 285 55 15 3 0 0 双室袋输液产品 2 0 0 0 0 0 双室袋增加微粒数c 0 0 0 0 0 0 沈敏娜等[16]a 粉针输液产品 322 68 23 7 0 0 配制增加微粒数 289 55 17 5 0 0 双室袋输液产品 3 1 0 0 0 0 双室袋增加微粒数c 0 0 0 0 0 0 王宇航等[8]a 粉针输液产品 240 326.5 43 24 7 0 双室袋输液产品 240 2 0 0 0 0 罗莉等[10]d 粉针输液产品 219.52±84.73 43.93±21.68 14.93±7.96 4.05±2.60 0.01±0.04 双室袋输液产品 3.49±0.95 0.39±0.19 0.20±0.11 0.13±0.09 0.03±0.03 a:实验重复配制(均≥100份),由于数据资料不服从正态分布,选中位数表征平均水平,表中均为中位数值;b:增加微粒数=溶液微粒数−(粉体+液体),表示溶配方法增加的不溶性微粒;c:双室袋法配置的不溶性微粒增加数计算结果为负值,由于混合前为取出粉末后在非封闭的环境中进行溶解测试,而混合后则是在封闭的袋内进行开通溶解后测试,从而导致粉体检测结果高于混合液的情况出现,因此即配型双室袋法配置的不溶性微粒增加数视为零;d:本实验所取数据为不溶性微粒数范围值。 -
[1] 伍红艳, 吴述敏, 崔夏子, 等. 非PVC粉-液双室输液软袋与传统型输液包装的功能比较[J]. 中国药学杂志, 2011, 46(6):474-476. [2] 蒋煜, 黄晓龙. 粉液双室袋产品的质量控制风险分析及其设计[J]. 中国新药杂志, 2016, 25(7):733-738. [3] 国家药品监督管理局. 关于发布粉液双室袋产品技术审评要点(试行)的通告(2015年第39号)[EB/OL]. (2015-07-28)[2023-12-28]. https://www.nmpa.gov.cn/xxgk/fgwj/gzwj/gzwjyp/20150728120001697.html. [4] 杨金伟.药品临床综合评价管理指南发布[N]. 健康报, 2021-07-29(001). DOI: 10.28415/n.cnki.njika.2021.003528. [5] 中国医药包装协会. 关于发布协会标准《基础输液临床使用评估指南》的通知 [EB/OL]. (2018-08-24)[2023-12-28]. https://www. cnppa.org/index.php/Home/Bz/show_2019/id/941.html. [6] 于庆坤, 阚淑月, 王春艳, 等. 注射用头孢噻肟钠在4种不同包装输液中的稳定性考察[J]. 中国药房, 2006, 17(5):375-377. doi: 10.3969/j.issn.1001-0408.2006.05.024 [7] BLEDSOE S, LITTLE J, WILKINSON R S, et al. Using lean methodology to improve operational and clinical efficiency[J]. Am J Health Syst Pharm, 2013, 70(17):1476-1477. doi: 10.2146/ajhp120547 [8] 王宇航, 李英, 陈月, 等. 即配型粉-液双室袋与传统包装形式的系统性对比[J]. 中国医院药学杂志, 2013, 33(21):1817-1819. [9] 唐维英, 张贝, 杨姗姗, 等. 双室袋法与注射器法所配静脉输液中药物含量的测定及比较[J]. 华西药学杂志, 2018, 33(2):207-209. [10] 罗莉, 孙宇, 夏晚秋, 等. 阿奇霉素粉-液双室袋与传统粉针配制的比较研究[J]. 中国抗生素杂志, 2017, 42(8):669-672. doi: 10.3969/j.issn.1001-8689.2017.08.009 [11] 李娅. 利用药物经济学指导输液包装差别定价[D] .沈阳: 沈阳药科大学,2007. [12] 颜耀东, 刘思川, 邹瑰丽, 等. 注射用乳糖酸阿奇霉素粉-液双室输液袋包材的相容性研究[J]. 中国药学杂志, 2017, 52(22):2007-2011. doi: 10.11669/cpj.2017.22.012 [13] 曹燕丽, 岩林苹, 乔立业, 等. 五层共挤膜输液用袋稳定性考察及其与4种自制注射液的相容性[J]. 中国医院药学杂志, 2014, 34(19):1690-1695. [14] 徐立人, 邬兰英. 输液中不溶性微粒的危害及其预防[J]. 中国实用护理杂志, 1988, 4(8):43-44. [15] 李英, 王宇航, 赵立波, 等. 双室袋法与注射器法配制静脉输液的不溶性微粒比较[J]. 中国药学杂志, 2013, 48(22):1969-1971. [16] 沈敏娜. 静脉输液药剂应用双室袋法比照注射器法的不溶性微粒对比研究[J]. 中国实用医药, 2015, 10(25):271-273. [17] 苗雅楠, 骆泰庆, 王薇. 重症监护室中各类基础输液产品包装的卫生经济学评价[J]. 中国卫生资源, 2020, 23(3):241-247. doi: 10.3969/j.issn.1007-953X.2020.03.011 [18] TURPIN R S, CANADA T, LIU F X, et al. Nutrition therapy cost analysis in the US: pre-mixed multi-chamber bag vs compounded parenteral nutrition[J]. Appl Health Econ Health Policy, 2011, 9(5):281-292. doi: 10.2165/11594980-000000000-00000 [19] 奚秋磊, 钦伦秀, 陶国清, 等. 中长链脂肪乳氨基酸葡萄糖三腔袋与院内配制全合一肠外营养液临床应用比较[J]. 中国新药杂志, 2021, 30(18):1692-1697. doi: 10.3969/j.issn.1003-3734.2021.18.011 [20] 赵燕君, 赵霞, 谢兰桂, 等. 国内外对药品上市后包装材料的变更管理概述[J]. 中国药事, 2022, 36(8):903-912. [21] 钱锋, 徐鑫芬, 楼晓光. 全封闭式输液系统的临床应用[J]. 黑龙江护理杂志, 2000, (10):74-75. [22] 冯丽婵. 静脉输液过程中药物配制及静脉穿刺存在的安全隐患及对策[J]. 现代临床护理, 2010, 9(10):49-50. doi: 10.3969/j.issn.1671-8283.2010.10.022 -




 下载:
下载: