-
蛋白质作为生命体的主要执行者,其稳态性对细胞功能的正常发挥至关重要[1]。蛋白质的合成与降解是调控人体生命活动、维持生理平衡的关键机制[2]。在人体细胞内,主要存在两种蛋白质降解途径:泛素−蛋白酶体途径(ubiquitin-proteasome system, UPS)和溶酶体途径(lysosomal pathway system, LPS)。其中,泛素介导蛋白降解过程,控制着真核细胞中大部分蛋白质的降解,进而调控细胞的增殖、分化、凋亡、DNA修复和蛋白质的转录[3-4]。这一过程不仅涉及人体的免疫应答和病原体致病,还在生长发育、生殖及衰老等生命周期活动中发挥核心的控制作用[5-6]。
线性泛素化修饰是近年来研究发现的一种新型多聚泛素连接方式。去线性泛素化酶(OTU domain DUB with linear linkage specificity,OTULIN)是目前唯一报道可特异性水解线性泛素链的去泛素化酶(deubiquitinating enzymes,DUBs)[7]。OTULIN在机体多种生理和病理过程中具有关键调控作用,广泛参与细胞凋亡、信号转导、胚胎血管生成、免疫应答及炎症反应等生物学过程,并与OTULIN相关自身炎症综合征及肿瘤的发生发展密切相关[8-12]。OTULIN作为唯一能够特异性识别及水解线性泛素链的酶,在调控机体生命活动中具有独特作用,已成为新兴的研究热点,并有望成为治疗相关疾病的潜在靶点[13]。现关于OTULIN的功能研究仍处于初级阶段,迄今为止尚无其小分子配体的相关报道。OTULIN的具体功能尚未明确,新的机制有待进一步深入研究。
本研究基于OTULIN蛋白的结构与功能,构建全新的体外生物活性评价体系。体外分子水平实验因仅存在目标分子,可排除体内复杂环境带来的诸多干扰,是较为理想的实验环境。表达纯化得到线性泛素的底物蛋白,是构建OTULIN体外生物活性评价体系的重要基础。据文献报道,OTULIN作为唯一特异性切割线性泛素化的DUBs,其活性区域位于80~352片段[14],设计了特异性的全新底物蛋白组氨酸标签-泛素分子-泛素分子-flag标签(His-Ub-Ub-Flag),用于构建靶向OTULIN体外酶活评价方法。
-
NanoDrop超微量分光光度计(Thermo)、天平(Sartorius)、纯水仪(Millipore)、低温高速离心机(Eppendorf)、控温摇床(上海知楚仪器有限公司)、超声破碎仪(宁波新艺超声设备有限公司)、水浴锅(群安科学仪器有限公司)、超净台(江苏苏净集团有限公司)、垂直电泳槽(天能,VE-180)、电泳仪(天能,100-
1300 )、电泳槽(上海天能Tanon)、纯水仪(Millipore公司)和往复式脱色摇床(KYLIN-BELL公司)。 -
灭菌水、灭菌枪头、灭菌EP管、灭菌摇菌管、感受态细胞BL21、DH5α,LB培养基、Ni-NTA磁珠、酶蛋白诱导剂、蛋白酶抑制剂、β-D-硫代半乳糖苷(IPTG)、卡那霉素和咪唑。SDS/PAGE胶及电泳液(雅酶,LK309),转膜液5 × Transfer Buffer(BIO-RAD,
10026938 )、PVDF膜(Merck)、速溶型蛋白上样缓冲液5 × Loading buffer(雅酶,LT101S)、双色预染蛋白Marker(雅酶,WJ102)、无蛋白快速封闭液(雅酶,PS108P)、通用型抗体稀释液(雅酶,PS119L)、Alexa Fluor® 680 AffiniPure Goat Anti-Mouse IgG(H+L)(翌圣,33218ES60,1:25 000)、Alexa Fluor® 680 AffiniPure Goat Anti-Rabbit IgG(H+L)(翌圣,33118ES60,1:25 000)和Mouse anti His-Tag mAb(爱博泰克,AE003)。OTULIN质粒、His-Ub-Ub-Flag质粒、考马斯亮蓝快速免脱色染色液(派翠,KB0016)。 -
根据文献方法[15]分析OTULIN与底物蛋白Met1-diUb复合晶体结构(PDB:5OE7,2.95 Å),采用人源Met1-Ub基因序列,设计了首个人源His-Ub-Ub-Flag重组表达质粒,由南京金斯瑞生物科技有限公司进行全基因合成,测序正确。His-Ub-Ub-Flag质粒序列如下所示。
-
MGSSHHHHHHSSGLVPRGSHMQIFVKTLTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTLHLVLRLRGGMQIFVKTLTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTLHLVLRLRGGKLDYKDDDDK。
-
ATGGGCAGCAGCCATCATCATCATCATCACAGCAGCGGCCTGGTGCCGCGCGGCAGCCATATGCAGATCTTCGTGAAAACCCTTACCGGCAAGACCATCACCCTTGAGGTGGAGCCCAGTGACACCATCGAAAATGTGAAGGCCAAGATCCAGGATAAGGAAGGCATTCCCCCCGACCAGCAGAGGCTCATCTTTGCAGGCAAGCAGCTGGAAGATGGCCGTACTCTTTCTGACTACAACATCCAGAAGGAGTCGACCCTGCACCTGGTCCTGCGTCTGAGAGGTGGTATGCAGATTTTCGTGAAAACCCTGACCGGCAAAACCATTACCCTGGAAGTGGAACCGAGCGATACCATTGAAAATGTGAAAGCGAAAATTCAGGATAAAGAAGGCATTCCGCCGGATCAGCAGCGCCTGATTTTTGCGGGCAAACAGCTGGAAGATGGCCGCACCCTGAGCGATTATAACATTCAGAAAGAAAGCACCCTGCATCTGGTGCTGCGCCTGCGCGGCGGCAAGCTTGACTACAAGGACGACGATGACAAGTAA。
-
根据文献方法[16],采用大肠埃希菌BL21(DE3)感受态细胞进行转化。首先,将质粒干粉溶解于40 μl ddH2O中,充分混匀后配制成终浓度为100 ng/μl的质粒溶液。取2 μl质粒溶液加入50 μl BL21(DE3)感受态细胞中,轻轻混匀后置于冰上静置30 min。随后,将感受态细胞于42℃热激90 s,以促进质粒进入细胞内,并立即置于冰上静置。之后加入800 μl LB液体培养基,于37℃、140 r/min摇床中振荡培养1 h,以促进细胞复苏。
复苏结束后,将菌液于3 000 r/min离心2 min,弃去上清液,保留菌体沉淀,并用100 μl LB培养基重悬。由于His-Ub-Ub-Flag质粒具有卡那霉素抗性,取100 μl重悬菌液均匀涂布于含卡那霉素的LB固体培养基平板上,倒置于37℃恒温培养箱中过夜培养。次日观察菌落生长情况,结果显示His-Ub-Ub-Flag质粒已成功转化至BL21(DE3)感受态细胞中,用于后续诱导表达。
-
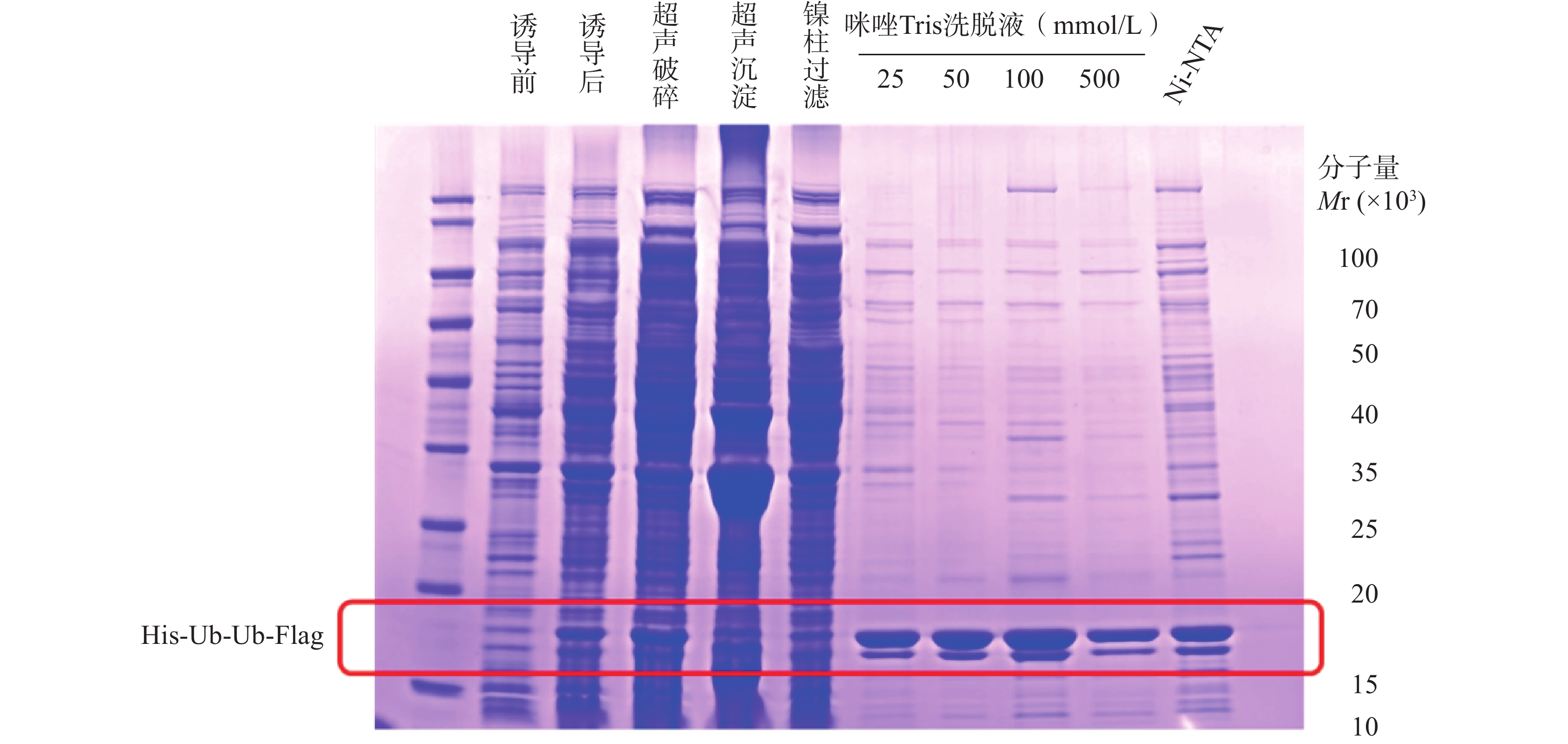
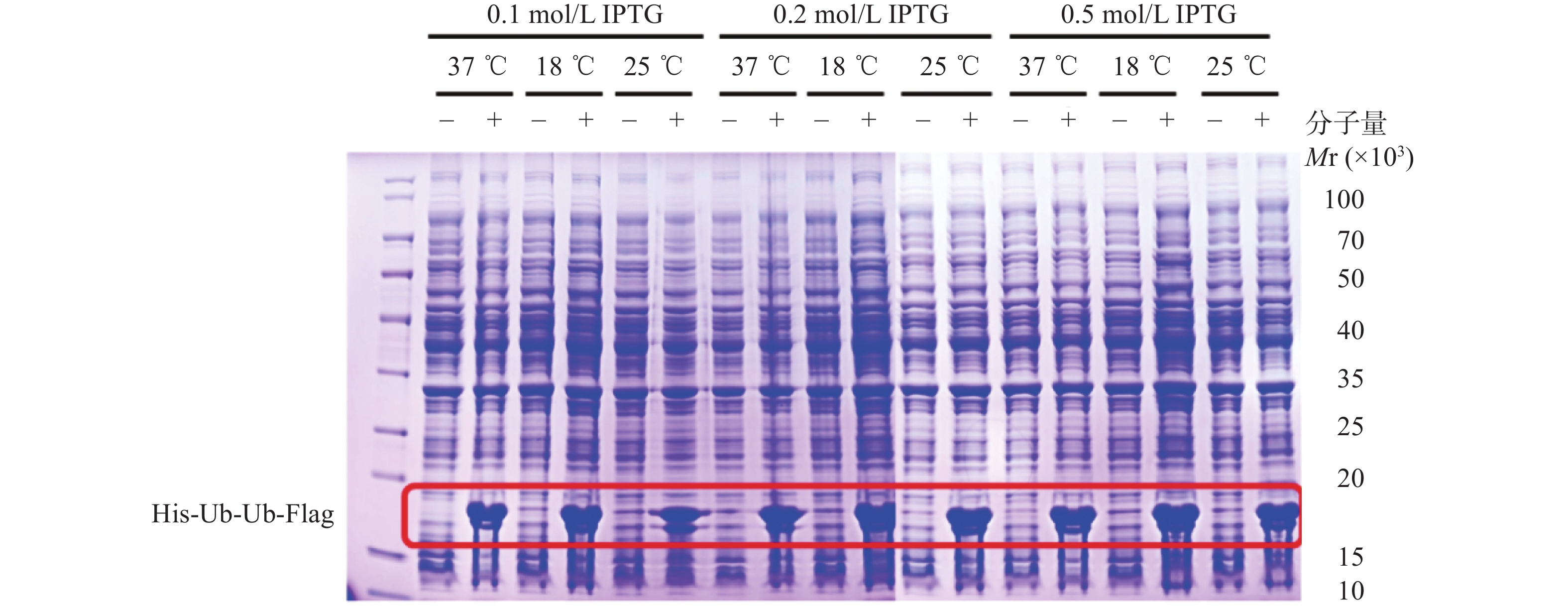
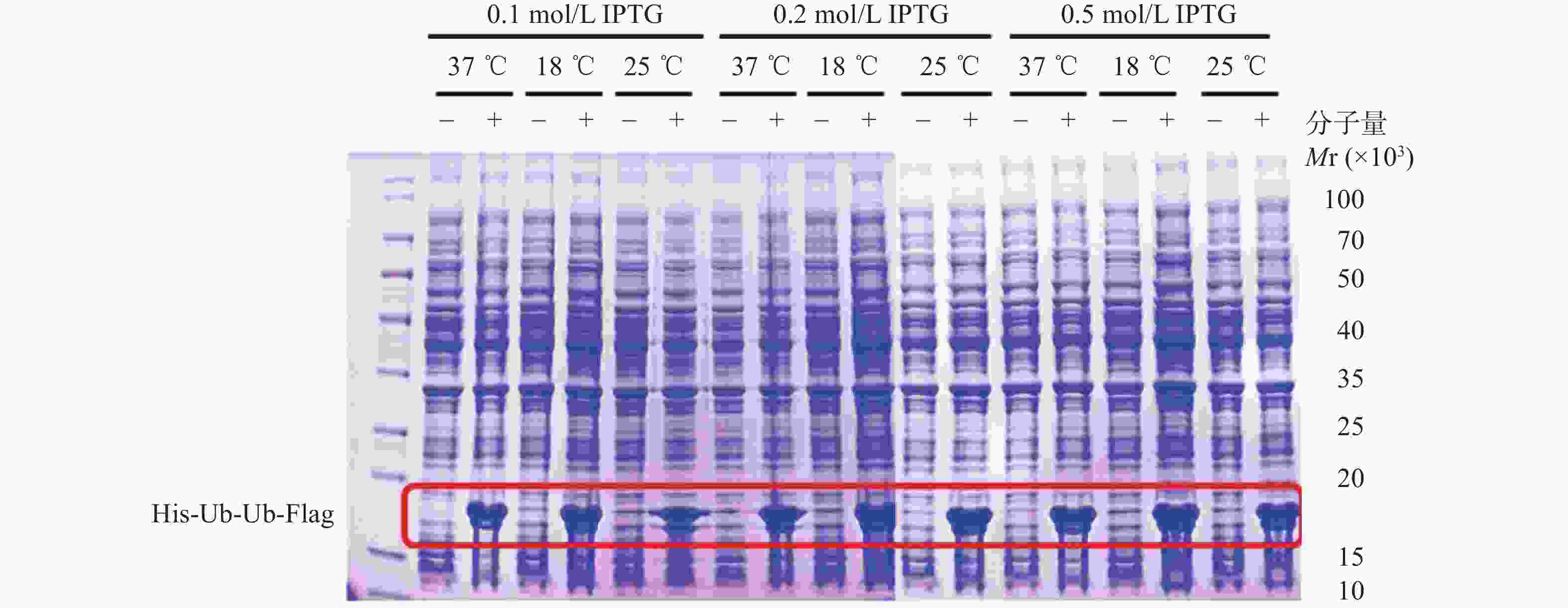
上述质粒转化实验结果显示,His-Ub-Ub-Flag在Escherichia coli (E.coli)的BL21转化效率较高。挑选单克隆菌落,转至3 ml含卡那霉素的LB液体培养基,置于37℃,220 r/min,摇床上震荡过夜,并收集小摇表达后的菌落。经过对蛋白诱导条件的摸索,考察不同浓度的异丙基-β-D-硫代半乳糖苷(Isopropyl-beta-D-thiogalactopyranoside,IPTG),在37、18、25℃温度下的蛋白诱导条件,分别将诱导得到的蛋白,电泳上样后用考马斯亮蓝染色方法检测蛋白纯度,发现最优的蛋白诱导条件为18℃,0.2 mmol/L IPTG,220 r/min,14~16 h(图1)。
-
挑选His-Ub-Ub-Flag质粒的在BL21中的单克隆菌落,取2 ml小摇菌液加入到准备好的具有卡那霉素抗性的400 ml LB液体培养基,置于37℃、220 r/min摇床上振荡过夜。待大摇菌液A值测试为0.6~1之间,加入0.2 mmol/L IPTG,置于18℃下,220 r/min,摇床振荡14~16 h诱导蛋白大量表达。次日,将大摇菌液分装50 ml离心管中,4℃,4 000 r/min,离心20 min。弃上清液,将菌落沉淀置于−80℃保存。
-
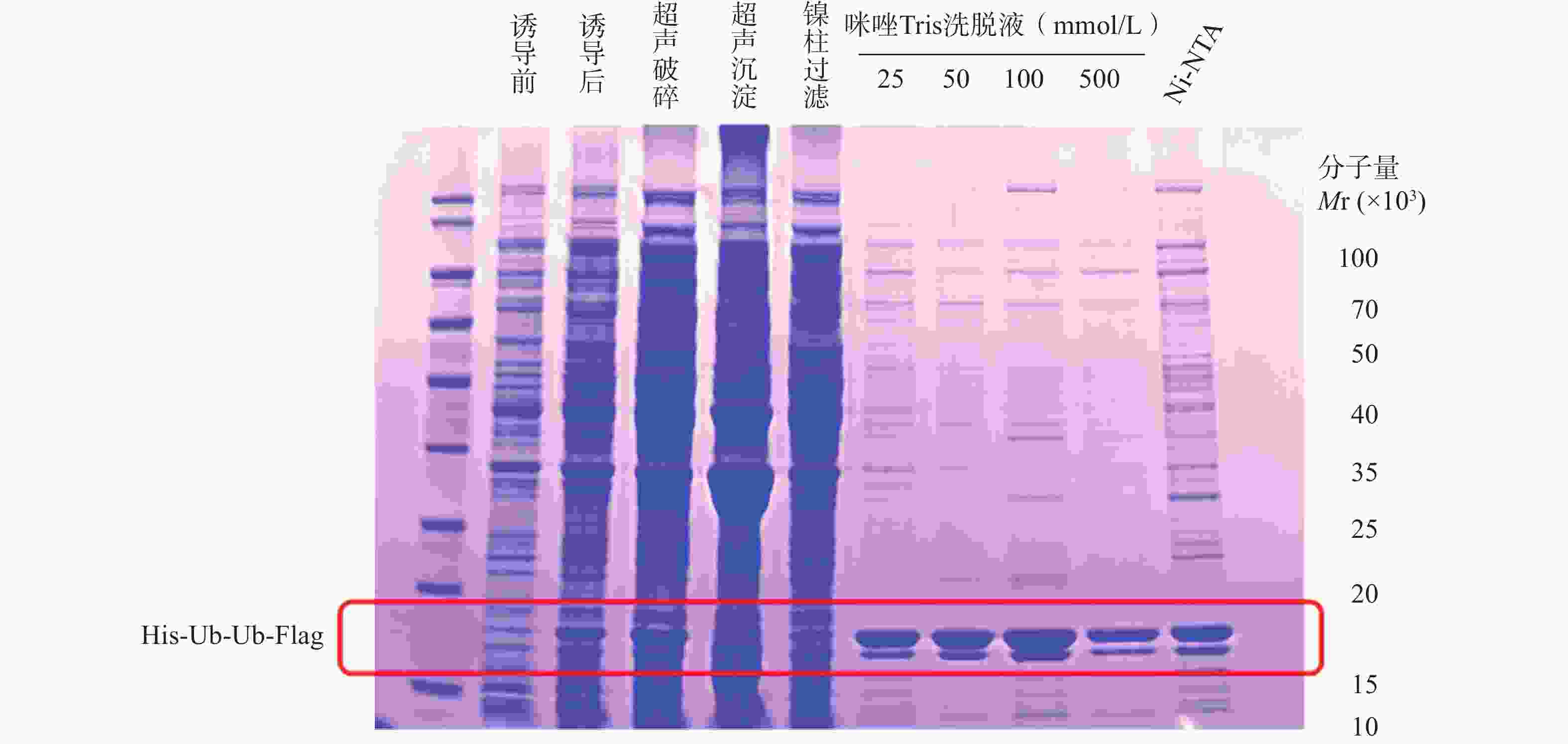
His-Ub-Ub-Flag表达载体携带6 × His Tag,蛋白大量表达后选用Ni2+离子亲和层析柱进行初步纯化。在蛋白纯化实验中,使用适量的蛋白裂解缓冲液buffer A(20 mmol/L Tris,500 mmol/L NaCl,pH 8.0)重悬菌体,离心后弃上清液,再加入适量蛋白酶抑制剂。将菌液置于超声破碎仪,破碎超声至菌液澄清。将菌液置于4℃,13 000 r/min,离心30 min。弃上清液,在沉淀中加入活化后的Ni-NTA磁珠共孵育。离心并弃上清液后,配制不同浓度比例咪唑的Tris buffer洗脱蛋白,反复清洗沉淀4次,洗脱掉不结合的杂蛋白,浓缩后收集目标蛋白。采用NanoDrop检测蛋白浓度,得到本批次His-Ub-Ub-Flag蛋白浓度为1.21 mg/ml。将每步留样蛋白依次上样电泳,用考马斯亮蓝染色法检测蛋白表达纯化结果,洗脱后得到符合分子量的蛋白条带(图2)。
-
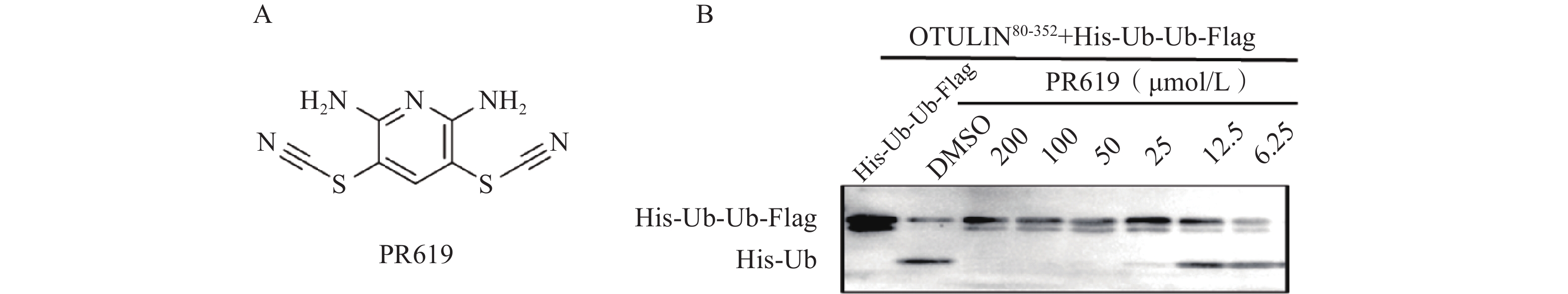
化合物2,6-二氨基-3,5-二硫氰基吡啶(2,6-Diamino-3,5-dithiocyanopyridine,PR619)可诱导细胞中多泛素化蛋白的积累,是非选择性且可逆的去泛素化酶抑制剂。文献报道PR619抑制多个DUBs蛋白的活性,如USP4(EC50=3.93 μmol/L),USP8(EC50=4.90 μmol/L),JOSD2(EC50=1.17 μmol/L),UCH-L3(EC50=2.95 μmol/L)[17-18]。经酶活评价验证,PR619具有浓度依赖性且可稳定抑制OTULIN蛋白的阳性对照药,其对OTULIN蛋白的EC50值为16.8 μmol/L(图3)。
-
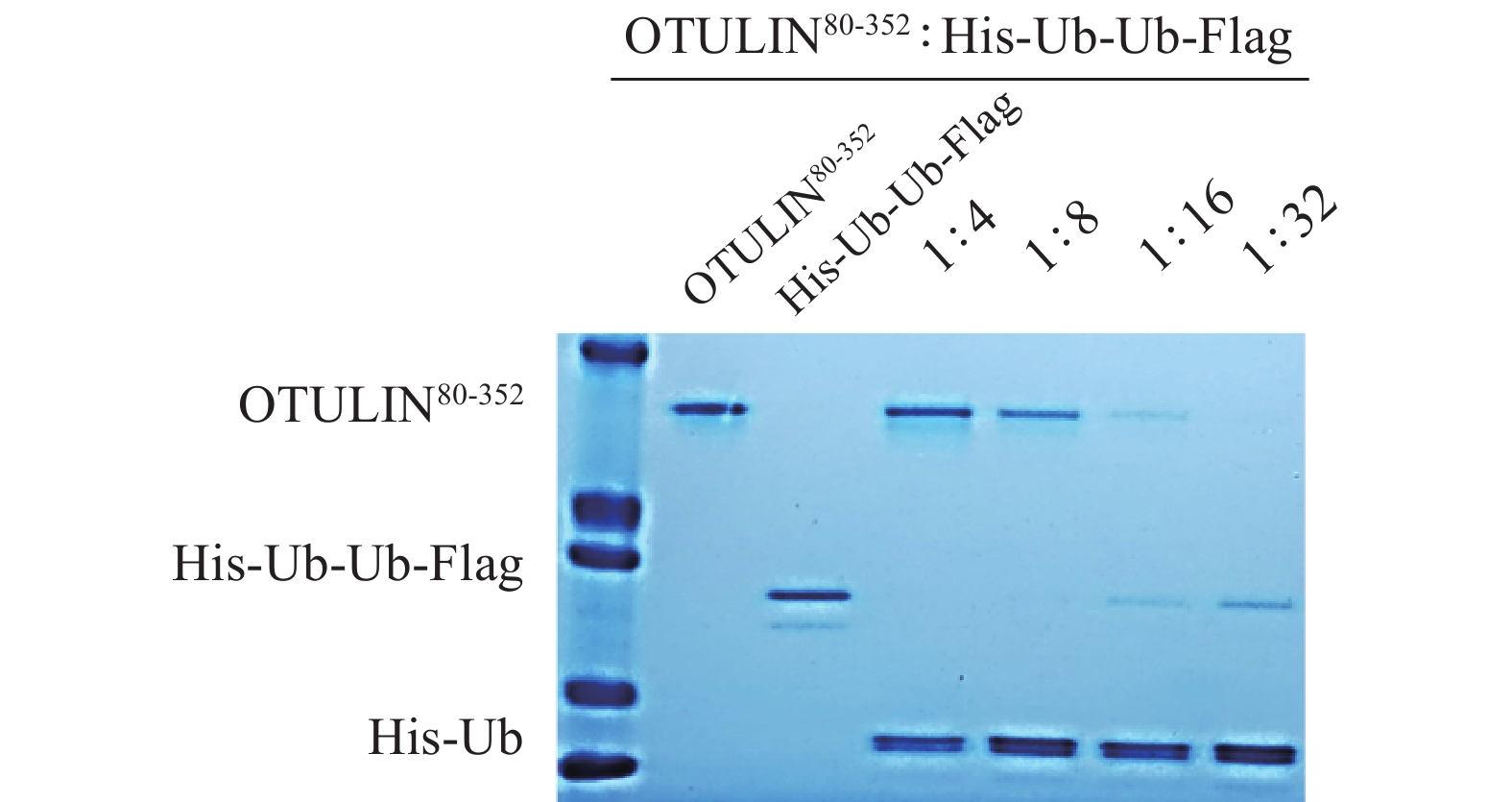
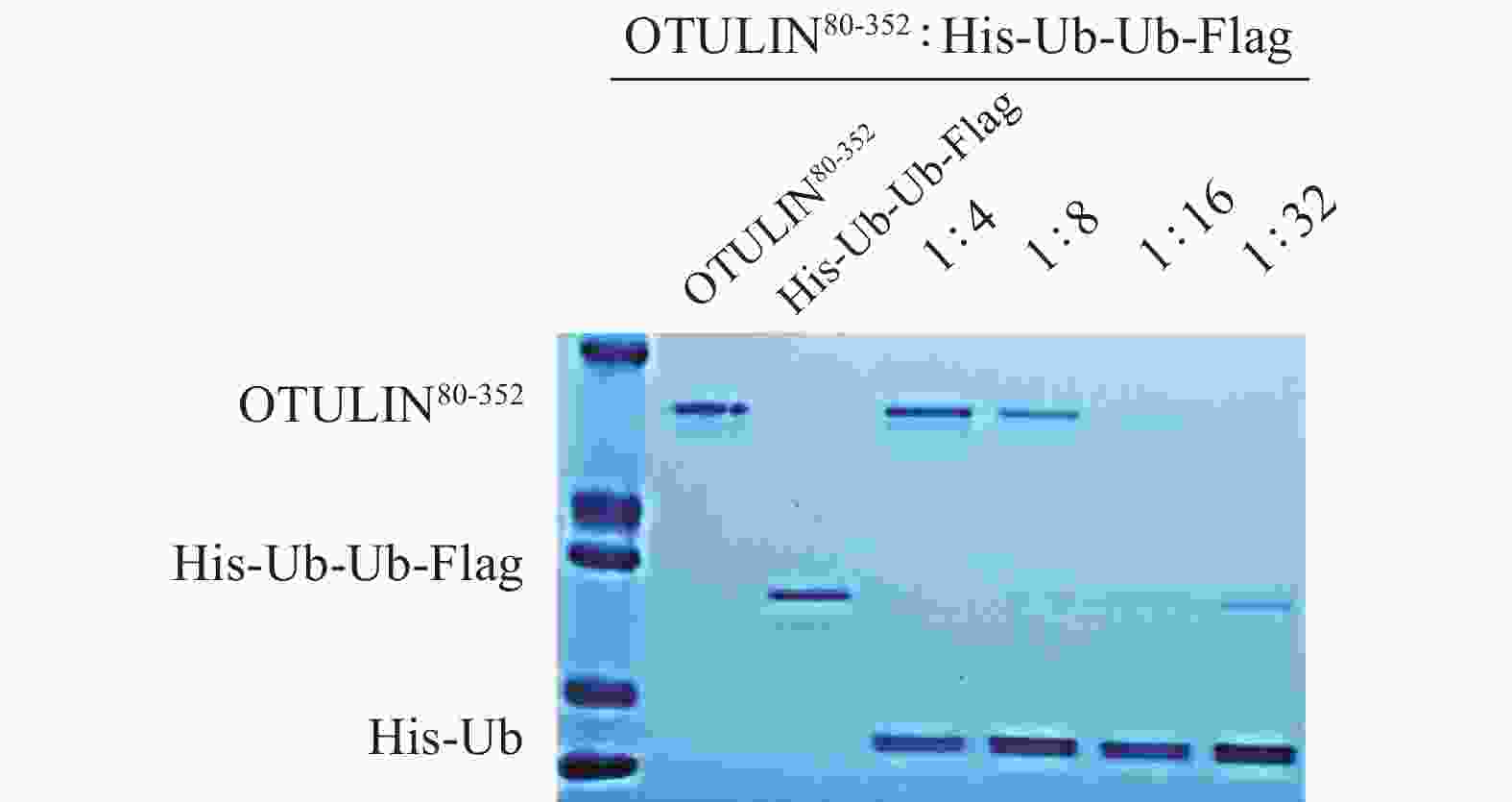
选用OTULIN活性片段(OTULIN80-352,分子量31 000),底物蛋白His-Ub-Ub-Flag,分子量20 500,阳性对照化合物PR619,空白对照DMSO。首先考察酶与底物蛋白在不同用量比下的酶活效率。将OTULIN80-352与PR619室温孵育,再加入底物蛋白His-Ub-Ub-Flag,37℃水浴孵育,电泳检测后用考马斯亮蓝染色法观察结果。根据实验结果,选择OTULIN80-352与底物蛋白His-Ub-Ub-Flag的用量比为1∶16,可清晰见到达酶切反应平衡的蛋白条带(图4)。
-
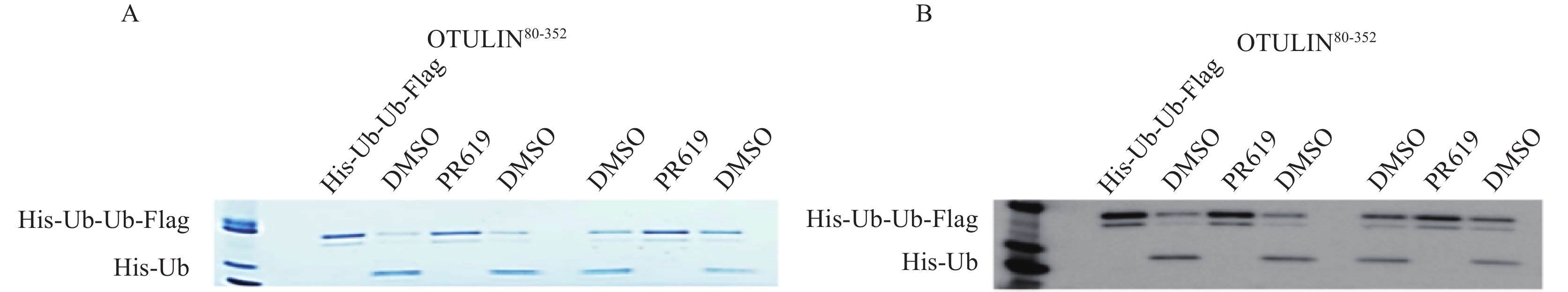
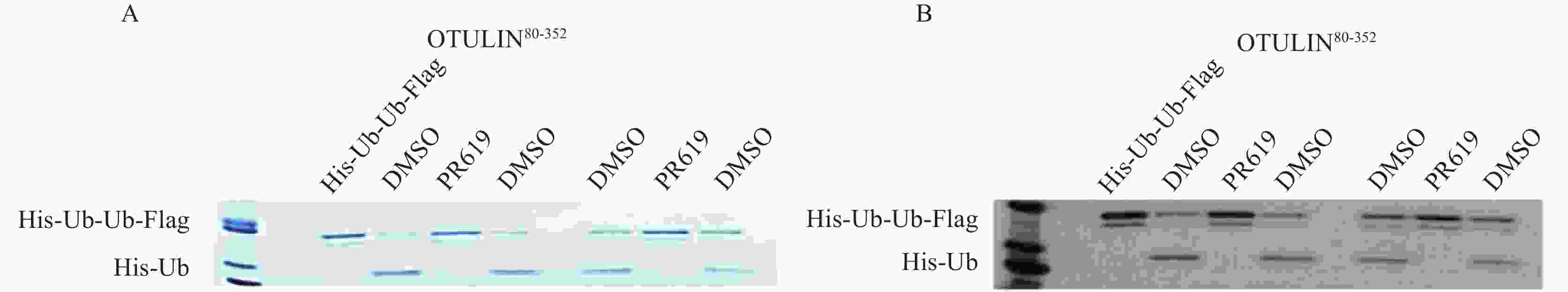
将30 μmol/L PR619与OTULIN80-352蛋白室温孵育30 min,加入相应的底物蛋白在37℃水浴下反应。电泳检测,考马斯亮蓝染色后对比观察。水浴37℃中反应10 min,酶切下的His-Ub条带不清晰,提示反应作用时间过短,水解不充分。当反应20 min时,可以明显观察到被OTULIN水解后的His-Ub蛋白。当反应30、40、60 min时,并无明显差异。为考察实验操作的一致性,每组条件设置2组DMSO组,为提高实验效率,选择酶水解底物反应条件为37℃,作用20 min,结果见图5。
-
在众多的蛋白质翻译后修饰(post-translational modification,PTM)类型中,线性泛素化因其独特的Met1连接方式,在NF-κB信号通路激活及炎症反应中发挥特异性作用。OTULIN作为该PTM的唯一已知逆转酶,其酶活性的精确调控直接决定了线性泛素化信号的强度与持续时间。为了建立高效的OTULIN活性检测体系,本研究首次成功构建、表达并纯化了线性泛素底物His-Ub-Ub-Flag。通过对酶与底物用量比及反应时间的梯度优化,确立了最佳酶促反应动力学窗口,在OTULIN蛋白与底物蛋白His-Ub-Ub-Flag用量是1∶16,37℃孵育20 min达到反应平衡,并采用广谱去泛素化酶抑制剂PR619作为阳性对照药物进行验证。实验结果显示,阳性对照药物PR619对OTULIN活性表现出明显的剂量依赖性抑制作用,证明了该体系对抑制剂检测的稳定性和灵敏度。利用构建的线性泛素蛋白底物,能有效评价去线性泛素化酶OTULIN的体外分子水平生物活性。
-
新药靶点的发现与确证是现代医药创新的核心驱动力。在众多药物类型中,小分子药物凭借其优良的理化性质及卓越的细胞膜透过能力,在靶向细胞内蛋白方面展现出天然优势。本研究聚焦的去线性泛素化酶OTULIN,作为线性泛素化这一特殊蛋白质翻译后修饰的唯一特异性逆转酶,在维持PTM动态平衡、调控NF-κB信号通路及先天免疫稳态中发挥着不可替代的作用。鉴于OTULIN功能异常与肿瘤及免疫疾病的密切关联,开发针对该靶点的特异性小分子抑制剂具有重要的转化医学价值。
本研究致力于解决OTULIN靶向药物筛选的方法学难题,成功构建了一套稳定、精准的体外活性评价体系,实现了对候选化合物抑制效应的定量评估。该体系的建立,不仅为解析OTULIN介导的PTM去修饰机制提供了有力工具,更为后续针对该潜在新药靶点开展高内涵、高通量的药物筛选提供了全新的技术方法。
Establishment of in vitro biological activity evaluation system for OTULIN
doi: 10.12206/j.issn.2097-2024.202601035
- Received Date: 2026-01-20
- Accepted Date: 2026-05-09
- Rev Recd Date: 2026-04-09
- Available Online: 2026-05-22
- Publish Date: 2026-05-25
-
Key words:
- OTULIN /
- linear ubiquitin /
- in vitro bioactivity /
- enzyme activity evaluation
Abstract:
| Citation: | XIA Zhewei, LI Yu, SHENG Chunquan. Establishment of in vitro biological activity evaluation system for OTULIN[J]. Journal of Pharmaceutical Practice and Service, 2026, 44(5): 259-263. doi: 10.12206/j.issn.2097-2024.202601035 |








 DownLoad:
DownLoad: