-
钠-葡萄糖协同转运蛋白2(sodium-dependent glucose transporters 2,SGLT2)抑制剂是一类新型口服降糖药,其通过抑制近端小管对葡萄糖的重吸收,增加葡萄糖从尿液中排泄,从而降低血糖,是一种不依赖于胰岛素的降糖药[1]。目前,我国上市的SGLT2抑制剂有达格列净、恩格列净、卡格列净、艾格列净、恒格列净和贝沙格列净6种。SGLT2抑制剂因降糖疗效确切,兼具心、肾保护等优势[2],临床应用广泛,但也存在一些安全性问题。据国外研究,SGLT2抑制剂可使2型糖尿病(type 2 diabetes mellitus,T2DM)患者发生糖尿病酮症酸中毒(diabetic ketoacidosis,DKA)的风险增加至少7倍,其中71%为非高血糖性酮症酸中毒(euglycemic diabetic ketoacidosis,euDKA)[3]。DKA作为一种严重的糖尿病急性并发症,主要特点是起病急、进展快,患者表现为高血糖、酮症和代谢性酸中毒等,严重者可危及生命[4]。然而,与DKA不同的是,SGLT2抑制剂相关euDKA患者的血糖升高往往不显著,多饮、多尿等症状也不明显,易被临床忽视而延误治疗,造成严重后果[5]。因此,本研究探讨SGLT2抑制剂相关euDKA的影响因素并构建风险预测模型,以期为其预防和早期诊治提供参考。
-
回顾性分析2020年1月至2023年12月于厦门大学附属东南医院接受SGLT2抑制剂治疗的T2DM住院患者的临床资料。纳入标准:①T2DM患者,糖尿病诊断及分型符合《中国2型糖尿病防治指南(2020年版)》的标准[6];②患者接受SGLT2抑制剂治疗,包括达格列净、恩格列净、卡格列净等;③年龄≥18岁。排除标准:①1型糖尿病患者;②未使用SGLT2抑制剂的患者;③出现DKA的患者;④临床资料不完整或失随访的患者;⑤合并重要脏器功能明显异常的患者。本研究经厦门大学附属东南医院医学伦理委员会批准通过。
-
收集患者的临床资料,包括:①个人信息:年龄、性别、体质指数等;②既往史:吸烟史、酗酒史、DKA史、消化系统病史、用药期间手术史;③现病史:是否入院前3 d食欲或进食下降和糖尿病病程等;④实验室检验:糖化血红蛋白、入院血糖、白细胞计数、中性粒细胞计数、淋巴细胞计数、血小板总数、估算肾小球滤过率(estimated glomerular filtration rate,eGFR)、总胆红素、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、甘油三酯(triglyceride,TG)、胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)等、C-反应蛋白(c-reactive protein,CRP)、降钙素原(procalcitonin,PCT)等;⑤合并疾病:高血压、感染、动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)等;⑥治疗方案:SGLT2抑制剂种类、用法用量、用药疗程、是否院前调整降糖药以及联合其他降糖药情况等;⑦结局指标:是否出现euDKA:入院末梢或静脉血清葡萄糖<13.9 mmol/L、伴阴离子间隙升高的代谢性酸中毒(pH<7.3和血清碳酸氢盐<18 mEq/L)和酮症[7]。
-
运用SPSS 21.0软件进行统计学分析,对符合正态性检验的计量资料,用($ \overline{x} $±s)表示,两组比较采用独立样本t检验;对不符合正态性检验的计量资料,用中位数和四分位数间距表示,两组比较采用Man-Whitney U检验;计数资料用例数(百分比)表示,两组比较采用χ2检验。采用多因素Logistic回归分析SGLT2抑制剂相关euDKA的独立影响因素,并建立风险预测模型。根据受试者工作特征(receiver operating characteristic curve,ROC)曲线确定预测模型的曲线下面积(area under the curve,AUC)及临界值[8]。P<0.05表示差异有统计学意义。应用Python 3.8软件对模型样本进行十折交叉验证[9]。
-
119例患者中,男性68例(57.14%),女性51例(42.86%);平均年龄(57.31±12.28)岁;平均体质指数(24.39±2.95)kg/m2;达格列净11例(9.24%),恩格列净56例(47.06%),卡格列净52例(43.70%);所有患者均使用低剂量的SGLT2抑制剂(如达格列净5 mg/d、恩格列净10 mg/d、卡格列净100 mg/d)。
-
共纳入119例患者,其中21例(17.65%)发生euDKA。21例患者均表现为恶心、呕吐、腹泻等消化道症状,其中1例患者出现明显嗜睡。发生euDKA后,患者均立即停用口服降糖药,改用小剂量胰岛素降糖,并积极给予补液消酮、纠酸等对症措施。所有患者均好转后出院,出院后未再使用SGLT2抑制剂。
-
根据是否出现euDKA将119例患者分为非euDKA组98例和euDKA组21例。两组患者的年龄、吸烟史、DKA病史、用药期间手术史等23项临床资料比较,差异有统计学意义(P<0.05),见表1。
项目 非euDKA组(n=98) euDKA组(n=21) u/χ2/t值 P值 年龄[岁,M(P25,P75)] 60.00(29.00,85.00) 50.00(24.00,75.00) −2.291 0.022 性别[男,n(%)] 52(53.06) 16(76.19) 3.778 0.052 体质指数(kg/m2,$ \overline{x} $±s) 24.62±2.87 23.30±3.12 1.873 0.064 吸烟史[n(%)] 21(21.43) 9(42.86) 4.212 0.040 酗酒史[n(%)] 7(7.14) 5(23.81) 3.619 0.057 DKA史[n(%)] 6(6.12) 5(23.81) 4.513 0.034 消化系统病史[n(%)] 42(42.86) 5(23.81) 2.626 0.105 用药期间手术史[n(%)] 52(53.06) 2(9.52) 13.225 <0.001 入院前3 d食欲或进食下降[n(%)] 4(4.08) 12(57.14) 37.405 <0.001 糖尿病病程 <1年[n(%)] 7(7.14) 1(4.76) <0.001 1.000 1~10年[n(%)] 39(39.80) 16(76.19) 9.216 0.002 >10年[n(%)] 52(53.06) 4(19.05) 8.031 0.005 糖化血红蛋白[%,M(P25,P75)] 7.95(5.40,13.40) 10.50(6.50,15.10) 3.319 0.001 入院血糖[mmol/L,M(P25,P75)] 8.22(3.01,29.20) 10.30(6.50,13.72) 2.523 0.012 白细胞计数[×109/L,M(P25,P75)] 6.68(2.78,14.46) 11.65(5.24,24.22) 4.186 <0.001 中性粒细胞计数[×109/L,M(P25,P75)] 3.55(1.79,12.89) 8.18(3.26,16.88) 5.507 <0.001 淋巴细胞计数(×109/L,$ \overline{x} $±s) 2.07±0.67 1.95±1.48 0.356 0.725 血小板总数[×109/L,M(P25,P75)] 231.50(101.00,358.00) 289.00(146.00,403.00) 2.558 0.011 eGFR[ml/(min·1.73m2),$ \overline{x} $±s] 95.41±32.31 106.68±35.47 −1.426 0.157 总胆红素(µmol/L,$ \overline{x} $±s) 11.51±5.50 13.41±11.70 −1.136 0.258 ALT(U/L,$ \overline{x} $±s) 29.59±40.99 23.93±19.51 0.617 0.539 AST(U/L,$ \overline{x} $±s) 22.01±17.87 21.09±9.87 0.230 0.818 TG(mmol/L,$ \overline{x} $±s) 3.61±14.42 3.10±3.32 0.161 0.872 TC(mmol/L,$ \overline{x} $±s) 4.39(2.33,8.94) 5.24(2.98,11.87) 3.004 0.003 HDL-C(mmol/L,$ \overline{x} $±s) 1.08±0.27 0.99±0.27 1.296 0.198 LDL-C(mmol/L,$ \overline{x} $±s) 2.46(0.85,5.66) 3.51(1.43,5.35) 3.067 0.002 CRP(mg/L,$ \overline{x} $±s) 2.31(0.07,341.00) 6.27(0.05,360.74) 2.938 0.003 PCT(ng/mL,$ \overline{x} $±s) 0.03(0.01,7.62) 0.06(0.01,12.15) 3.011 0.003 合并疾病 高血压[n(%)] 50(51.02) 3(14.29) 9.448 0.002 感染[n(%)] 17(17.35) 12(57.14) 14.860 <0.001 ASCVD[n(%)] 34(34.69) 7(33.33) 0.014 0.905 治疗方案 达格列净[n(%)] 6(6.12) 5(23.81) 4.513 0.034 恩格列净[n(%)] 46(46.94) 10(47.62) 0.003 0.955 卡格列净[n(%)] 46(46.94) 6(28.57) 2.371 0.124 用药疗程 <1月[n(%)] 16(16.33) 6(28.57) 1.004 0.316 1月~1年[n(%)] 54(55.10) 5(23.81) 6.774 0.009 >1年[n(%)] 28(28.57) 10(47.62) 2.887 0.089 院前调整降糖药 2(2.04) 7(33.33) 19.954 <0.001 联合其他降糖药情况 联合二甲双胍[n(%)] 64(65.31) 19(90.48) 5.193 0.023 联合磺脲类/非磺脲类 [n(%)] 38(38.78) 3(14.29) 4.593 0.032 联合α-糖苷酶抑制剂[n(%)] 44(44.90) 9(42.86) 0.029 0.864 联合噻唑烷二酮类[n(%)] 8(8.16) 4(19.05) 1.219 0.270 联合二肽基肽酶-4抑制剂[n(%)] 31(31.63) 5(23.81) 0.502 0.479 联合胰高血糖素样肽-1受体激动剂[n(%)] 7(7.14) 2(9.52) 0.140 0.708 联合胰岛素[n(%)] 34(34.69) 4(19.05) 1.948 0.163 注:DKA:糖尿病酮症酸中毒;eGFR:估算肾小球滤过率;ALT:丙氨酸氨基转移酶;AST:天门冬氨酸氨基转移酶;TG:甘油三酯;TC:胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;CRP:C-反应蛋白; PCT:降钙素原;ASCVD:动脉粥样硬化性心血管疾病。 -
以上述单因素分析中有统计学意义的变量作为自变量(二分类变量,否=0,是=1;糖尿病病程:<1年=0,1~10年=1,>10年=2;用药疗程:<1月=0,1月~1年=1,>1年=2;连续变量采用原数据),以患者是否出现euDKA为因变量(未出现=0,出现=1),进行多因素 Logistic回归分析。结果显示,DKA病史、入院前3 d食欲或进食下降、中性粒细胞计数升高、院前调整降糖药是增加SGLT2抑制剂相关euDKA风险的独立影响因素;而用药期间手术史是降低其风险的独立影响因素,见表2。
项目 回归系数B 标准误S.E 卡方值Waldχ2 自由度df 比值比OR 95%CI置信区间 P值 DKA病史 4.738 2.017 5.515 1 114.153 2.189~5 952.744 0.019 用药期间手术史 −4.956 1.958 6.410 1 0.007 0.000~0.326 0.011 入院前3 d食欲或进食下降 3.081 1.262 5.957 1 21.774 1.834~258.463 0.015 中性粒细胞计数 0.721 0.202 12.678 1 2.056 1.383~3.058 <0.001 院前调整降糖药 3.823 1.483 6.649 1 45.745 2.502~836.278 0.010 常量 −6.575 1.564 17.666 1 0.001 / <0.001 -
以上述5个独立影响因素建立Logistic回归方程,Logit(P)= 4.738(DKA病史)−4.956(用药期间手术史)+3.081(入院前3 d食欲或进食下降)+0.721(中性粒细胞计数)+3.823(院前调整降糖药)−6.575,采用H-L法(Hosmerand Lemeshow test)对模型的拟合度进行检验,结果显示模型拟合良好(χ2值=3.557,P=0.895)。对上述回归方程转换后得出预测模型的计算公式=中性粒细胞计数+6.571(DKA病史)−6.874(用药期间手术史)+4.273(入院前3 d食欲或进食下降)+ 5.302(院前调整降糖药)。
-
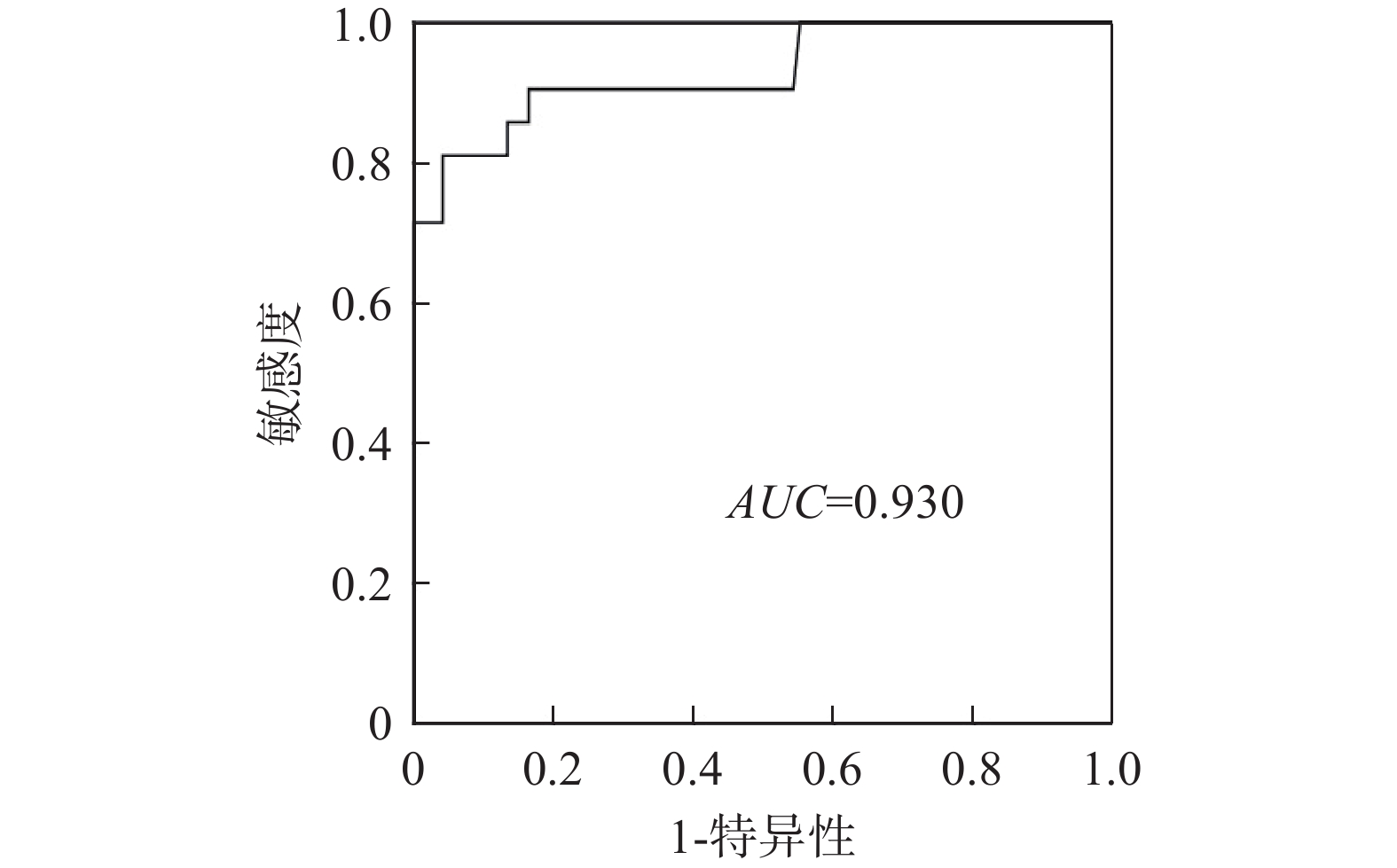
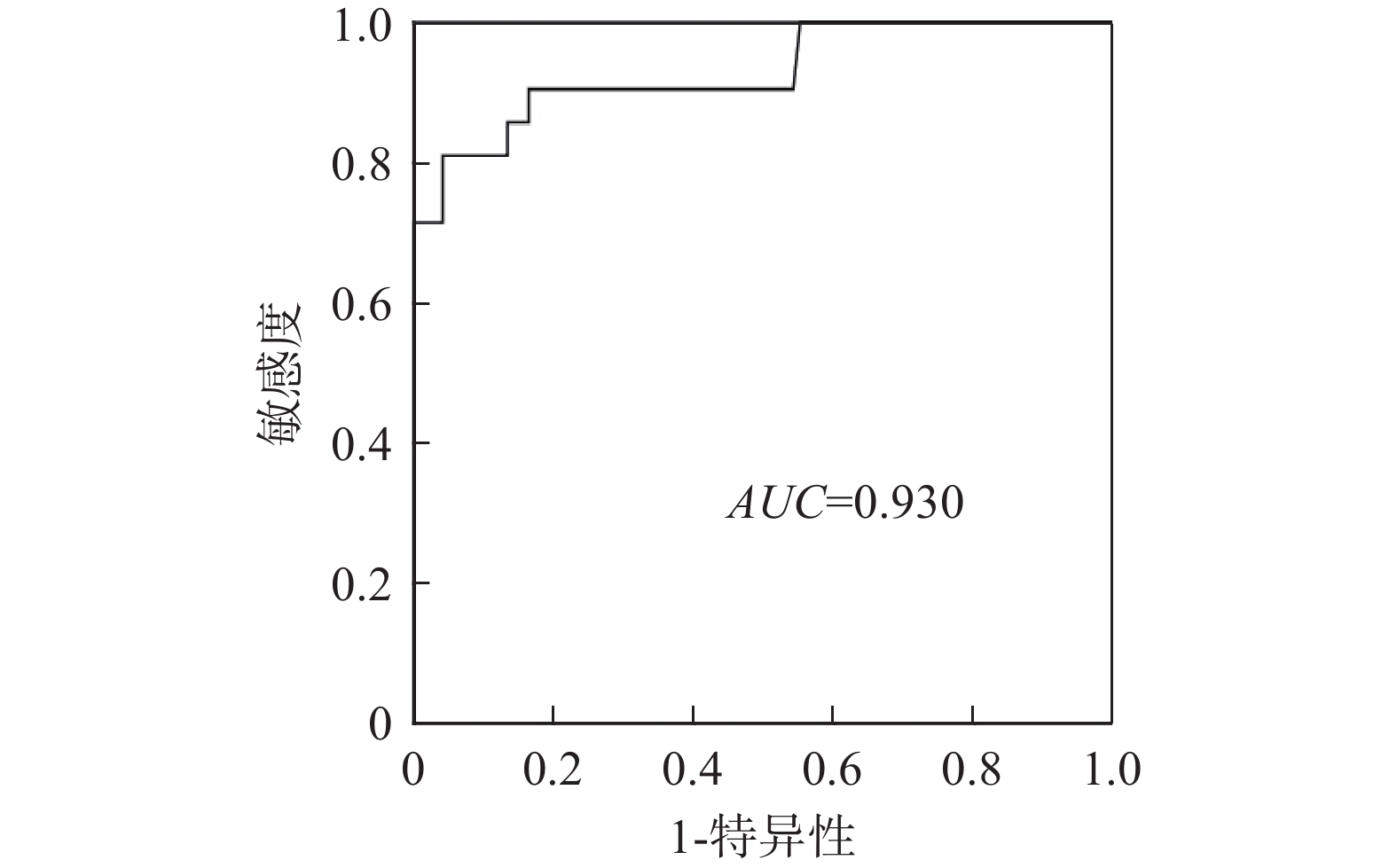
预测模型ROC曲线的AUC为0.982(P<0.001),准确率为94.96%,敏感度为0.905,特异性为0.959,临界值为7.405,见表3。模型十折交叉验证后预测模型ROC曲线的AUC为0.930,预测效果好,见图1。在预测模型外部验证的过程中,本研究选取2024年1月至12月期间符合纳排标准的34例住院患者作为验证集。将上述患者的中性粒细胞计数、DKA病史、用药期间手术史、入院前3 d食欲或进食下降、院前调整降糖药的数据代入计算公式中,得分高于7.405则表示存在euDKA高风险,并将预测结果与实际情况比较。结果显示,正确29例,假阴性3例,假阳性2例,模型预测的准确率为85.29%。
项目 最佳临界值 敏感度 特异性 约登指数 AUC P 中性粒细胞计数 4.555 0.905 0.755 0.660 0.884(0.805~0.963) <0.001 DKA病史 0.500 0.238 0.939 0.177 0.588(0.443~0.734) 0.205 用药期间手术史 0.500 0.952 0.469 0.422 0.282(0.176~0.388) 0.002 入院前3 d食欲或进食下降 0.500 0.571 0.959 0.531 0.765(0.630~0.901) <0.001 院前调整降糖药 0.500 0.333 0.980 0.313 0.656(0.509~0.804) 0.025 预测模型 7.405 0.905 0.959 0.864 0.982(0.961~1.000) <0.001 -
euDKA是一种隐匿发病的糖尿病急症,特点是患者的血或尿酮体升高、碳酸氢盐降低伴阴离子间隙升高的代谢性酸中毒(pH<7.3),但血糖升高不明显,通常不超过13.9 mmol/L[10-11]。早在2015年,Hayami等[12]报道了全球首例由SGLT2抑制剂引起的euDKA。同年12月,美国FDA报告了73例患者服用SGLT2抑制剂后出现DKA,其中部分患者表现为euDKA[13]。由于euDKA易被漏诊,此前的研究中euDKA的比例较低,仅占所有DKA的2.6%~3.2%[14]。但随着SGLT2抑制剂临床应用增加,euDKA的发生率也有所增加。Goldenberg等[15]最新的研究发现,SGLT2抑制剂相关euDKA占所有DKA的比例高达70%,需格外重视。
SGLT2抑制剂诱发euDKA的可能机制主要包括:①促进尿糖排泄,降低血糖水平,一方面刺激胰高血糖素,增加糖异生,使代谢底物从碳水化合物转变为脂质[16];另一方面胰岛素分泌减少,对脂肪动员的抑制减弱,上述两方面均导致酮体生成增多[17];②抑制近端小管对钠和葡萄糖的重吸收,通过管球反馈降低肾脏对酮体的清除率[18];③利钠和渗透性利尿作用,造成血容量减少,激活下丘脑-垂体-肾上腺轴,分泌皮质醇和儿茶酚胺增多,加速脂肪动员,进一步增加酮体生成[19]。由此可见,SGLT2抑制剂可通过多种途径造成酮体在体内蓄积,引发酮症酸中毒。同时,SGLT2抑制剂促进尿糖排泄,导致机体出现血糖不高的酮症酸中毒状态,即euDKA。
有研究报道,SGLT2抑制剂相关euDKA的诱因包括合并急症(如感染、心肌梗死等)、手术、创伤、低血容量、饥饿或低碳水化合物饮食、胰岛素停用或减量以及饮酒等[20]。Bamgboye等[21]研究证实,感染如肺炎、胰腺炎、脓肿、败血症等均可引起euDKA。原因可能与感染导致碳水化合物的消耗减少,增加酮体生成有关[22]。中性粒细胞计数是临床上判断感染性疾病最常用的指标之一,其升高与炎性反应密切相关,细菌感染时更为明显[23]。本研究的结果同样得出,中性粒细胞计数升高的感染患者,SGLT2抑制剂相关euDKA的风险增加。
SGLT2抑制剂围术期用药的安全性,长期以来备受关注。Kameda等[24]研究发现,围术期患者使用SGLT2抑制剂易出现euDKA。Burke等[25]研究认为,约30%的患者术后服用SGLT2抑制剂可出现euDKA。患者术前常规禁食致血糖降低,胰岛素用量减少,术后应激又升高血糖,血糖调节失去平衡,促进脂肪氧化产生酮体,可能是围术期易出现SGLT2抑制剂相关euDKA的主要原因[26]。此前,美国内分泌协会曾建议择期手术患者术前1~3 d停用SGLT2抑制剂[27]。本研究结果显示,既往存在SGLT2抑制剂用药期间手术史的患者相比未行手术的患者出现euDKA的风险降低。因此,对于SGLT2抑制剂用药期间首次进行手术的患者,需特别警惕其euDKA的风险,应考虑术前1~3 d停止用药以降低该风险。
另外,与此前的报道相同的是,入院前3 d食欲或进食下降和院前调整降糖药也是SGLT2抑制剂相关euDKA的影响因素。减肥、限制饮食(尤其是生酮饮食)均会导致脂肪分解增加,酮体生成增多,出现euDKA的风险增高[11]。院前调整降糖药(尤其是胰岛素减量或停药)可能导致胰岛素相对缺乏,同样也会刺激脂肪组织动员,产生酮体[28]。除此之外,本研究还发现既往有DKA病史的患者出现SGLT2抑制剂相关euDKA的风险更高,可能与该类患者长期饮食不规律、用药依从性不高、不良生活习惯较多等有关。
综上所述,本研究结果显示DKA病史、入院前3 d食欲或进食下降、中性粒细胞计数升高和院前调整降糖药是增加SGLT2抑制剂相关euDKA风险的影响因素;用药期间手术史是降低该风险的影响因素。联合上述影响因素构建的预测模型对SGLT2抑制剂相关euDKA风险具有较好的预测价值,为早期预防和诊治提供了决策依据。
Risk factors analysis and prediction model construction of SGLT2 inhibitor-associated euglycemic diabetic ketoacidosis
doi: 10.12206/j.issn.2097-2024.202403056
- Received Date: 2024-03-27
- Rev Recd Date: 2025-01-21
- Available Online: 2026-04-30
-
Key words:
- sodium-dependent glucose transporters 2 /
- SGLT2 inhibitor /
- euglycemic diabetic ketoacidosis /
- type 2 diabetes /
- prediction model
Abstract:
| Citation: | HUANG Wenhui, CHEN Xiufen, CHEN Jianming, HONG Yana, CAI Jingjing, CHEN Jinshan. Risk factors analysis and prediction model construction of SGLT2 inhibitor-associated euglycemic diabetic ketoacidosis[J]. Journal of Pharmaceutical Practice and Service. doi: 10.12206/j.issn.2097-2024.202403056 |







 DownLoad:
DownLoad: