-
中药配方颗粒是以符合标准的单味中药饮片为原料,经现代工艺提取、浓缩、制粒而成的一种新型中药制剂[1]。1992年,国家批准了试点生产企业进行中药配方颗粒研发,2001年,将其规范命名为“中药配方颗粒”,同时纳入中药饮片管理范畴。2021年国家先后公布了两批次196种配方颗粒的国家标准[2-3],标志着中药配方颗粒正式步入历史舞台。地龙配方颗粒目前仍属于企业在研品种,由于药材来源、制备工艺和质量标准不同,其产品质量亦存在差异,加之2020年版《中国药典》中地龙项下缺少指标成分和定量评价方法[4],使其仍缺少统一的评价指标。
核苷类成分是地龙舒张支气管、抗组胺、平喘的物质基础[5],通过对核苷类成分的评测,可在一定程度上反映地龙药材和配方颗粒的内在质量。有研究表明,利用高效液相色谱法(HPLC)建立的特征图谱,能较好地表征地龙药材中核苷类成分[6-7],同时可对其进行含量测定[8-12],也有用该方法测定地龙配方颗粒中次黄嘌呤的含量并对其进行质量评价的研究报道[13-14]。本研究采用高效液相色谱法测定不同厂家地龙配方颗粒中次黄嘌呤、肌苷、鸟苷和腺苷4种核苷类成分的含量,并应用《中药色谱指纹图谱相似度评价系统(2012.130723版)》建立指纹图谱进行质量评价。
-
Thermo Vanquish Core高效液相色谱仪(赛默飞世尔科技有限公司);Thermo AcclaimTM120 C18色谱柱(4.6 mm × 250 mm,5 μm)。EX125DZH型十万分之一电子分析天平(奥豪斯仪器(常州)有限公司);ME204E/02型万分之一电子分析天平(梅特勒-托利多有限公司);SB-5200DTD型超声波清洗机(上海般诺生物科技有限公司)。
-
乙腈(上海泰坦科技股份有限公司);水(屈臣氏蒸馏水)。
-
尿嘧啶对照品(批号:B20908),次黄嘌呤对照品(批号:B20211),尿苷对照品(批号:B20907),鸟苷对照品(批号:B20902),肌苷对照品(批号:B20582),以上对照品购自上海源叶生物科技有限公司;黄嘌呤对照品(批号:C12004027,上海阿拉丁生化科技股份有限公司);腺苷对照品(批号:SA8060,北京索莱宝科技有限公司);纯度均大于98%。地龙对照药材(参环毛蚓,Pheretima,批号:120987-201508,中国食品药品检定研究所);样品S1~S10为不同厂家或批次生产的地龙配方颗粒。
-
Thermo AcclaimTM120 C18色谱柱(4.6 mm×250 mm,5 μm);流动相乙腈(A)-水(B),梯度洗脱,洗脱条件见表1;流速0.6 ml/min;柱温25 ℃;检测波长254 nm;进样量10 μl。理论塔板数按肌苷峰计算不小于3500。
时间 (min) 流动相比例(%) 流动相A 流动相B 0~15 2 98 15~25 2~3 98~97 25~30 3~8 97~92 30~40 8~20 92~80 40~50 20 80 50~55 20~50 80~50 55~60 50~100 50~0 60~63 100 0 63~68 100~2 0~98 -
取地龙对照药材约0.5 g,精密称定,置具塞锥形瓶中,精密加入双蒸水50 ml,称定重量。于60 ℃水浴30 min,再超声(功率300 W,频率40 kHz)30 min,放至室温,称定重量,用水补足减失的重量,摇匀,取上清液,经0.45 μm微孔滤膜滤过,取续滤液,即得。
分别称取对照品适量,制成含尿嘧啶0.504 mg/ml,次黄嘌呤0.326 mg/ml,黄嘌呤0.345 mg/ml,尿苷0.420 mg/ml,肌苷0.420 mg/ml,鸟苷0.338 mg/ml,腺苷0.350 mg/ml的储备液,置4 ℃储存备用。取上述对照品储备液适量,制成含尿嘧啶20.16 μg/ml,次黄嘌呤60.52 μg/ml,黄嘌呤17.25 μg/ml,尿苷21.00 μg/ml,肌苷138.2 μg/ml,鸟苷33.82 μg/ml和腺苷35.02 μg/ml的混合对照溶液。
-
取地龙配方颗粒适量,研细,取0.5 g,精密称定,置具塞锥形瓶中,精密加入双蒸水50 ml,称定重量,超声处理(功率300 W,频率40 kHz)30 min,放至室温,再称定重量,用水补足减失的重量,摇匀,取上清液,经0.45 μm微孔滤膜滤过,取续滤液,即得。
-
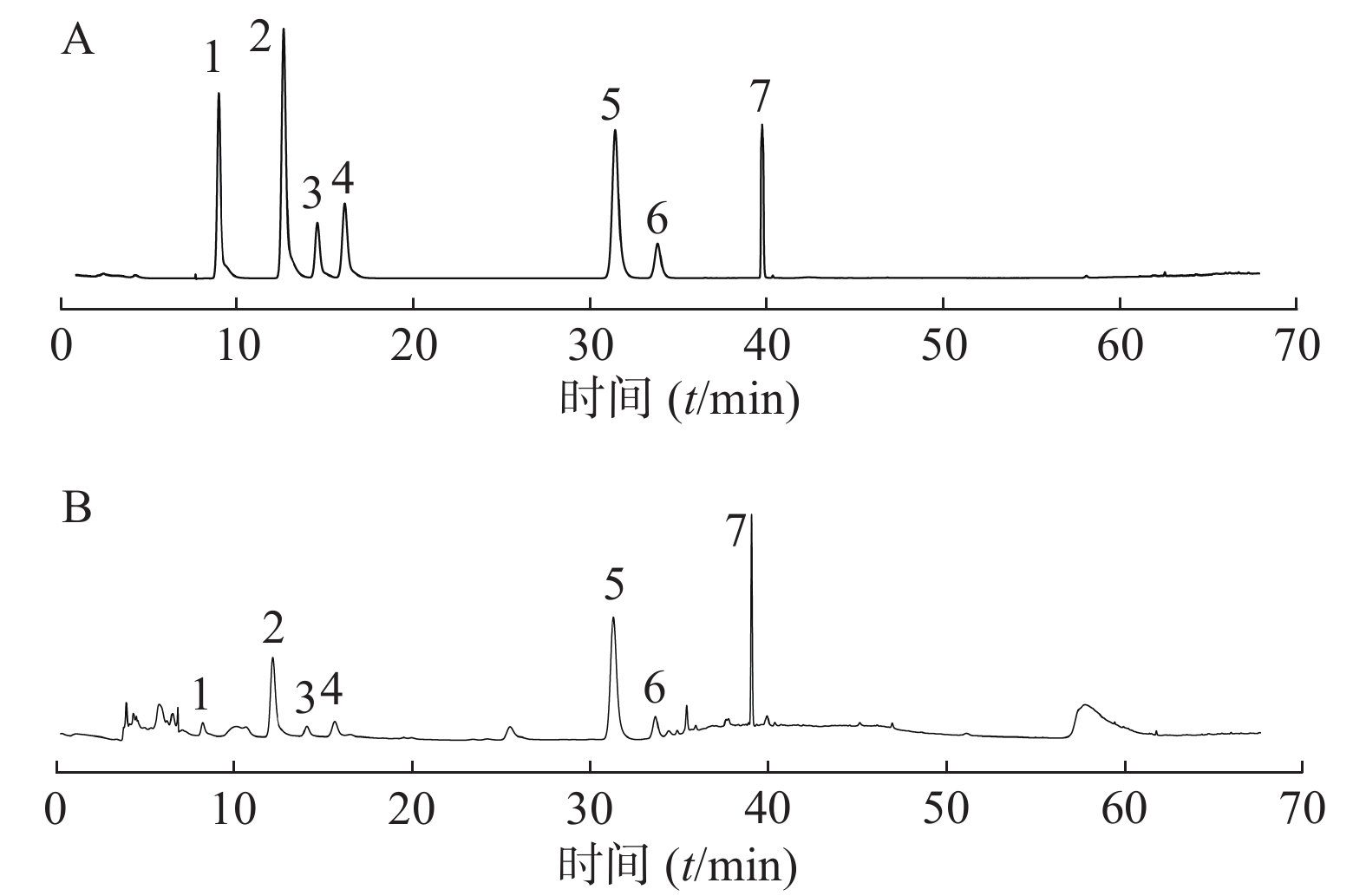
取混合对照溶液和样品S1,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样检测,记录色谱图。根据对照品的保留时间,指认了地龙配方颗粒HPLC图谱中7个主要色谱峰(图1),分别为尿嘧啶(峰1)、次黄嘌呤(峰2)、黄嘌呤(峰3)、尿苷(峰4)、肌苷(峰5)、鸟苷(峰6)和腺苷(峰7)。
-
取样品S1,按“2.2.2”项制备供试品溶液,按“2.1”项下色谱条件测定6次,以肌苷峰为参照峰,计算各共有峰相对保留时间和相对峰面积,二者RSD分别小于0.12%和2.46%,表明仪器精密度良好。
-
取样品S1,按“2.2.2”项制备供试品溶液,分别于0、4、8、12、16、24 h时按“2.1”项下色谱条件测定,以肌苷峰为参照峰,各共有峰相对保留时间和相对峰面积RSD分别小于0.16%和2.73%,表明该溶液在24 h内稳定性良好。
-
取6份样品S1,按“2.2.2”项制备供试品溶液,按“2.1”项下色谱条件测定,以肌苷峰为参照峰,各共有峰相对保留时间和相对峰面积RSD分别小于0.14%和2.52%,表明该方法重复性良好。
-
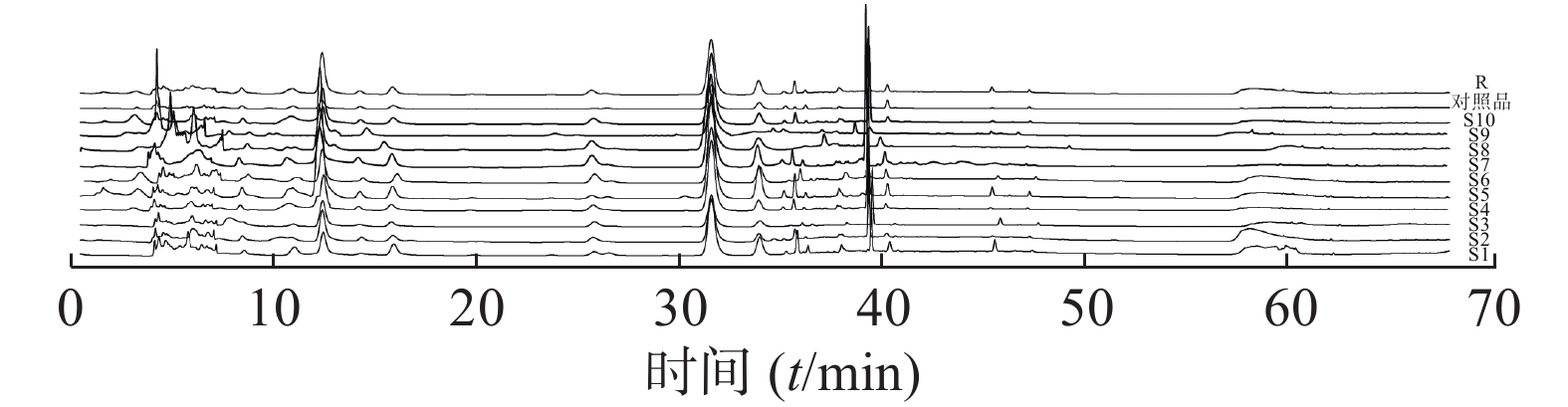
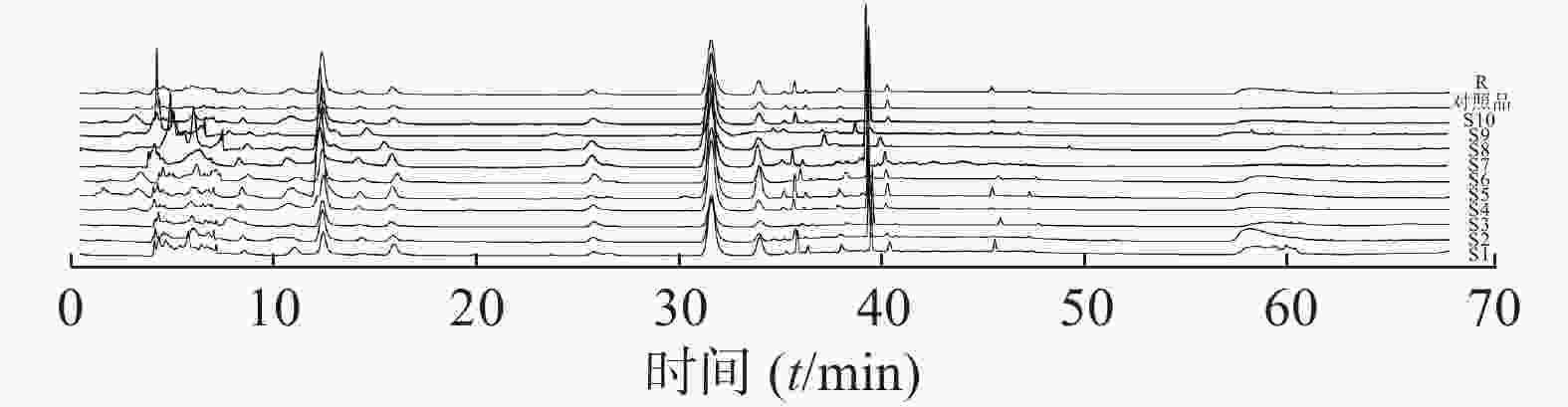
取样品(S1~S10)和对照药材,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件测定,将所得的HPLC图谱导入《中药色谱指纹图谱相似度评价系统(2012.130723版)》软件,以样品S1色谱图为参照图谱,时间窗宽度为0.1,经多点校正后,进行全谱峰匹配,采用中位数法生成对照指纹图谱R(图2)。
-
使用《中药色谱指纹图谱相似度评价系统(2012.130723版)》软件对各厂家的地龙配方颗粒和对照药材的HPLC图谱与对照特征图谱进行相似度计算。结果10批次地龙配方颗粒(S1~S10)和对照药材的HPLC指纹图谱与对照指纹图谱的相似度分别为:0.943、0.953、0.961、0.982、0.912、0.970、0.989、0.974、0.972、0.978、0.945,均大于0.912,表明不同厂家生产的地龙配方颗粒之间,及其与地龙对照药材所含成分种类较为相似,但成分含量上具有一定的差异。
-
分别取混合对照溶液0.1、0.25、1.0、2.0、4.0、6.0、8.0 ml置于10 ml容量瓶中,定容。取上述溶液和混合对照溶液适量,0.45 μm滤膜滤过,按“2.1”项下色谱条件检测(n=2),以样品浓度(X)为横坐标,峰面积(Y)为纵坐标,计算得回归方程和相关系数,结果见表2。结果各回归方程的相关系数r≥0.999 9,表明4种成分在各自浓度范围内线性关系良好。
组分 回归方程 相关系数 线性范围(μg/ml) 次黄嘌呤 Y=1.168 2X−0.004 5 0.999 9 0.605 2~60.520 0 肌苷 Y=0.605 0X+0.071 9 0.999 9 1.382 4~138.240 0 鸟苷 Y=0.705 3X+0.031 7 0.999 9 0.338 2~33.820 0 腺苷 Y=0.808 0X+0.029 1 0.999 9 0.350 2~35.020 0 -
取混合对照溶液,按“2.1”项下色谱条件连续进样6次,次黄嘌呤、肌苷、鸟苷和腺苷峰面积的RSD分别为0.19%、0.07%、0.26%、0.13%,表明仪器精密度良好。
-
取S1样品6份,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件检测,记录峰面积并计算含量。次黄嘌呤、肌苷、鸟苷和腺苷含量的RSD分别为1.94%、0.83%、0.94%、1.51%,表明该方法重复性良好。
-
取S1样品按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件分别于配制0、4、8、12、16、24 h时检测,记录峰面积。次黄嘌呤、肌苷、鸟苷和腺苷峰面积的RSD分别为0.37%、0.41%、0.47%、1.31%,表明供试品溶液在24 h之内稳定性良好。
-
精密称取S1样品0.25 g,共9份,分别精密加入相当于已知含量的50%、100%和150%的次黄嘌呤、肌苷、鸟苷和腺苷对照品溶液,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件测定,计算平均加样回收率。结果,次黄嘌呤平均回收率为97.95%,RSD为0.47%;肌苷平均回收率为102.98%,RSD为0.71%;鸟苷平均回收率为99.20%,RSD为0.26%;腺苷平均回收率为103.45%,RSD为0.59%。表明该方法准确度良好。
-
按上述供试品溶液的制备方法和测定条件,测定10批次地龙配方颗粒和对照药材中次黄嘌呤、肌苷、鸟苷和腺苷的含量,结果见表3。
样品 含量(mg/g) 总含量(mg/g) 次黄嘌呤 肌苷 鸟苷 腺苷 S1 4.457 4 7.805 0 1.596 1 0.689 2 14.547 7 S2 0.740 0 4.770 9 0.999 3 0.596 0 7.106 2 S3 1.037 5 2.323 6 0.386 8 0.814 2 4.562 1 S4 1.322 1 6.257 1 0.605 1 1.145 1 9.329 4 S5 1.070 8 4.487 3 0.993 1 2.222 9 8.774 1 S6 1.063 5 3.836 9 0.452 8 1.431 2 6.784 4 S7 1.444 6 5.775 1 0.839 6 1.077 7 9.137 0 S8 1.038 5 3.095 7 0.606 9 0.161 3 4.902 3 S9 3.672 3 6.932 4 1.332 5 0.477 3 12.414 5 S10 1.200 1 2.132 3 0.325 4 0.537 2 4.195 0 对照品 0.2526 1.8422 0.2962 0.0308 2.4218 -
中药配方颗粒是将单味中药饮片水提后经多道工序制备而成。药材产地、质量、制备工艺的不同,使产品质量存在差异。从不同厂家地龙配方颗粒中核苷类成分与含量的测定结果来看,所有配方颗粒中均含有次黄嘌呤、肌苷、鸟苷和腺苷4种核苷类成分,而且肌苷含量最高,次黄嘌呤次之,与地龙药材(饮片)中核苷类成分含量中肌苷含量最高,次黄嘌呤含量次之的报道比较相符[7-11],说明从饮片提取至颗粒成品过程中,肌苷和次黄嘌呤的相对含量未发生较大变化,也表明了该成分在颗粒和药材(饮片)中具有一定的稳定性。而从含量测定结果来看,不同厂家地龙配方颗粒中4种核苷类成分构成比差异较大,可能是水提过程中,活性酶的存在和条件的差异使核苷类成分发生了转化或分解[10,11]。
-
指纹图谱能表征样品在特定条件下的特性,对照指纹图谱能表征多个样品的共性,二者的相似度大小能反映样品之间共性的多少。本研究用不同厂家10批次配方颗粒的HPLC指纹图谱建立了对照指纹图谱,各样品的HPLC指纹图谱与对照特征图谱的相似度在0.910以上,说明各厂家的地龙配方颗粒成分组成上具有一致性。本研究还将地龙对照药材HPLC指纹图谱与配方颗粒图谱进行了相似度评价,其与对照特征图谱的相似度在0.94以上,表明配方颗粒与对照药材在成分构成上也具有高度一致性。由此可知,HPLC指纹图谱可以反映配方颗粒之间的共性与差异,也可以表征配方颗粒与对照药材间的异同。因此,HPLC指纹图谱可用于配方颗粒的质量控制与评价。
-
随着部分中药配方颗粒标准的颁布,中药配方颗粒质量将逐步完善,而合理选择质量控制成分仍是保证质量和药效的前提。目前,大部分配方颗粒仍执行省药监部门标准,经查阅多省地龙配方颗粒质量标准公示稿发现,其质量控制成分均为肌苷,但含量范围存在较大差异。地龙配方颗粒中的核苷类成分可对平喘功效进行评价,而其与清热定惊、通络、利尿等功效的关联关系仍不明确。因此,通过核苷类成分单一维度来对地龙的整体质量状况进行评价是不全面的,需要从多维度建立地龙配方颗粒的质量评价标准,使其能全面反映地龙的不同功效。
本实验在同一色谱条件下建立了地龙配方颗粒的指纹图谱,测定并比较了不同厂家地龙配方颗粒中次黄嘌呤、肌苷、鸟苷和腺苷4种成分的含量,从一定程度上反映了地龙配方颗粒的特征及内在质量。本研究所用方法简便、稳定,具备定性和定量作用,并且分析和评价能力良好,能为地龙配方颗粒的鉴别和质量评价研究提供参考。
Determination of multi-index components and quality evaluation of Dilong Formula Granules
doi: 10.12206/j.issn.2097-2024.202209086
- Received Date: 2022-09-30
- Rev Recd Date: 2023-02-27
- Available Online: 2023-09-25
- Publish Date: 2023-09-25
-
Key words:
- Dilong formula granule /
- fingerprints /
- hypoxanthine /
- inosine /
- guanosine /
- adenosine /
- quality evaluation
Abstract:
| Citation: | LI Lei, ZHANG Chengzhong, ZHANG Hanming, BU Qitao, ZHANG Lei. Determination of multi-index components and quality evaluation of Dilong Formula Granules[J]. Journal of Pharmaceutical Practice and Service, 2023, 41(9): 547-551. doi: 10.12206/j.issn.2097-2024.202209086 |







 DownLoad:
DownLoad: