-
白首乌为萝藦科(Asclepiadaceae)鹅绒藤属(Cynanchum)植物泰山白首乌(戟叶牛皮消)C. bungei Decne.、隔山消(隔山牛皮消)C. wilfordii(Maxim.)Hemsl.及滨海白首乌(耳叶牛皮消)C. auriculatum Royle ex Wight.的块根[1-2],其主要生物活性成分为苯乙酮和C21-甾体皂苷类,具有抗肿瘤、抗炎、舒张心血管,保肝、降糖和神经保护等作用[3-13]。泰山白首乌块根作为正品传统中药白首乌曾收录于1977年版《中国药典》,为泰山四大名药之首,是山东道地药材[14]。2002年版《中国中药志》记载,白首乌还包含滨海白首乌C. auriculatum和隔山消C. wilfordii。滨海白首乌在2015年被国家卫计委批准为普通食品,隔山消于2008年被《韩国药典》收载[1-2]。
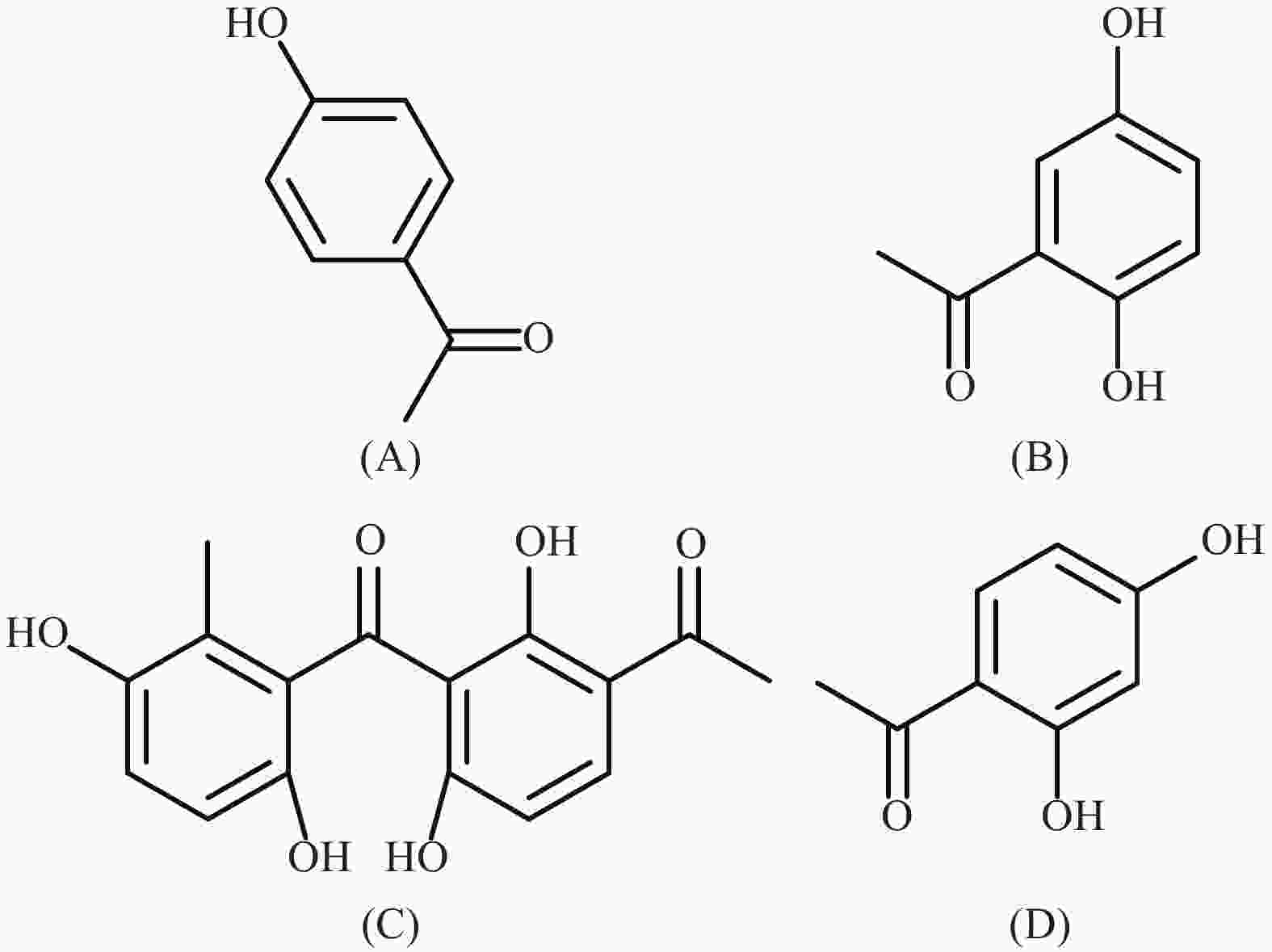
随着对白首乌生物活性研究的不断深入,其药用价值不断体现,市场需求也逐年攀升,但是白首乌药材市场存在以下问题:白首乌正品(泰山白首乌)为野生型、两年生,产量低,人工栽培极其困难,市场供应不足,因此有人将滨海白首乌和隔山消都作为白首乌正品销售,存在白首乌品种混淆的现象[15]。泰山白首乌与其近缘种滨海白首乌和隔山消的品质是否有差异,两种近缘种当作白首乌药材应用是否合理,针对这些问题,本研究收集25批白首乌类药材,建立不同产地白首乌的HPLC指纹图谱,运用HPLC指纹图谱进行质量评价。同时对不同批次的白首乌中4种苯乙酮类成分进行含量测定,结构式见图1,从而为不同品种白首乌药材的品质评价提供理论依据。
-
LC-20AD高效液相色谱仪(岛津,四元梯度系统);色谱柱Diamonsil C18柱(4.6 mm× 250 mm, 5 μm);AG285型电子分析天平(瑞士Mettler-Toledo公司)。
4-羟基苯乙酮(CAS:99-93-4,纯度≥98%)、2',4'-二羟基苯乙酮(CAS:89-84-9,纯度≥98%)、2',5'-二羟基苯乙酮(CAS490-78-8,纯度≥98%)均为国药集团提供,白首乌二苯酮为实验室自制(纯度≥98%)。
白首乌药材样品均于2018年采集或购买自国内不同地区(表1),并经山东中医药大学药学院中药鉴定教研室徐凌川教授分别鉴定为泰山白首乌C. bungei Decne.、耳叶牛皮消C. auriculatum Royle ex Wight.和隔山消C. wilfordii (Maxim.) Hemsl.,密封存放于4 ℃冰箱。
表 1 25批白首乌样品来源
样品 产地 物种 类型 S1 山东济南 泰山白首乌 栽培(两年) S2 山东临沂 泰山白首乌 栽培(两年) S3 山东泰安 泰山白首乌 栽培(一年) S4 山东临沂 隔山消 栽培(两年) S5 四川巴蜀 滨海白首乌 饮片 S6 湖南湘西 滨海白首乌 野生 S7 四川成都 滨海白首乌 饮片 S8 湖南张家界 滨海白首乌 饮片 S9 广东广州 滨海白首乌 饮片 S10 山东济南 隔山消 栽培(两年) S11 安徽阜阳 滨海白首乌 饮片 S12 四川遂宁 滨海白首乌 饮片 S13 安徽亳州 滨海白首乌 饮片 S14 江苏南京 滨海白首乌 饮片 S15 广西玉林 滨海白首乌 饮片 S16 江苏徐州 滨海白首乌 饮片 S17 贵州毕节 滨海白首乌 饮片 S18 江西南昌 滨海白首乌 饮片 S19 江苏滨海 滨海白首乌 饮片 S20 云南昆明 滨海白首乌 饮片 S21 云南大理 滨海白首乌 饮片 S22 安徽大别山 隔山消 野生 S23 四川广安 隔山消 野生 S24 陕西汉中 隔山消 野生 S25 河北安国 滨海白首乌 饮片 -
岛津LC-20AD高效液相色谱仪,Diamonsil C18 (4.6 mm×250 mm, 5 μm);流动相为甲醇-0.1%磷酸水溶液梯度洗脱(0~7 min,15%甲醇; 7~18 min,15%~24%甲醇;18~27 min,24%甲醇;27~32 min,24%~30%甲醇;32~40 min,30%甲醇;40~45 min,30%~15%甲醇),流速为1 ml/min,柱温为30 ℃,检测波长为260 nm(4-羟基苯乙酮、白首乌二苯酮、2',4'-二羟基苯乙酮)和280 nm(2',5'-二羟基苯乙酮),进样量为10 μl。
-
精确称取标准品4-羟基苯乙酮156.12 mg、2',5'-二羟基苯乙酮162.08 mg、白首乌二苯酮98.02 mg和2',4'-二羟基苯乙酮133.45 mg,置于1 000 ml容量瓶中,用甲醇溶解并稀释至刻度线,摇匀,制得混合对照品储备液。精密量取混合对照品储备液适量,用甲醇稀释10倍,得到4-羟基苯乙酮、2',5-'二羟基苯乙酮、白首乌二苯酮和2',4'-二羟基苯乙酮质量浓度分别为0.015 61、0.016 21、0.009 802、0.013 34 mg/ml的混合对照品溶液,过0.45 μm微孔滤膜作对照品溶液,置于4 ℃冰箱中备用。
-
称取白首乌样品粉末(过五号筛)约2.0 g,精密称定,置于50 ml具塞锥形瓶中,精密加入甲醇20.0 ml,密塞,称定重量,超声处理30 min,放冷,再称定重量,用甲醇补足超声过程中损失的重量,摇匀,滤过,再取续滤液,过0.45 μm微孔滤膜,即得。
-
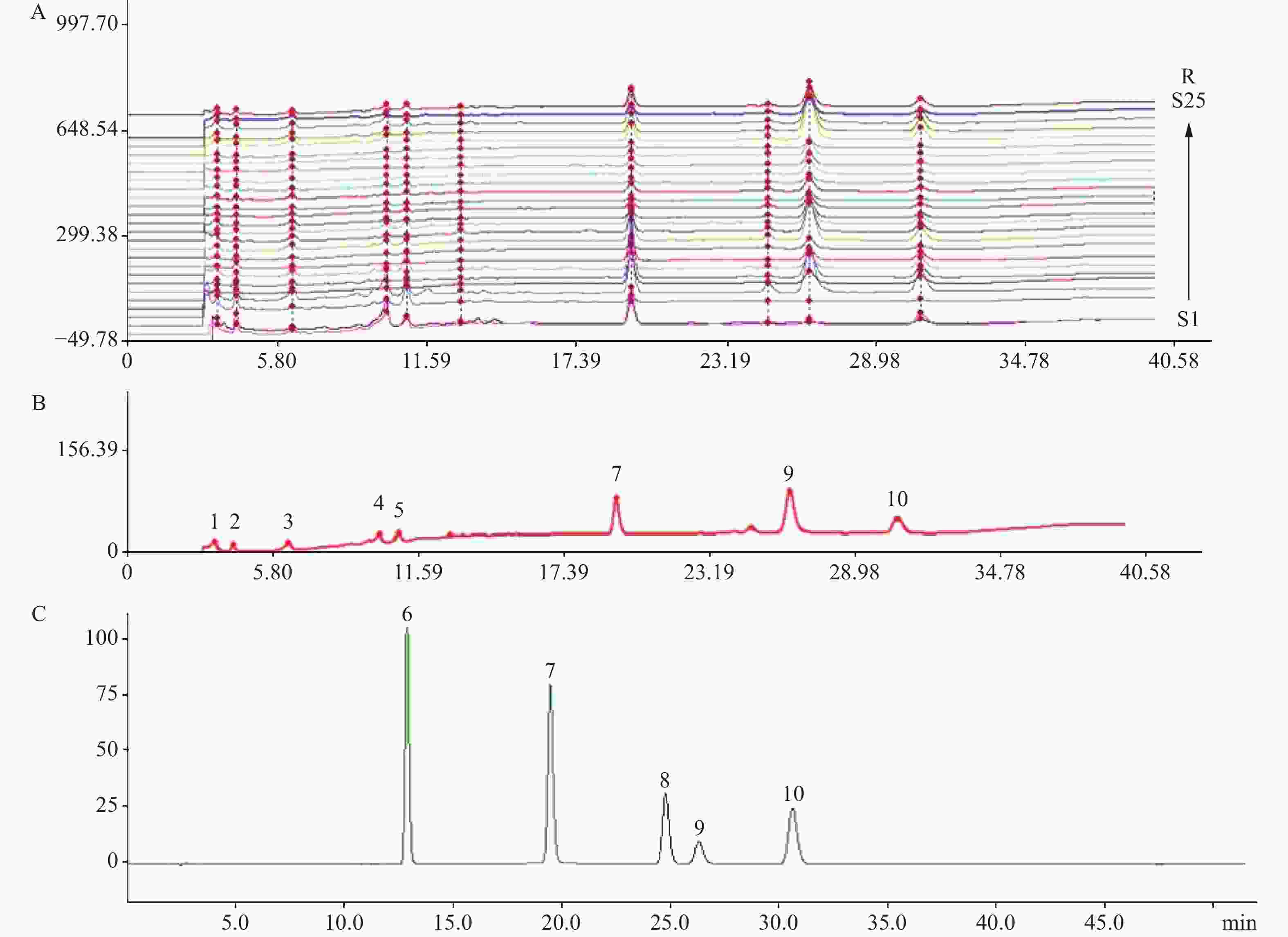
取25批白首乌样品,分别按实验方法制备供试品溶液,按“1.2”项色谱条件进行测定,得到25个样品的HPLC指纹叠加图谱及10个共有峰,并对指纹图谱中的4种苯乙酮类成分进行归属确认。其中,对4-羟基苯乙酮(保留时间19.531 min)、2',5'-二羟基苯乙酮(保留时间24.773 min)、白首乌二苯酮(保留时间26.455 min)和2',4'-二羟基苯乙酮(保留时间30.768 min)进行了指认,白首乌指纹图谱、对照图谱及混合对照品图谱如图2所示。
本研究采用国家药典委员会“中药色谱指纹图谱相似度评价系统”(2012 A版)对25批白首乌样品的HPLC指纹图谱进行数据分析处理,运用多点校正法对其指纹图谱进行相似度评价,选取S16作为参照图谱,设置“时间窗宽度”为0.6 min,以平均数的方法生成白首乌共有模式的指纹对照图谱。在相似度评价中,25批白首乌样品除了S1(产地山东济南)、S2(产地山东临沂)、S3(产地山东泰安)之外,其余相似度均在0.823~0.980之间。故可以通过相似度分析初步将S1、S2、S3这3个批次的白首乌样品归为一类,从色谱图上可以看出其某些成分含量较低,与其他产地的白首乌差距明显,结果显示均为泰山白首乌。研究结果表明,可以明显将以上3个批次的泰山白首乌与其他2个种白首乌(滨海白首乌和隔山消)区分为2大类,说明泰山白首乌与其它白首乌品种(滨海白首乌和隔山消)的化学成分差距显著。
相似度分析可以根据化学特征峰差异明显地区分泰山白首乌,但是滨海白首乌和隔山消不易区分。因此,将其他22批次白首乌样品的10个特征峰面积组成数据矩阵,导入SPSS 20.0统计软件,采用组间联接法以及欧氏距离对指纹图谱进行聚类分析,结果如图3。结果表明,化学距离为2.5,可以将22个样品分为2类,第Ⅰ类的6组均为隔山消,第Ⅱ类的16组均为滨海白首乌。聚类分析结果表明,隔山消和滨海白首乌化学成分含量差异明显。
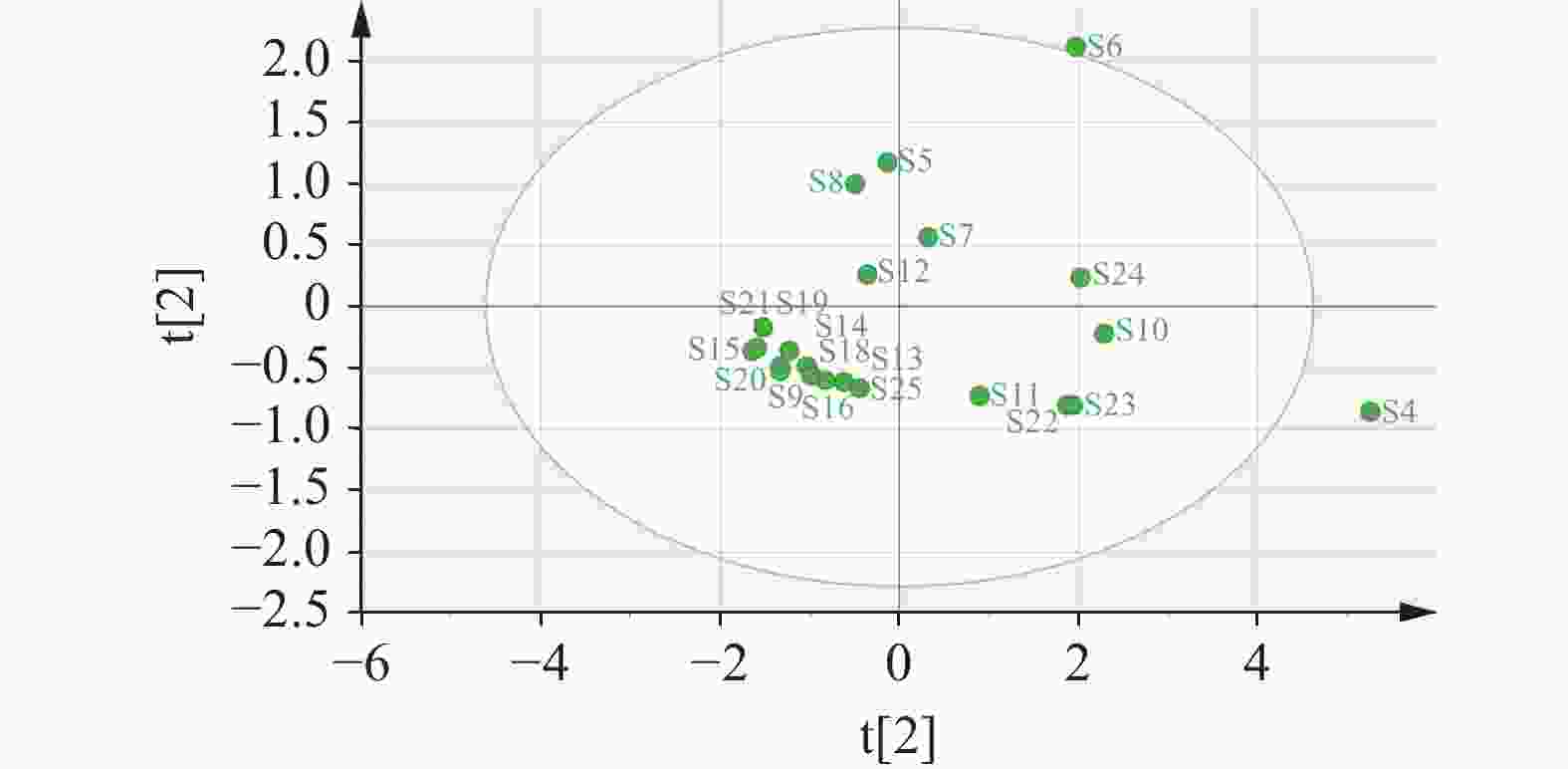
为了评价22批次样品所有成分的样品分辨能力,运用SIMCA 14.1 分析软件对其进行主成分分析,结果见图4。由PCA图可以看出,S9、S13~S21、S25聚为一类,S5、S7、S8、S12聚为一类,S10、S22、S23、S24聚为一类,与聚类分析的结果基本一致,样品之间的离散程度较大,表明样品差异性较大。
-
精密吸取混合对照品溶液1、2、4、8、16、32 μl,分别注入高效液相色谱仪,在“1.2”项实验色谱条件下,重复进样3次,测定4-羟基苯乙酮、2',5'-二羟基苯乙酮、白首乌二苯酮和2',4'-二羟基苯乙酮的峰面积,对结果进行线性回归分析,以各对照品浓度(X, μg)对峰面积(Y)绘制各标准曲线。线性关系考察结果见表2。
表 2 线性关系考察结果
成分 回归方程 R2 线性范围(μg) 4-羟基苯乙酮 Y=47 109X-22 868 0.999 9 0.015 61-0.499 6 2',5'二羟基苯乙酮 Y =23 028X-12 341 0.999 8 0.016 21-0.518 7 白首乌二苯酮 Y=15 075X-7 940.1 0.999 8 0.009 802-0.313 7 2',4'二羟基苯乙酮 Y=28 725X-12 816 0.999 9 0.013 34-0.427 0 -
按“1.2”项色谱条件对混合对照品溶液,重复进样6次,测定并计算4-羟基苯乙酮、2',5'-二羟基苯乙酮、白首乌二苯酮和2',4'-二羟基苯乙酮峰面积的RSD分别为1.35%、1.15%、1.27%和1.37%。
-
取混合对照品溶液,室温放置,按“1.2”项色谱条件,分别在0 h、2 h、4 h、6 h、12 h和24 h进样,测定并计算得到RSD分别为0.99%、0.82%、0.92%和0.88%,RSD值均小于3%,结果表明供试品溶液在24 h稳定性良好。
-
取同一批白首乌(S16)样品粉末6份,精密称定,按“1.3.2”项方法制备供试品溶液,按“1.2”项色谱条件测定,4-羟基苯乙酮、2',5'-二羟基苯乙酮、白首乌二苯酮和2',4'-二羟基苯乙酮峰面积的RSD分别为1.48%、1.84%、1.13%和2.01%,RSD值均小于3%,表明方法重复性良好。
-
精密称取同一批次白首乌(S16)样品粉末6份,每份1.0 g,按1:1质量比分别加入适量的4-羟基苯乙酮、2',5'-二羟基苯乙酮、白首乌二苯酮和2',4'-二羟基苯乙酮对照品,按照样品溶液的配制方法制备供试品溶液,在“1.2”项色谱条件下,测定并计算得到平均加样回收率(n=6)分别为97.77%、99.15%、98.81%和96.77%,RSD分别为2.07%、1.57%、1.20%和1.19%,加样回收率结果见表3。
表 3 加样回收率实验结果
成分 加样量(m/g) 样品含量(m/mg) 加对照品量(m/mg) 测得量(m/mg) 回收率(%) 平均回收率(%) RSD(%) 4-羟基苯乙酮 1.000 0 0.102 1 0.100 0 0.198 2 98.07 97.77 2.07 1.000 3 0.102 1 0.100 0 0.193 4 95.70 1.000 6 0.102 2 0.100 0 0.204 8 101.29 1.000 2 0.102 1 0.100 0 0.193 6 95.79 1.000 8 0.102 2 0.100 0 0.196 7 97.27 1.000 9 0.102 2 0.100 0 0.199 3 98.57 2',5'-二羟基苯乙酮 1.000 0 0.087 3 0.090 0 0.179 3 101.11 99.15 1.57 1.000 3 0.087 3 0.090 0 0.178 9 100.90 1.000 6 0.087 4 0.090 0 0.172 5 97.24 1.000 2 0.087 3 0.090 0 0.174 9 98.64 1.000 8 0.087 4 0.090 0 0.175 8 99.10 1.000 9 0.087 4 0.090 0 0.173 7 97.91 白首乌二苯酮 1.000 0 0.742 1 0.750 0 1.487 2 99.67 98.81 1.20 1.000 3 0.742 3 0.750 0 1.459 1 97.77 1.000 6 0.742 5 0.750 0 1.498 5 100.40 1.000 2 0.742 2 0.750 0 1.483 4 99.41 1.000 8 0.742 7 0.750 0 1.452 9 97.33 1.000 9 0.742 8 0.750 0 1.467 0 98.27 2',4'-二羟基苯乙酮 1.000 0 0.119 8 0.120 0 0.229 7 95.79 96.77 1.19 1.000 3 0.119 8 0.120 0 0.232 2 96.83 1.000 6 0.119 9 0.120 0 0.236 2 98.46 1.000 2 0.119 8 0.120 0 0.228 3 95.20 1.000 8 0.119 9 0.120 0 0.231 9 96.67 1.000 9 0.119 9 0.120 0 0.234 3 97.67 -
取25个批次的白首乌各2.0 g,按照样品溶液的配制方法制备白首乌供试品溶液,进样后记录各色谱峰的峰面积,将所得数据代入各标准曲线回归方程计算其含量,结果如表4。不同批次白首乌中各化合物成分存在显著差异,总苯乙酮类成分的含量也不同。
表 4 25批白首乌中苯乙酮类化学成分含量测定结果(n=3,mg/g)
编号 4-羟基
苯乙酮2',5'-二羟
基苯乙酮白首乌
二苯酮2',4'-二羟
基苯乙酮总苯乙酮
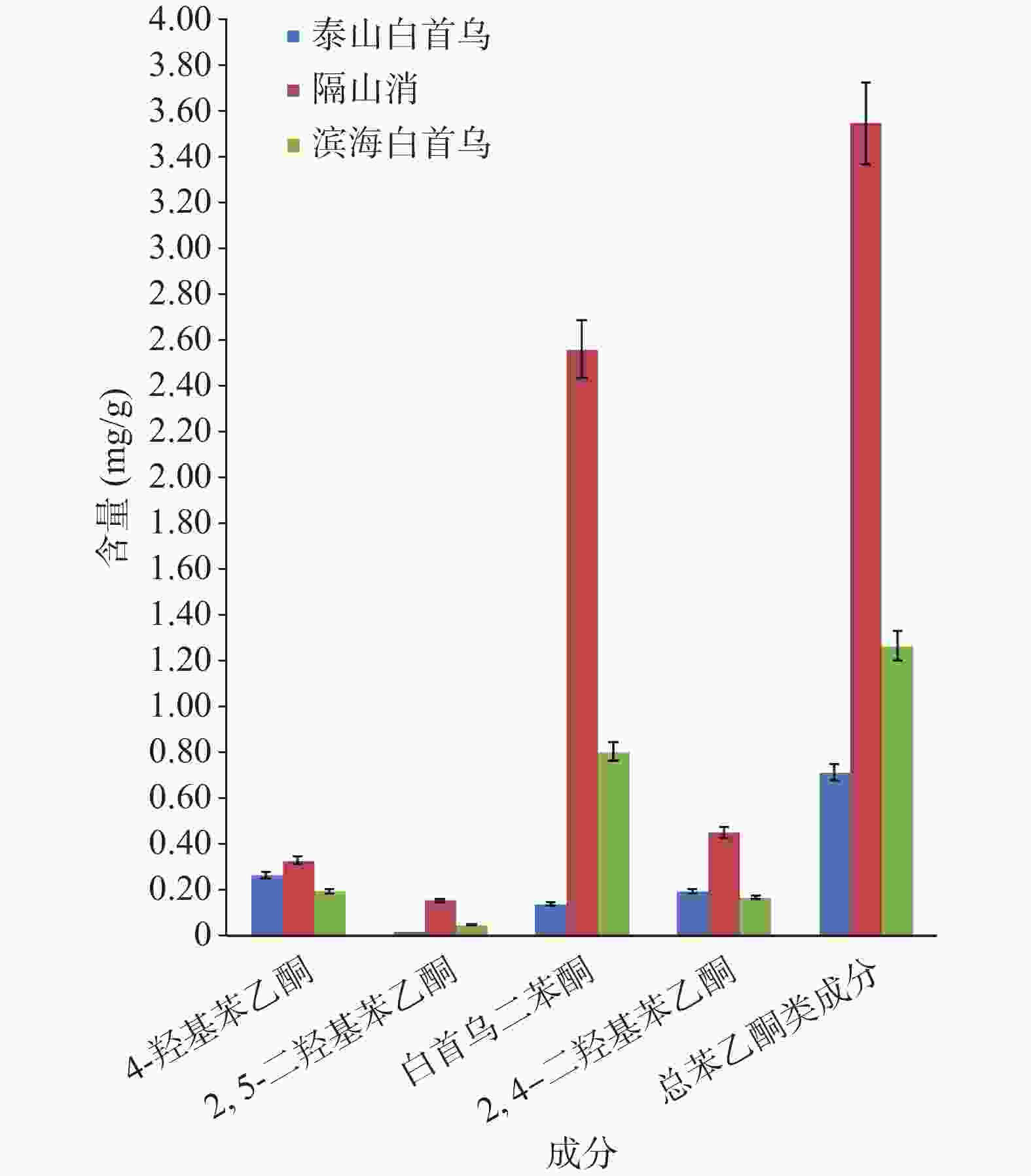
类成分S1 0.274 8 − 0.071 8 0.137 6 0.529 8 S2 0.470 9 0.045 4 0.344 7 0.384 0 1.432 3 S3 0.069 5 − 0.015 4 0.077 6 0.196 7 S4 0.497 5 0.311 1 2.808 6 0.683 7 4.373 9 S5 0.380 5 0.044 2 0.696 7 0.218 3 1.397 9 S6 0.679 3 0.065 3 1.781 4 0.360 8 2.955 1 S7 0.277 1 0.064 5 0.890 9 0.338 9 1.598 0 S8 0.290 4 0.020 4 0.650 6 0.240 4 1.247 7 S9 0.070 8 0.059 6 0.595 7 0.086 9 0.858 2 S10 0.364 5 0.155 5 2.171 7 0.402 2 3.115 2 S11 0.202 0 0.132 1 1.697 6 0.264 5 2.328 4 S12 0.210 4 0.034 2 1.192 0 0.211 9 1.676 6 S13 0.114 5 0.084 2 1.011 4 0.127 6 1.372 0 S14 0.095 0 0.070 6 0.703 3 0.110 3 1.028 3 S15 0.061 5 0.041 7 0.482 9 0.067 4 0.701 4 S16 0.102 1 0.087 3 0.742 1 0.119 8 1.066 0 S17 0.067 6 0.026 8 0.522 4 0.121 5 0.804 0 S18 0.088 8 0.067 5 0.867 2 0.105 9 1.160 1 S19 0.084 3 0.048 8 0.705 2 0.112 0 0.966 7 S20 0.064 2 0.052 6 0.742 4 0.083 5 0.955 2 S21 0.072 6 0.048 3 0.424 0 0.068 0 0.648 6 S22 0.209 0 0.113 2 2.710 9 0.401 7 3.469 3 S23 0.212 9 0.118 3 2.683 9 0.410 0 3.456 4 S24 0.392 7 0.099 8 2.466 8 0.383 3 3.359 6 S25 0.110 5 0.092 3 1.023 1 0.161 4 1.400 3 注:“−”表示含量很低,超出线性范围。 泰山白首乌历来被认为是白首乌的正品,而隔山消和滨海白首乌尽管也用作白首乌,但仍被认为是泰山白首乌的近缘品种。本研究发现,隔山消中总苯乙酮类成分的含量最高,滨海白首乌次之,泰山白首乌最低,总苯乙酮含量仅为隔山消的20%(图5)。栽培的隔山消中总苯乙酮含量与野生的相差不大,说明隔山消野生变家养驯化成功。
滨海白首乌是目前流通的主流品种,江苏滨海、湖南、安徽、四川等地均有栽培,含量差异不大,然而野生的滨海白首乌总苯乙酮含量显著高于栽培品,说明该品种的种植存在着改良的空间,可以从种植环境、栽培技术等方面予以改进。
-
本研究通过建立白首乌指纹图谱来评价白首乌药材的品质,对25批次不同白首乌的4种苯乙酮类指标性成分进行含量测定分析,并对其方法学进行考察。HPLC指纹图谱中相似度和聚类分析研究表明,泰山白首乌、滨海白首乌及隔山消的化学成分差异显著。HPLC含量测定分析发现,隔山消中总苯乙酮类的含量明显高于滨海白首乌和泰山白首乌。后续可以对3种白首乌的植物基源、化学成分、药理及毒理作用进行综合对比研究,为滨海白首乌和隔山消是否可以替代泰山白首乌作为白首乌正品药材应用,提供理论依据。
Species differences of Baishouwu based on characteristic chromatogram and content determination of acetophenones
-
摘要:
目的 建立不同产地白首乌药材的指纹图谱,并测定苯乙酮类成分含量,为不同品种白首乌药材的质量控制提供科学依据。 方法 采用HPLC-DAD法建立白首乌药材HPLC指纹图谱,同时对4种苯乙酮类成分进行含量测定。其中,色谱柱为Diamonsil C18(4.6 mm× 250 mm, 5 μm),流动相为甲醇-0.1%磷酸梯度洗脱,流速为1 ml/min,柱温为30 ℃,检测波长为260 nm(4-羟基苯乙酮、白首乌二苯酮、2',4'-二羟基苯乙酮)和280 nm(2',5'-二羟基苯乙酮)。 结果 泰山白首乌、滨海白首乌及隔山消中化学成分差异显著,隔山消中总苯乙酮类成分含量明显高于滨海白首乌和泰山白首乌。 结论 以苯乙酮类成分为评价指标,隔山消的总苯乙酮含量较高,可作为白首乌药材的优质资源。 Abstract:Objectives To provide scientific basis for the quality control of different species of Baishouwu by establishing the HPLC fingerprint of domestic of Baishouwu and determining the main active components of acetophenones. Methods HPLC-DAD method was used to determine the HPLC fingerprints of domestic of Baishouwu. Then, the content of 4 kinds of acetophenones in Baishouwu was determined. The column was Diamonsil C18(250mm×4.6mm, 5μm)with the mobile phase of methanol and 0.1% phosphoric acid at a flow rate of 1.0 ml/min. The detection wavelength of p-Hydroxyl acetophenone, baishouwu benzophenone, 2',4'-Dihydroxy acetophenone was set at 260 nm and 2',5'-Dihydroxy acetophenone at 280 nm respectively. Results The similarity and cluster analysis in HPLC fingerprint showed that the constituents were significantly different among C. bungei, C. auriculatum and C. wilfordii. The content of total acetophenones in C. wilfordii was significantly higher than that in other localities of C. auriculatum and C. bungei. Conclusions Acetophenone could be used as the evaluation index to evaluate the quality of Baishouwu in different origins. The content of total acetophenone in C. wilfordii is the highest, which could be used as the best quality resource of Baishouwu. -
Key words:
- Baishouwu /
- acetophenone /
- HPLC /
- characteristic chromatogram /
- contents determination
-
表 1 25批白首乌样品来源
样品 产地 物种 类型 S1 山东济南 泰山白首乌 栽培(两年) S2 山东临沂 泰山白首乌 栽培(两年) S3 山东泰安 泰山白首乌 栽培(一年) S4 山东临沂 隔山消 栽培(两年) S5 四川巴蜀 滨海白首乌 饮片 S6 湖南湘西 滨海白首乌 野生 S7 四川成都 滨海白首乌 饮片 S8 湖南张家界 滨海白首乌 饮片 S9 广东广州 滨海白首乌 饮片 S10 山东济南 隔山消 栽培(两年) S11 安徽阜阳 滨海白首乌 饮片 S12 四川遂宁 滨海白首乌 饮片 S13 安徽亳州 滨海白首乌 饮片 S14 江苏南京 滨海白首乌 饮片 S15 广西玉林 滨海白首乌 饮片 S16 江苏徐州 滨海白首乌 饮片 S17 贵州毕节 滨海白首乌 饮片 S18 江西南昌 滨海白首乌 饮片 S19 江苏滨海 滨海白首乌 饮片 S20 云南昆明 滨海白首乌 饮片 S21 云南大理 滨海白首乌 饮片 S22 安徽大别山 隔山消 野生 S23 四川广安 隔山消 野生 S24 陕西汉中 隔山消 野生 S25 河北安国 滨海白首乌 饮片 表 2 线性关系考察结果
成分 回归方程 R2 线性范围(μg) 4-羟基苯乙酮 Y=47 109X-22 868 0.999 9 0.015 61-0.499 6 2',5'二羟基苯乙酮 Y =23 028X-12 341 0.999 8 0.016 21-0.518 7 白首乌二苯酮 Y=15 075X-7 940.1 0.999 8 0.009 802-0.313 7 2',4'二羟基苯乙酮 Y=28 725X-12 816 0.999 9 0.013 34-0.427 0 表 3 加样回收率实验结果
成分 加样量(m/g) 样品含量(m/mg) 加对照品量(m/mg) 测得量(m/mg) 回收率(%) 平均回收率(%) RSD(%) 4-羟基苯乙酮 1.000 0 0.102 1 0.100 0 0.198 2 98.07 97.77 2.07 1.000 3 0.102 1 0.100 0 0.193 4 95.70 1.000 6 0.102 2 0.100 0 0.204 8 101.29 1.000 2 0.102 1 0.100 0 0.193 6 95.79 1.000 8 0.102 2 0.100 0 0.196 7 97.27 1.000 9 0.102 2 0.100 0 0.199 3 98.57 2',5'-二羟基苯乙酮 1.000 0 0.087 3 0.090 0 0.179 3 101.11 99.15 1.57 1.000 3 0.087 3 0.090 0 0.178 9 100.90 1.000 6 0.087 4 0.090 0 0.172 5 97.24 1.000 2 0.087 3 0.090 0 0.174 9 98.64 1.000 8 0.087 4 0.090 0 0.175 8 99.10 1.000 9 0.087 4 0.090 0 0.173 7 97.91 白首乌二苯酮 1.000 0 0.742 1 0.750 0 1.487 2 99.67 98.81 1.20 1.000 3 0.742 3 0.750 0 1.459 1 97.77 1.000 6 0.742 5 0.750 0 1.498 5 100.40 1.000 2 0.742 2 0.750 0 1.483 4 99.41 1.000 8 0.742 7 0.750 0 1.452 9 97.33 1.000 9 0.742 8 0.750 0 1.467 0 98.27 2',4'-二羟基苯乙酮 1.000 0 0.119 8 0.120 0 0.229 7 95.79 96.77 1.19 1.000 3 0.119 8 0.120 0 0.232 2 96.83 1.000 6 0.119 9 0.120 0 0.236 2 98.46 1.000 2 0.119 8 0.120 0 0.228 3 95.20 1.000 8 0.119 9 0.120 0 0.231 9 96.67 1.000 9 0.119 9 0.120 0 0.234 3 97.67 表 4 25批白首乌中苯乙酮类化学成分含量测定结果(n=3,mg/g)
编号 4-羟基
苯乙酮2',5'-二羟
基苯乙酮白首乌
二苯酮2',4'-二羟
基苯乙酮总苯乙酮
类成分S1 0.274 8 − 0.071 8 0.137 6 0.529 8 S2 0.470 9 0.045 4 0.344 7 0.384 0 1.432 3 S3 0.069 5 − 0.015 4 0.077 6 0.196 7 S4 0.497 5 0.311 1 2.808 6 0.683 7 4.373 9 S5 0.380 5 0.044 2 0.696 7 0.218 3 1.397 9 S6 0.679 3 0.065 3 1.781 4 0.360 8 2.955 1 S7 0.277 1 0.064 5 0.890 9 0.338 9 1.598 0 S8 0.290 4 0.020 4 0.650 6 0.240 4 1.247 7 S9 0.070 8 0.059 6 0.595 7 0.086 9 0.858 2 S10 0.364 5 0.155 5 2.171 7 0.402 2 3.115 2 S11 0.202 0 0.132 1 1.697 6 0.264 5 2.328 4 S12 0.210 4 0.034 2 1.192 0 0.211 9 1.676 6 S13 0.114 5 0.084 2 1.011 4 0.127 6 1.372 0 S14 0.095 0 0.070 6 0.703 3 0.110 3 1.028 3 S15 0.061 5 0.041 7 0.482 9 0.067 4 0.701 4 S16 0.102 1 0.087 3 0.742 1 0.119 8 1.066 0 S17 0.067 6 0.026 8 0.522 4 0.121 5 0.804 0 S18 0.088 8 0.067 5 0.867 2 0.105 9 1.160 1 S19 0.084 3 0.048 8 0.705 2 0.112 0 0.966 7 S20 0.064 2 0.052 6 0.742 4 0.083 5 0.955 2 S21 0.072 6 0.048 3 0.424 0 0.068 0 0.648 6 S22 0.209 0 0.113 2 2.710 9 0.401 7 3.469 3 S23 0.212 9 0.118 3 2.683 9 0.410 0 3.456 4 S24 0.392 7 0.099 8 2.466 8 0.383 3 3.359 6 S25 0.110 5 0.092 3 1.023 1 0.161 4 1.400 3 注:“−”表示含量很低,超出线性范围。 -
[1] 彭蕴茹, 丁永芳, 李友宾, 等. 白首乌研究现状[J]. 中草药, 2013, 44(3):370-378. doi: 10.7501/j.issn.0253-2670.2013.03.026 [2] 孙彦敏, 王辉, 徐凌川. 近10年白首乌研究进展[J]. 中国中医药信息杂志, 2015, 27(7):131-136. doi: 10.3969/j.issn.1005-5304.2015.07.041 [3] CHEN W H, ZHANG Z Z, BAN Y F, et al. Cynanchum bungei Decne and its two related species for “Baishouwu”: a review on traditional uses, phytochemistry, and pharmacological activities[J]. J Ethnopharmacol,2019,243:112110. doi: 10.1016/j.jep.2019.112110 [4] JIANG H W, LIN J, WANG G M, et al. Acetophenone derivatives from the root bark of Cynanchum wilfordii as potential neuroprotective agents[J]. Phytochem Lett,2018,24:179-183. doi: 10.1016/j.phytol.2018.02.002 [5] SUN Y S, LIU Z B, WANG J H, et al. Aqueous ionic liquid based ultrasonic assisted extraction of four acetophenones from the Chinese medicinal plant Cynanchum bungei Decne[J]. Ultrason Sonochem,2013,20(1):180-186. doi: 10.1016/j.ultsonch.2012.07.002 [6] HAN L, ZHOU X P, YANG M M, et al. Ethnobotany, phytochemistry and pharmacological effects of plants in genus Cynanchum Linn. (Asclepiadaceae)[J]. Molecules,2018,23(5):1194. doi: 10.3390/molecules23051194 [7] 谢凯强. 隔山消化学成分及生物活性研究[D]. 贵阳: 贵州大学, 2017. [8] LEE M K, YEO H, KIM J, et al. Protection of rat hepatocytes exposed to CCl4 in-vitro by cynandione A, a biacetophenone from Cynanchum wilfordii[J]. J Pharm Pharmacol,2000,52(3):341-345. [9] YANG S B, LEE S M, PARK J H, et al. Cynandione A from Cynanchum wilfordii attenuates the production of inflammatory mediators in LPS-induced BV-2 microglial cells via NF-κB inactivation[J]. Biol Pharm Bull,2014,37(8):1390-1396. doi: 10.1248/bpb.b13-00939 [10] KIM S H, LEE T H, LEE S M, et al. Cynandione A attenuates lipopolysaccharide-induced production of inflammatory mediators via MAPK inhibition and NF-κB inactivation in RAW264.7 macrophages and protects mice against endotoxin shock[J]. Exp Biol Med (Maywood),2015,240(7):946-954. doi: 10.1177/1535370214558022 [11] KOO H J, SOHN E H, PYO S, et al. An ethanol root extract of Cynanchum wilfordii containing acetophenones suppresses the expression of VCAM-1 and ICAM-1 in TNF-α-stimulated human aortic smooth muscle cells through the NF-κB pathway[J]. Int J Mol Med,2015,35(4):915-924. doi: 10.3892/ijmm.2015.2112 [12] JIANG H W, GU S S, CAO L, et al. Potential hypoglycemic effect of acetophenones from the root bark of Cynanchum wilfordii[J]. Nat Prod Res,2019,33(16):2314-2321. doi: 10.1080/14786419.2018.1443100 [13] HA D T, TRUNG T N, HIEN T T, et al. Selected compounds derived from Moutan Cortex stimulated glucose uptake and glycogen synthesis via AMPK activation in human HepG2 cells[J]. J Ethnopharmacol,2010,131(2):417-424. doi: 10.1016/j.jep.2010.07.010 [14] 王光辉, 王琦, 时元林. 泰山四大名药[J]. 山东中医杂志, 2006, 25(3):203-204. doi: 10.3969/j.issn.0257-358X.2006.03.028 [15] 刘琪, 谷巍, 杨兵, 等. 基于ITS2序列的滨海白首乌及其近缘种DNA分子鉴定[J]. 中草药, 2018, 49(24):5901-5909. doi: 10.7501/j.issn.0253-2670.2018.24.025 -




 下载:
下载: