-
近年来,真菌感染尤其是念珠菌感染日益严重,感染率居高不下[1]。并且由于免疫损伤以及长期住院患者增多,又进一步增加了机会性和系统性真菌感染的可能[2]。临床上常见的抗真菌药物如氟康唑等,由于真菌耐药性和毒性等问题,限制了其使用。因此,研发新的抗菌药物已经成为迫切任务。
天然产物的抑菌作用受到了普遍关注,天然产物以其结构新颖、生物活性强、毒性低等特点,成为了近年寻找抗真菌新药及其先导化合物的研究热点。没食子酸(gallic acid,GA),又称五倍子酸或棓酸,即3,4,5-三羟基苯甲酸,是一种存在于五倍子和漆树等植物中的有机酸。文献报道[3-7]其具有抗菌、抗病毒、抗肿瘤等作用。近期有研究[3]报道,没食子酸于体内外表现出较好的抗真菌作用。课题组以此为基础,对没食子酸进行结构改造,合成了系列没食子酰哌嗪类化合物,并进一步评价了其单独及协同抗真菌作用,为进一步研究和开发没食子类抗真菌化合物提供了基础。
-
所使用原料均为市售分析纯或化学纯试剂。核磁共振氢谱(HNMR)和碳谱由Bruker AVANCE II 300或600型核磁共振仪测得;质谱(MS)由Q-Tof micro (ESI-MS)或Finingan LCQ Deca XP MAX质谱仪测定。
-
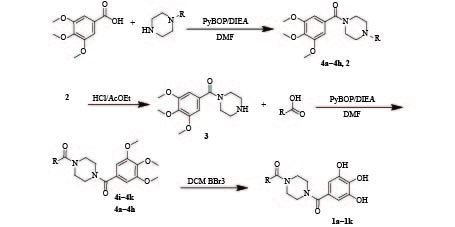
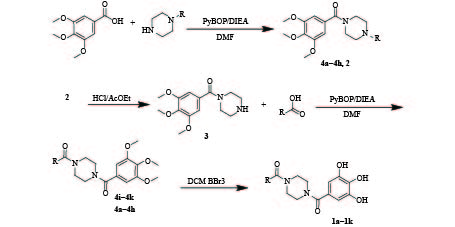
以三甲氧基没食子酸为原料,在PyBOP/DIEA存在下与Boc保护哌嗪或取代哌嗪缩合得到化合物4a~4h或2,然后2在HCl/乙酸乙酯溶液中脱Boc得到三甲氧基没食子酰哌嗪(3),3再与不同取代苯甲酸在PyBOP/DIEA条件下缩合得到化合物4i~4k。最后,4a~4k采用BBr3脱甲基得到目标化合物1a~1k。具体合成路线见图1。
-
取三甲氧基苯甲酸2.1 g(10 mmol),BOC保护的哌嗪盐酸盐2.2 g(12 mmol),PyBOP 7.8 g(15 mmol),DIEA 1.9 g(15 mmol),置入于100 ml茄形瓶中,加入20 ml干燥DMF,室温搅拌4~6 h,TCL监测反应,待原料点消失后,将反应液倒入到200 ml冰水中,终止反应,并继续搅拌1 h。然后将析出的固体过滤,用乙醇重结晶,得到中间体3.1 g(8 mmol),收率80%。化合物4a~4h也采用此法合成。
-
取中间体(2)1 g(5.3 mmol),加入到HCl-乙酸乙酯溶液中常温搅拌约3 h,TCL监测反应,待原料点消失后过滤,烘干,得到中间体三甲氧基没食子酰哌嗪(3)1.4 g,直接用于下一步反应。
-
取三甲氧基没食子酰哌嗪(3)0.5 g(1.8 mmol)、2,3-二氯苯甲酸0.35 g(1.85 mmol),其余方法同化合物2的合成。得到目标化合物 0.56 g(1.26 mmol),收率70%。化合物4j~4n的合成均采用此法。
-
取4a 0.56 g(1.26 mmol),在无水、无氧条件下,置于100 ml的三口瓶,加入20 ml干燥二氯甲烷,然后降温至(–20~–30)℃,加入5 ml 2 mol/L的三溴化硼二氯甲烷溶液,然后缓慢升温至室温,并搅拌反应10 h。再将反应液降温至–10 ℃,然后缓慢加入200 ml冰水猝灭反应,再室温搅拌1 h,如有固体析出,过滤。滤液用分液漏斗分出二氯甲烷层,并用10 ml水,洗2次,Na2SO4干燥,然后除去硫酸钠,再除去溶剂,得到的固体和前面的滤饼合并,并经乙醇重结晶,放置于烘箱烘干。得到最终产物273 mg,收率(0.67 mmol)53%。其余1类化合物均采用此方法合成。
-
选用ATCC标准株Candida albicans为质控菌,临床耐药株Candida albicans 103 为实验菌株。氟康唑注射液(批号:A447404)购自美国辉瑞公司。采用美国国家临床实验室标准委员会(CLSI)推荐的标准化抗真菌敏感性实验方法[8]测试体外抗真菌活性,以目标化合物MIC80作为判断终点。
-
共合成化合物11个,经检索,均未见文献报道。所有目标化合物均经1H NMR和MS确证结构,相关理化数据见表1。目标化合物的抗真菌活性实验结果见表2。
表 1 目标化合物的结构及核磁共振图谱和质谱数据
化合物 结构式 MS[M+H]+ 1H NMR(δ, ppm) 1a 
425 (300 MHz, CDCl3) 7.20 (q, J=8.1 Hz, 2H), 6.99 (d, J=7.5 Hz, 1H), 6.68 (s, 2H), 4.09 – 3.59 (m, 13H), 3.09 (s, 4H) 1b 
383 1H NMR (600 MHz, MeOD) δ 7.30 – 7.19 (m, 2H), 7.14 – 7.06 (m, 1H), 6.48 (s, 2H), 3.81 (s, 4H), 3.06 (s, 4H) 1c 
390 (600 MHz, Chloroform-d) δ 7.19 (t, J=8.1 Hz, 1H), 6.92 – 6.86 (m, 2H), 6.82 – 6.79 (m, 1H), 6.65 (s, 2H), 3.87 (d, J=4.9 Hz, 9H), 3.86 – 3.33 (m, 4H), 3.21 (s, 4H) 1d 
348 (600 MHz, Methanol-d4) δ 7.19 (t, J=8.1 Hz, 1H), 6.96 (t, J=2.2 Hz, 1H), 6.92 – 6.87 (m, 1H), 6.85 – 6.79 (m, 1H), 6.46 (s, 2H), 3.75 (s, 4H), 3.21 (s, 4H) 1e 
390 (300 MHz, Chloroform-d) δ 7.43 – 7.35 (m, 1H), 7.29 – 7.20 (m, 1H), 7.08 – 6.96 (m, 2H), 6.67 (d, J=1.9 Hz, 2H), 4.12 (d, J=5.1 Hz, 2H), 3.88 (dd, J=5.4, 1.8 Hz, 9H), 3.67 (d, J=15.9 Hz, 2H), 3.08 (s, 4H) 1f 
348 (600 MHz, Methanol-d4) δ 7.39 (dd, J=7.9, 1.5 Hz, 1H), 7.28 (s, 1H), 7.17 – 7.15 (m, 1H), 7.05 (d, J=1.5 Hz, 1H), 6.48 (s, 2H), 3.84 (d, J=47.0 Hz, 4H), 3.06 (s, 4H) 1g 
386 (300 MHz, Chloroform-d) δ 7.26 (d, J=8.0 Hz, 1H), 7.21 (d, J=8.2 Hz, 1H), 6.66 (s, 3H), 6.54 (d, J=8.2 Hz, 1H), 3.87 (d, J=2.9 Hz, 12H), 3.80 (s, 4H), 3.24 (s, 4H) 1h 
386 (600 MHz, Chloroform-d) δ 6.91 (s, 2H), 6.85 (d, J=9.0 Hz, 2H), 6.65 (s, 2H), 3.87 (s, 9H), 3.86 (s, 3H), 3.77 (s, 4H), 3.08 (s, 4H) 1i 
452 (300 MHz, Chloroform-d) δ 7.52 (d, J=8.0 Hz, 1H), 7.30 (s, 1H), 7.21 (d, J=1.5 Hz, 1H), 6.63 (s, 2H), 3.87 (d, J=2.9 Hz, 9H), 3.81 – 3.14 (m, 8H) 1j 
483 (300 MHz, Chloroform-d) δ 7.40 (d, J=2.5 Hz, 1H), 7.21 (dd, J=8.8, 2.5 Hz, 1H), 6.97 (d, J=8.8 Hz, 1H), 6.63 (s, 2H), 4.80 (s, 2H), 3.88 (s, 9H), 3.69 (s, 4H), 3.66 (s, 4H) 1k 
410 (300 MHz, Chloroform-d) δ 7.72 (d, J=15.3 Hz, 1H), 7.62 – 7.48 (m, 2H), 7.44 – 7.32 (m, 3H), 6.87 (d, J=15.4 Hz, 1H), 6.65 (s, 2H), 3.88 (d, J=1.5 Hz, 9H), 3.75 (s, 8H) -
目标化合物采用PyBop/DIEA条件下与相应的哌嗪缩合而得到,该反应操作和条件简便易行,收率较高。脱甲基保护采用三溴化硼的方法,副反应少,收率较好。文献报道了没食子酸体外对敏感念珠菌的MIC值在12.5~100 μg/ml[3];体内模式实验中,腹腔注射80 mg/(kg·d)可以显著提高系统性真菌感染的治愈率[3]。因此,没食子酸是一个较好的先导化合物。活性测试所选用的2株白色念珠菌临床分离株均为耐药菌株(氟康唑的MIC80 > 64 μg/ml)。合成的目标化合物中,所有没食子酰哌嗪(1b,1d和1f)化合物无论单用还是联用,均对2株耐药菌表现出较好的抗真菌活性,并且这些活性化合物在单用时MIC80≤64 μg/ml,均显著优于没食子酸的抗真菌活性(MIC80>64 μg/ml)。初步的构效关系表明,没食子酸的游离三羟基结构是重要的药效团,如果羟基被保护起来,活性将会丧失。本研究结果为进一步设计具有抗真菌作用的没食子酸衍生物提供了理论和物质基础。
表 2 目标化合物的体外抗真菌活性
化合物 C. albicans 103 (μg/ml) 分级抑制浓度指数(FICI) 单用 联用1) 1a >64 >64 >1 1b 16 4 0.254 1c >64 >64 >1 1d 64 4 0.141 1e >64 >64 >1 1f 32 8 0.254 1g >64 >64 >1 1h >64 >64 >1 1i >64 >64 >1 1j >64 >64 >1 1k >64 >64 >1 没食子酸 >64 4 0.035 注:1)表示与氟康唑(8 μg/ml)联用。
Study on synthesis and antifungal activities of galloyl piperazine derivatives
-
摘要:
目的 设计合成没食子酰哌嗪衍生物,考察其对耐药真菌的抗菌活性。 方法 以三甲氧基没食子酸为原料,在PyBOP/DIEA存在下与哌嗪反应得到中间体,在脱保护后与相应的酸缩合,最后脱甲基得到目标化合物。采用美国国家临床实验室标准委员会(CLSI)推荐方法,将目标化合物对2株临床分离的耐药白色念珠菌株进行体外抗真菌活性试验,进而与氟康唑(8 μg/ml)联用,开展协同抗真菌活性试验。 结果 共合成了11个化合物,其中6个化合物表现出优于没食子酸的抗真菌活性。 结论 没食子酰哌嗪可以提高没食子酸的抗真菌活性,没食子酸酰结构是重要的药效团,若引入桂皮酸或2,3-二氯苯甲酸可以进一步提高活性。 Abstract:Objective To design, synthesize and measure antifungal activities of galloyl piperazine derivatives. Methods Trimethoxyl gallic acid was used as starting material, reacted with piperazine in the presence of PyBOP/DIEA to afford the intermediates. The target compounds were obtained through the reaction with corresponding acids after deprotection gave. The antifungal activities of the target compounds were evaluated by FLC-resistant Candida albican isolated according to the CLSI recommended method. Results 11 target compounds were synthesized and six of them showed more potent antifungal activities than gallic acid. Conclusion Galloyl piperazine derivatives could enhance antifungal activities. Galloyl moiety was an important pharmacophore, which could improve antifungal activities with the introduction of cinnamic acid and 2,3-dichlorobenzoic acid. -
Key words:
- gallic acid /
- antifungals /
- synergy /
- synthesis
-
表 1 目标化合物的结构及核磁共振图谱和质谱数据
化合物 结构式 MS[M+H]+ 1H NMR(δ, ppm) 1a 425 (300 MHz, CDCl3) 7.20 (q, J=8.1 Hz, 2H), 6.99 (d, J=7.5 Hz, 1H), 6.68 (s, 2H), 4.09 – 3.59 (m, 13H), 3.09 (s, 4H) 1b 383 1H NMR (600 MHz, MeOD) δ 7.30 – 7.19 (m, 2H), 7.14 – 7.06 (m, 1H), 6.48 (s, 2H), 3.81 (s, 4H), 3.06 (s, 4H) 1c 390 (600 MHz, Chloroform-d) δ 7.19 (t, J=8.1 Hz, 1H), 6.92 – 6.86 (m, 2H), 6.82 – 6.79 (m, 1H), 6.65 (s, 2H), 3.87 (d, J=4.9 Hz, 9H), 3.86 – 3.33 (m, 4H), 3.21 (s, 4H) 1d 348 (600 MHz, Methanol-d4) δ 7.19 (t, J=8.1 Hz, 1H), 6.96 (t, J=2.2 Hz, 1H), 6.92 – 6.87 (m, 1H), 6.85 – 6.79 (m, 1H), 6.46 (s, 2H), 3.75 (s, 4H), 3.21 (s, 4H) 1e 390 (300 MHz, Chloroform-d) δ 7.43 – 7.35 (m, 1H), 7.29 – 7.20 (m, 1H), 7.08 – 6.96 (m, 2H), 6.67 (d, J=1.9 Hz, 2H), 4.12 (d, J=5.1 Hz, 2H), 3.88 (dd, J=5.4, 1.8 Hz, 9H), 3.67 (d, J=15.9 Hz, 2H), 3.08 (s, 4H) 1f 348 (600 MHz, Methanol-d4) δ 7.39 (dd, J=7.9, 1.5 Hz, 1H), 7.28 (s, 1H), 7.17 – 7.15 (m, 1H), 7.05 (d, J=1.5 Hz, 1H), 6.48 (s, 2H), 3.84 (d, J=47.0 Hz, 4H), 3.06 (s, 4H) 1g 386 (300 MHz, Chloroform-d) δ 7.26 (d, J=8.0 Hz, 1H), 7.21 (d, J=8.2 Hz, 1H), 6.66 (s, 3H), 6.54 (d, J=8.2 Hz, 1H), 3.87 (d, J=2.9 Hz, 12H), 3.80 (s, 4H), 3.24 (s, 4H) 1h 386 (600 MHz, Chloroform-d) δ 6.91 (s, 2H), 6.85 (d, J=9.0 Hz, 2H), 6.65 (s, 2H), 3.87 (s, 9H), 3.86 (s, 3H), 3.77 (s, 4H), 3.08 (s, 4H) 1i 452 (300 MHz, Chloroform-d) δ 7.52 (d, J=8.0 Hz, 1H), 7.30 (s, 1H), 7.21 (d, J=1.5 Hz, 1H), 6.63 (s, 2H), 3.87 (d, J=2.9 Hz, 9H), 3.81 – 3.14 (m, 8H) 1j 483 (300 MHz, Chloroform-d) δ 7.40 (d, J=2.5 Hz, 1H), 7.21 (dd, J=8.8, 2.5 Hz, 1H), 6.97 (d, J=8.8 Hz, 1H), 6.63 (s, 2H), 4.80 (s, 2H), 3.88 (s, 9H), 3.69 (s, 4H), 3.66 (s, 4H) 1k 410 (300 MHz, Chloroform-d) δ 7.72 (d, J=15.3 Hz, 1H), 7.62 – 7.48 (m, 2H), 7.44 – 7.32 (m, 3H), 6.87 (d, J=15.4 Hz, 1H), 6.65 (s, 2H), 3.88 (d, J=1.5 Hz, 9H), 3.75 (s, 8H) 表 2 目标化合物的体外抗真菌活性
化合物 C. albicans 103 (μg/ml) 分级抑制浓度指数(FICI) 单用 联用1) 1a >64 >64 >1 1b 16 4 0.254 1c >64 >64 >1 1d 64 4 0.141 1e >64 >64 >1 1f 32 8 0.254 1g >64 >64 >1 1h >64 >64 >1 1i >64 >64 >1 1j >64 >64 >1 1k >64 >64 >1 没食子酸 >64 4 0.035 注:1)表示与氟康唑(8 μg/ml)联用。 -
[1] ALI I, SATTI N K, DUTT P, et al. Hydroxychavicol: A phytochemical targeting cutaneous fungal infections[J]. Sci Rep,2016,6:37867. doi: 10.1038/srep37867 [2] PERUSQUÍA-ORTIZ A M, VÁZQUEZ-GONZÁLEZ D, BONIFAZ A. Opportunistic filamentous mycoses: aspergillosis, mucormycosis, phaeohyphomycosis and hyalohyphomycosis[J]. JDDG,2012,10(9):611-621. [3] LI Z J, LIU M, DAWUTI G, et al. Antifungal activity of Gallic acid in vitro and in vivo[J]. Phytother Res,2017,31(7):1039-1045. doi: 10.1002/ptr.5823 [4] AGLAN H A, AHMED H H, EL-TOUMY S A, et al. Gallic acid against hepatocellular carcinoma: An integrated scheme of the potential mechanisms of action from in vivo study[J]. Tumour Biol,2017,39(6):101042831769912. [5] LIMA K G, KRAUSE G C, SCHUSTER A D, et al. Gallic acid reduces cell growth by induction of apoptosis and reduction of IL-8 in HepG2 cells[J]. Biomed Pharmacother,2016,84:1282-1290. doi: 10.1016/j.biopha.2016.10.048 [6] TAKAI E, HIRANO A, SHIRAKI K. Effects of alkyl chain length of gallate on self-association and membrane binding[J]. J Biochem,2011,150(2):165-171. doi: 10.1093/jb/mvr048 [7] WANG Z Y, XIA Q, LIU X, et al. Phytochemistry, pharmacology, quality control and future research of forsythia suspensa (thunb.) vahl: A review[J]. J Ethnopharmacol,2018,210:318-339. doi: 10.1016/j.jep.2017.08.040 [8] CLSI. Reference Method for Broth Dilution Antifungal Susceptibility Testing of Yeasts, Approved Standard M27-A3.3rd ed. Wayne, PA: Clinical and Laboratory Standards Institute, 2008. -




 下载:
下载: